为了测定某碳酸钠样品中杂质氯化钠的质量分数,晓萍进行了三次实验。实验数据如下表,请根据数据完成计算:
(1)第______ 次实验氯化钙和碳酸钠恰好完全反应;
(2)碳酸钠样品中碳酸钠的质量分数是____ ?
(3)把氯化钙和碳酸钠恰好完全反应后的混合物过滤,所得溶液溶质质量分数为____ 。
| 编号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 49 | 49 | 69 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
(1)第
(2)碳酸钠样品中碳酸钠的质量分数是
(3)把氯化钙和碳酸钠恰好完全反应后的混合物过滤,所得溶液溶质质量分数为
更新时间:2019-12-17 22:53:34
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】金属及金属材料广泛应用于生产、生活及科学实验。
(1)下列生活用品,利用金属导电性的是_________ 。(填字母代号)
a.铁锅 b.铜导线 c.金饰品 d.铝箔包装纸
(2)国产大型客机C919机壳采用铝锂合金,合金比纯金属的优点是_________ (写出一点即可)。
(3)如图为工业炼铁的流程。请回答下列问题:_________ 。
②高炉中一氧化碳还原氧化铁的化学方程式为_________ 。
(4)铁在潮湿的空气中易生锈。如图是某探究小组设计的铁钉生锈条件的探究实验,要达到实验目的,还需要补充的实验是_________ 。
①滤渣中含有的物质是_________ 。
②蓝色溶液变无色的原因是_________ (用化学方程式表示)。
(6)黄铜是铜和锌的合金,常用来制造机械零件、仪表等。化学小组想测定黄铜中铜的含量,将10g黄铜粉末放入烧杯中,加入足量稀盐酸,完全反应后生成0.1g氢气。请计算黄铜样品中铜的质量分数。
(1)下列生活用品,利用金属导电性的是
a.铁锅 b.铜导线 c.金饰品 d.铝箔包装纸
(2)国产大型客机C919机壳采用铝锂合金,合金比纯金属的优点是
(3)如图为工业炼铁的流程。请回答下列问题:

②高炉中一氧化碳还原氧化铁的化学方程式为
(4)铁在潮湿的空气中易生锈。如图是某探究小组设计的铁钉生锈条件的探究实验,要达到实验目的,还需要补充的实验是

①滤渣中含有的物质是
②蓝色溶液变无色的原因是
(6)黄铜是铜和锌的合金,常用来制造机械零件、仪表等。化学小组想测定黄铜中铜的含量,将10g黄铜粉末放入烧杯中,加入足量稀盐酸,完全反应后生成0.1g氢气。请计算黄铜样品中铜的质量分数。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】围绕酸、碱、盐构建大单元学习主题,能更好地建立知识间的内在联系。
【活动一】探究酸和碱的化学性质
(1)下列有关酸和碱的说法中,正确的是__________ 。
a.敞口放置浓硫酸,溶液浓度变大 b.稀盐酸能使紫色石蕊溶液变蓝色
c.氢氧化钙固体可用于检验铵态氮肥 d.打开盛浓盐酸的试剂瓶,瓶口有白烟产生
(2)稀盐酸与氢氧化钠溶液反应时溶液的 pH变化曲线如图1所示。__________________ 。
②已知中和反应是放热反应,则图1中__________ 点的温度最高。
【活动二】探究 NaOH溶液与CO2的反应
(3)如图2所示,将少量氢氧化钠溶液倒入盛有CO2的塑料软瓶中,立即拧紧瓶盖, 一段时间后,观察到_____________ 。__________ ?
【活动三】探究粗盐中的可溶性杂质
(5)为探究粗盐溶液中可能含有的CaCl2、MgCl2、Na2SO4 等可溶性杂质,进行如下实验。
①向粗盐溶液中滴加过量NaOH溶液,未出现明显现象。
②向①的溶液中滴加过量 Na2CO3溶液,产生白色沉淀,过滤。
③向②的滤液中滴加过量BaCl2溶液,产生白色沉淀,过滤。
④向③的沉淀中滴加足量稀盐酸,观察到沉淀__________ 的现象。
结论:粗盐溶液中含有________________ 和 Na2SO4等可溶性杂质。
【活动四】利用相关知识解决实际问题
(6)工业碳酸钠中通常含有一定量杂质(杂质不发生反应),为测定某样品中碳酸钠的质量 分数,取25 g 该样品,加入足量稀盐酸,充分反应后得到8.8g气体,则该样品中碳酸 钠的质量分数是多少?
【活动一】探究酸和碱的化学性质
(1)下列有关酸和碱的说法中,正确的是
a.敞口放置浓硫酸,溶液浓度变大 b.稀盐酸能使紫色石蕊溶液变蓝色
c.氢氧化钙固体可用于检验铵态氮肥 d.打开盛浓盐酸的试剂瓶,瓶口有白烟产生
(2)稀盐酸与氢氧化钠溶液反应时溶液的 pH变化曲线如图1所示。

②已知中和反应是放热反应,则图1中
【活动二】探究 NaOH溶液与CO2的反应
(3)如图2所示,将少量氢氧化钠溶液倒入盛有CO2的塑料软瓶中,立即拧紧瓶盖, 一段时间后,观察到

【活动三】探究粗盐中的可溶性杂质
(5)为探究粗盐溶液中可能含有的CaCl2、MgCl2、Na2SO4 等可溶性杂质,进行如下实验。
①向粗盐溶液中滴加过量NaOH溶液,未出现明显现象。
②向①的溶液中滴加过量 Na2CO3溶液,产生白色沉淀,过滤。
③向②的滤液中滴加过量BaCl2溶液,产生白色沉淀,过滤。
④向③的沉淀中滴加足量稀盐酸,观察到沉淀
结论:粗盐溶液中含有
【活动四】利用相关知识解决实际问题
(6)工业碳酸钠中通常含有一定量杂质(杂质不发生反应),为测定某样品中碳酸钠的质量 分数,取25 g 该样品,加入足量稀盐酸,充分反应后得到8.8g气体,则该样品中碳酸 钠的质量分数是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】碳和碳的化合物在自然界中广泛存在。请回答:
(1)金刚石和石墨是两种常见的碳单质,其物理性质相差很大的原因是_______ 。
(2)下列是有关C、CO、CO2三种物质的说法:
①三种物质都含有碳元素,都可以燃烧
②CO、CO2都是没有颜色、没有气味的气体
③CO2可用于光合作用,CO可用于人工降雨
④CO2能产生温室效应,CO易与血液中的血红蛋白结合引起中毒
⑤CO2可用来灭火,CO可用作燃料
上述说法中正确的是_______ 。
A ①②③ B ②③④ C ②④⑤ D ①③⑤
(3)以下是常用的实验装置图:

①写出实验室用A装置制取氧气的化学方程式_______ 。
②装置B或装置C都可用来制二氧化碳,其中装置C的优点是_____ 。在装置E中按照气流方向,补充导管_____ 。
③若用D装置收集H2,则H2应从_______ (填“a”或“b”)端通入。
④用装置C制取气体,在反应过程中,用弹簧夹夹住导管上的橡皮管,过一会反应就会停止,其原因是什么?____
(4)实验室常用石灰石和稀盐酸制取二氧化碳,取含碳酸钙80%的石灰石12.5g和足量稀盐酸完全反应(石灰石中的杂质不溶于水,也不与稀盐酸反应),求生成二氧化碳的质量____ 。
(1)金刚石和石墨是两种常见的碳单质,其物理性质相差很大的原因是
(2)下列是有关C、CO、CO2三种物质的说法:
①三种物质都含有碳元素,都可以燃烧
②CO、CO2都是没有颜色、没有气味的气体
③CO2可用于光合作用,CO可用于人工降雨
④CO2能产生温室效应,CO易与血液中的血红蛋白结合引起中毒
⑤CO2可用来灭火,CO可用作燃料
上述说法中正确的是
A ①②③ B ②③④ C ②④⑤ D ①③⑤
(3)以下是常用的实验装置图:

①写出实验室用A装置制取氧气的化学方程式
②装置B或装置C都可用来制二氧化碳,其中装置C的优点是
③若用D装置收集H2,则H2应从
④用装置C制取气体,在反应过程中,用弹簧夹夹住导管上的橡皮管,过一会反应就会停止,其原因是什么?
(4)实验室常用石灰石和稀盐酸制取二氧化碳,取含碳酸钙80%的石灰石12.5g和足量稀盐酸完全反应(石灰石中的杂质不溶于水,也不与稀盐酸反应),求生成二氧化碳的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】金属材料与人们的生活密切相关。
(1)①《梦溪笔谈》中记载,“古人以剂钢为刃,柔铁为茎干,不尔则多断折”。“剂钢”和“柔铁”都是铁的合金,它们的硬度比纯铁的________ (选填“大”或“小”);
②《本草纲目拾遗》中记载:“舶上铁丝……日久起销(锈)……所刮下之销末,名铁线粉”。铁有良好的________ 性,能拉成铁丝。铁丝“日久起销”的原因是铁与___________ 同时接触的结果;
(2)闪锌矿(主要成分为 )经过焙烧得锌焙砂,锌焙砂主要含
)经过焙烧得锌焙砂,锌焙砂主要含 、
、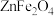 ,以及少量
,以及少量 、
、 ,工业上用其制备金属锌,具体过程如图所示。
,工业上用其制备金属锌,具体过程如图所示。 与
与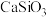 类似,可以看作是复合氧化物。若
类似,可以看作是复合氧化物。若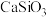 可以写为
可以写为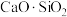 的形式,那么推测
的形式,那么推测 可以写为
可以写为__________ 的形式。
②溶液B中的阳离子有__________ (写离子符号)。
③反应b的化学方程式是__________________ 。
④假设闪锌矿中杂质不含硫元素且整个过程硫元素没有损失,那么生产____  金属锌的同时能获得
金属锌的同时能获得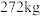 硫酸钙。
硫酸钙。
(3)湿法冶金是利用溶液中的置换反应。向一定质量 和
和 的混合溶液中加入
的混合溶液中加入 ,溶液质量与加入
,溶液质量与加入 的质量变化趋势如图所示。下列说法不正确的是______(填编号)。
的质量变化趋势如图所示。下列说法不正确的是______(填编号)。
(1)①《梦溪笔谈》中记载,“古人以剂钢为刃,柔铁为茎干,不尔则多断折”。“剂钢”和“柔铁”都是铁的合金,它们的硬度比纯铁的
②《本草纲目拾遗》中记载:“舶上铁丝……日久起销(锈)……所刮下之销末,名铁线粉”。铁有良好的
(2)闪锌矿(主要成分为
 )经过焙烧得锌焙砂,锌焙砂主要含
)经过焙烧得锌焙砂,锌焙砂主要含 、
、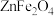 ,以及少量
,以及少量 、
、 ,工业上用其制备金属锌,具体过程如图所示。
,工业上用其制备金属锌,具体过程如图所示。
 与
与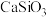 类似,可以看作是复合氧化物。若
类似,可以看作是复合氧化物。若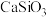 可以写为
可以写为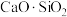 的形式,那么推测
的形式,那么推测 可以写为
可以写为②溶液B中的阳离子有
③反应b的化学方程式是
④假设闪锌矿中杂质不含硫元素且整个过程硫元素没有损失,那么生产
 金属锌的同时能获得
金属锌的同时能获得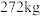 硫酸钙。
硫酸钙。(3)湿法冶金是利用溶液中的置换反应。向一定质量
 和
和 的混合溶液中加入
的混合溶液中加入 ,溶液质量与加入
,溶液质量与加入 的质量变化趋势如图所示。下列说法不正确的是______(填编号)。
的质量变化趋势如图所示。下列说法不正确的是______(填编号)。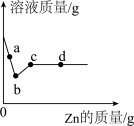
| A.a点溶液中溶质只有2种 | B.c点溶液中溶质为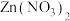 |
C.若取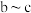 段之间的溶液,滴加稀盐酸,有白色沉淀产生 段之间的溶液,滴加稀盐酸,有白色沉淀产生 | D.取d点的固体,加入稀盐酸,有气泡产生 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】基于实验事实进行证据推理是化学学科重要的思维方式。
(1)实验室中有两瓶失去标签的无色溶液,只知道是稀盐酸和稀硫酸中的一种,丽丽同学想利用老师提供的几种物质,通过化学方法确定这两种无色溶液各是什么。
①丽丽同学所选择的鉴别试剂最好是下列选项中的___________ (填选项序号之一)。
A.酚酞溶液 B.石蕊溶液 C.BaCl2溶液 D.NaCl溶液
②用两只洁净的试管分别取两种无色溶液各少量,各加入适量所选的鉴别试剂,若观察到一只试管中有___________ (填现象),可证明这只试管中所取的溶液是稀硫酸。
(2)已知某无色溶液A中的溶质是KNO3和Na2CO3,另有一固体样品B,其中可能含有CuO和CuCl2或两者之一,按下图所示进行探究实验,出现的现象如图中所述(设过程中所发生的反应都恰好完全反应)。

试根据实验过程和发生的现象,填写以下空白:
①气体C通入紫色石蕊试液,试液变___________ 色。
②白色沉淀H的化学式为___________ 。
③溶液D中大量存在的酸根阴离子是___________ (写离子符号)。
④写出步骤II中发生的一个反应的化学方程式___________ 。
(1)实验室中有两瓶失去标签的无色溶液,只知道是稀盐酸和稀硫酸中的一种,丽丽同学想利用老师提供的几种物质,通过化学方法确定这两种无色溶液各是什么。
①丽丽同学所选择的鉴别试剂最好是下列选项中的
A.酚酞溶液 B.石蕊溶液 C.BaCl2溶液 D.NaCl溶液
②用两只洁净的试管分别取两种无色溶液各少量,各加入适量所选的鉴别试剂,若观察到一只试管中有
(2)已知某无色溶液A中的溶质是KNO3和Na2CO3,另有一固体样品B,其中可能含有CuO和CuCl2或两者之一,按下图所示进行探究实验,出现的现象如图中所述(设过程中所发生的反应都恰好完全反应)。

试根据实验过程和发生的现象,填写以下空白:
①气体C通入紫色石蕊试液,试液变
②白色沉淀H的化学式为
③溶液D中大量存在的酸根阴离子是
④写出步骤II中发生的一个反应的化学方程式
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐3】绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一:《唐本草》和《天工开物》等古籍都记载中国焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色料、重要着色剂。
材料二:公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
(1)某研究性学习小组用下图装置对绿矾的焙烧反应进行探究。_______ 。
②装置C的作用是_______ 。
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入_______ (填试剂名称),溶液呈红色,说明“矾精”中含有H+;检验“矾精”中含有 的方法为
的方法为_______ 。
(2)某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)
①绿矾的相对分子质量为_______ 。
②高纯度铁红中铁元素的质量分数为_______ 。
(3)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略:硫酸沸点338℃,硝酸沸点85.5℃)如图:
材料一:《唐本草》和《天工开物》等古籍都记载中国焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色料、重要着色剂。
材料二:公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
(1)某研究性学习小组用下图装置对绿矾的焙烧反应进行探究。

②装置C的作用是
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入
 的方法为
的方法为(2)某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)
①绿矾的相对分子质量为
②高纯度铁红中铁元素的质量分数为
(3)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略:硫酸沸点338℃,硝酸沸点85.5℃)如图:

| A.该流程涉及2种基本反应类型 |
| B.制备步骤,H2SO4与HNO3的化学计量系数之比为1:1 |
| C.吸收、制备步骤,铁质仪器易被腐蚀 |
您最近一年使用:0次



