生铁和钢都是由铁和碳组成的合金,生铁中碳的含量为2%~4.3%,钢中碳的含量为 0.03%~2%,为测定某种铁合金中碳的含量,小王同学取一定质量的合金样品盛放在烧杯中,并向其中逐滴加入稀盐酸至恰好完全反应,实验数据如下表所示:
注:碳既不溶于水也不与稀盐酸发生反应。
请根据相关信息完成下列计算:
(1)生成氢气的质量为_____ g;
(2)样品中碳的质量分数(计算结果保留到0.1%);
(3)反应后得到氯化亚铁质量。
| 烧杯质量 | 样品的质量 | 稀盐酸的质量 | 烧杯+剩余物的总质量 |
| 50g | 11.6g | 94.8g | 156g |
请根据相关信息完成下列计算:
(1)生成氢气的质量为_____ g;
(2)样品中碳的质量分数(计算结果保留到0.1%);
(3)反应后得到氯化亚铁质量。
更新时间:2020-01-05 22:56:19
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某同学为了测定生锈的铁制品中氧化铁的质量分数进行了如下实验:取生锈的铁制品样品20g,加入200g稀盐酸,充分反应,观察到烧杯中的固体物质全部消失。
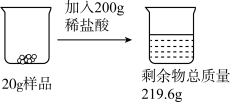
(1)根据题中信息_____ (填“能”或“不能”)计算稀盐酸的溶质质量分数。
(2)计算生锈的铁制品中氧化铁的质量分数____ 。

(1)根据题中信息
(2)计算生锈的铁制品中氧化铁的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下(烧杯质量均相同):
请回答下列问题:
(1) 同学取用的稀硫酸和样品恰好完全反应;
(2)计算黄铜样品中锌的质量分数。
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸质量 | 139g | 129g | 129g |
| 加入黄铜样品质量 | 20g | 24g | 20g |
| 充分反应后,烧杯+剩余物质质量 | 158.8g | 152.8g | 148.8g |
请回答下列问题:
(1) 同学取用的稀硫酸和样品恰好完全反应;
(2)计算黄铜样品中锌的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】为了测定某铁样品中铁的质量分数(杂质中不含铁元素,杂质不溶于水,不与其它物质反应),某化学小组进行了如下实验。请根据信息回答下列问题:______ 。
(2)该铁样品中铁的质量分数为______ 。
(3)根据已知条件,列出求解生成FeSO4质量(x)的比例式______ 。
(4)a的数值为______ 。
(5)若用70%的硫酸溶液(密度为1.4g/cm3)配制上述实验中所用的稀硫酸,配制过程中,量取70%的硫酸溶液时,应选择量程为______ (填“10”或“20”或“25”)mL的量筒。
(6)钢铁厂用1000t含Fe2O380%的赤铁矿石,理论上可以炼出上述铁样品的质量为______ 。

(2)该铁样品中铁的质量分数为
(3)根据已知条件,列出求解生成FeSO4质量(x)的比例式
(4)a的数值为
(5)若用70%的硫酸溶液(密度为1.4g/cm3)配制上述实验中所用的稀硫酸,配制过程中,量取70%的硫酸溶液时,应选择量程为
(6)钢铁厂用1000t含Fe2O380%的赤铁矿石,理论上可以炼出上述铁样品的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组的同学为了测定某铁铜合金样品中铁的质量分数,在实验室称取了该铁铜合金15g放入烧杯中,分两次加入稀硫酸,充分反应。测得实验数据如下表。
(1)两次加稀硫酸后,生成氢气的总质量是______________ g。
(2)计算该样品中铁的质量分数。(温馨提示: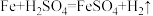 )
)
| 加稀硫酸的次数 | 第一次 | 第二次 |
| 加稀硫酸的质量/g | 50 | 50 |
| 生成气体的质量/g | 0.2 | 0.1 |
(2)计算该样品中铁的质量分数。(温馨提示:
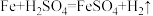 )
)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】化学学习小组的同学要测定某Cu-Zn合金中铜的质量分数,做了如下实验:将100.0g稀硫酸,加入盛有10.0g合金样品的烧杯中,恰好完全反应,反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示。试计算:
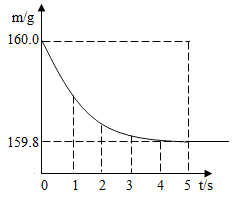
(1)反应生成H2的质量为 。
(2)计算反应后所得溶液中硫酸锌的质量分数。(写出解答过程,精确到0.1%)

(1)反应生成H2的质量为 。
(2)计算反应后所得溶液中硫酸锌的质量分数。(写出解答过程,精确到0.1%)
您最近一年使用:0次



