实验室中有一瓶未知浓度的硫酸铜熔液,为了测定其定量组成,小宇同学设计并进行了如图一所示的探究实验,图二为反应生成沉淀的质量与滴入氢氧化钠溶液质量的变化关系,发生反应的化学方程式为:
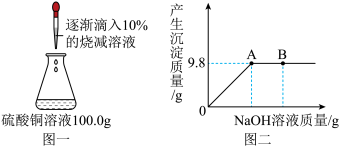
根据上述信息,请你回答下列问题:
(1)图2中B点对应溶液里所含的溶质为______ (填化学式)。
(2)试计算:该硫酸铜溶液的溶质质量分数是多少______ ?


根据上述信息,请你回答下列问题:
(1)图2中B点对应溶液里所含的溶质为
(2)试计算:该硫酸铜溶液的溶质质量分数是多少
更新时间:2020-01-12 08:59:25
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】现有 H2SO4与 CuSO4的混合溶液,为了分析混合溶液中 H2SO4与 CuSO4的质量分数, 设计了如图所示的实验方案(注:硫酸铜溶液略显酸性)。
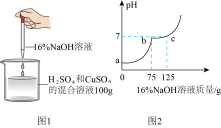
(1) c点表示混合溶液与 NaOH 恰好反应完全,此点溶液中的溶质为________(写化学式)。
(2)与硫酸铜溶液反应的氢氧化钠溶液的质量为____________g;请计算该混合溶液中 CuSO4的溶质质量分数(写出具体计算过程)。
(3)若在 100g 混合溶液中不断加入上述氢氧化钠的溶液,请你画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图(标出曲线中必要的数据)_________。

(4)在图2所示的曲线中,b-c段表示的溶液pH稍小于7,其原因是___________。

(1) c点表示混合溶液与 NaOH 恰好反应完全,此点溶液中的溶质为________(写化学式)。
(2)与硫酸铜溶液反应的氢氧化钠溶液的质量为____________g;请计算该混合溶液中 CuSO4的溶质质量分数(写出具体计算过程)。
(3)若在 100g 混合溶液中不断加入上述氢氧化钠的溶液,请你画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图(标出曲线中必要的数据)_________。

(4)在图2所示的曲线中,b-c段表示的溶液pH稍小于7,其原因是___________。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐2】梧州市某化学兴趣小组检测某硫酸厂排放的废液中硫酸的含量,取废液样品100g,逐滴加入4%的NaOH溶液,溶液的pH随加入NaOH溶液质量变化如图所示(假设废液中其它成分均为中性,且不和NaOH反应)。

请计算:
(1)H2O的相对分子质量=______。
(2)该废液中硫酸的质量分数。______(结果精确到0.01%)

请计算:
(1)H2O的相对分子质量=______。
(2)该废液中硫酸的质量分数。______(结果精确到0.01%)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂主要成分为碳酸钙,现将100g盐酸分成5等份,逐次加到用40g该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象。请根据有关信息回答问题:

(1)a的数值为___,该品牌补钙药剂中CaCO3的质量分数是___。
(2)求该盐酸中溶质的质量分数。(写出计算过程,计算结果保留一位小数)
(3)如果在配制该盐酸时质量分数偏小了,对该品牌补钙药剂中CaCO3的质量分数计算是否有影响。你的看法是___。
| 序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 35 | 30 | 25 | 20 | a |

(1)a的数值为___,该品牌补钙药剂中CaCO3的质量分数是___。
(2)求该盐酸中溶质的质量分数。(写出计算过程,计算结果保留一位小数)
(3)如果在配制该盐酸时质量分数偏小了,对该品牌补钙药剂中CaCO3的质量分数计算是否有影响。你的看法是___。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】为测定某化工厂排放的废水中CuSO4的含量,化学小组同学取150g废水,平均分为三份,每一份样品均按如图所示装置进行实验,实验数据记录如下表:

试分析并计算:
(1)50g废水完全反应时,所得沉淀的质量为____ g。
(2)计算该化工厂废水中CuSO4的质量分数_____ 。

| 实验1 | 实验2 | 实验3 | |
| 样品质量/g | 50 | 50 | 50 |
| NaOH溶液质量/g | 20 | 40 | 60 |
| m/g | 44.9 | 49.8 | 49.8 |
(1)50g废水完全反应时,所得沉淀的质量为
(2)计算该化工厂废水中CuSO4的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】工业盐酸中通常含少量FeC13而呈黄色,小亮为测定某工业盐酸中HCl的含量进行如下实验,取某工业盐酸50g,滴加溶质质量分数为20%的NaOH溶液,反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表,请根据表格和图象完成下列问题:
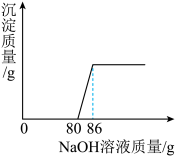
(1)开始没有产生沉淀的原因是_____。
(2)m=______(结果保留两位小数)。
(3)该工业盐酸中HCl的质量分数为_____。
| 加入NaOH溶液的质量/g | 25 | 50 | 75 | 100 |
| 所得溶液的质量/g | 75 | 100 | 125 | m |

(1)开始没有产生沉淀的原因是_____。
(2)m=______(结果保留两位小数)。
(3)该工业盐酸中HCl的质量分数为_____。
您最近一年使用:0次




