实验室中加热氯酸钾和二氧化锰的混合物可制得氧气,在制备过程中,MnO2在混合物中的质量分数随加热时间的变化图像如图所示。
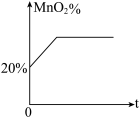
(1)当MnO2的质量分数达到多少时不再产生氧气?
(2)当反应完毕后剩余固体的质量为10.5g,则产生氧气多少克?

(1)当MnO2的质量分数达到多少时不再产生氧气?
(2)当反应完毕后剩余固体的质量为10.5g,则产生氧气多少克?
更新时间:2020-01-14 09:17:08
|
【知识点】 含杂质的化学方程式计算解读
相似题推荐
计算题
|
较难
(0.4)
【推荐1】取碳酸钠和氯化钠的固体13.6 g与质量为73 g的稀盐酸恰好完全反应,产生4.4g二氧化碳。计算:(可能用到的相对原子质量:C-12 O-16 Na-23.5 Cl-35.5)
(1)固体混合物中氯化钠的质量;
(2)该稀盐酸中氯化氢的质量分数。
(1)固体混合物中氯化钠的质量;
(2)该稀盐酸中氯化氢的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】实验室有部分已变质为碳酸钠的氢氧化钠样品,质量为1.86 g。某实验小组将此样品加入水中完全溶解,配成100 g溶液,然后向其中缓慢滴加9.8%的稀硫酸,搅拌使气体全部逸出。滴加过程中,相关数据如表所示。
回答下列问题。
(1)第______ 次测定时,溶液中只有一种溶质。表中m=______ 。
(2)第4次测定时,溶液中的阳离子有______ 。
(3)计算样品中碳酸钠的质量分数。(结果精确到1%)
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 滴加稀硫酸总质量/g | 0 | 10 | 20 | 30 | 40 |
| 溶液总质量/g | 100 | 110 | 119.56 | 129.56 | m |
| 溶液pH | 13.3 | 10.2 | 7.0 | 0.9 | 0.8 |
(1)第
(2)第4次测定时,溶液中的阳离子有
(3)计算样品中碳酸钠的质量分数。(结果精确到1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】某补钙剂(有效成分为碳酸钙,其他成分不含钙元素)的说明书的部分信息如图所示。为了检验该产品,现将20片该药剂制成的粉末,放入40g稀盐酸中HCl与补钙品有效成分刚好完全反应(其他成分不与盐酸反应),反应后称得剩余物的质量为55.6g。试计算:

(1)生成二氧化碳气体的质量是_____;
(2)该品牌补钙剂每片含的CaCO3质量为_______;(写出计算过程)
(3)通过计算分析。该补钙剂说明书中“含钙量”的数值________(填“符合”、“不符合”)标示,若不符合,应将“含钙量”的数值修改为__________。

(1)生成二氧化碳气体的质量是_____;
(2)该品牌补钙剂每片含的CaCO3质量为_______;(写出计算过程)
(3)通过计算分析。该补钙剂说明书中“含钙量”的数值________(填“符合”、“不符合”)标示,若不符合,应将“含钙量”的数值修改为__________。
您最近一年使用:0次



