某实验小组为研究碳酸钠和碳酸氢钠混合物的组成做了以下实验:充分加热10.0 g样品至恒重,剩余固体质量为6.9 g。
查阅资料已知:碳酸氢钠受热易分解,2NaHCO3 Na2CO3+H2O+CO2↑,碳酸钠受热不易分解。 计算:
Na2CO3+H2O+CO2↑,碳酸钠受热不易分解。 计算:
(1)生成二氧化碳的质量____;
(2)混合物中碳酸钠的质量分数。
查阅资料已知:碳酸氢钠受热易分解,2NaHCO3
 Na2CO3+H2O+CO2↑,碳酸钠受热不易分解。 计算:
Na2CO3+H2O+CO2↑,碳酸钠受热不易分解。 计算:(1)生成二氧化碳的质量____;
(2)混合物中碳酸钠的质量分数。
更新时间:2020-04-05 01:59:45
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】如图为“XX”钙片商品标签图,请根据标签的有关信息完成下列各题。

(1)每片钙片中含钙元素的质量至少为___克
(2)小红同学为测定其中碳酸钙的含量标注是否属实,她取出10片钙片,研碎后放入小烧杯中,再加入50g稀盐酸,在T0至T3时间段,测得反应剩余物的质量变化如下:
①生成的二氧化碳的质量是___克;
②通过计算判断该钙片中碳酸钙的含量标注是否属实___。(写出计算过程)

(1)每片钙片中含钙元素的质量至少为___克
(2)小红同学为测定其中碳酸钙的含量标注是否属实,她取出10片钙片,研碎后放入小烧杯中,再加入50g稀盐酸,在T0至T3时间段,测得反应剩余物的质量变化如下:
| 时间 | T0 | T1 | T2 | T3 |
| 反应剩余物质量(g) | 70 | 65 | 63.4 | 63.4 |
①生成的二氧化碳的质量是___克;
②通过计算判断该钙片中碳酸钙的含量标注是否属实___。(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某纯碱样品中含有少量NaCl,小红同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,充分反应后得到溶液质量为324.2g,反应产生的气体质量与稀盐酸的用量关系如图所示,请回答下列问题:
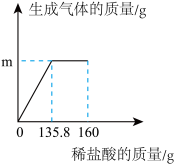
(1)Na2CO3的化学式量为______ ;
(2)生成二氧化碳的质量m=______ g;
(3)恰好完全反应时溶液中溶质的质量分数。(写出计算过程,结果保留到0.1%)

(1)Na2CO3的化学式量为
(2)生成二氧化碳的质量m=
(3)恰好完全反应时溶液中溶质的质量分数。(写出计算过程,结果保留到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】现有l00g 8%的NaOH溶液,通过计算回答下列有关问题:
(1)若用该溶液吸收CO2,最多可以生成Na2CO3多少克?____(写出详细计算过程)
(2)当NaOH全部转化成为Na2CO3后,Na2CO3还会继续与CO2、H2O发生反应:Na2CO3+CO2+H2O=2NaHCO3,直至Na2CO3完全反应完。请在如图画出利用l00g8%的NaOH溶液吸收CO2与生成NaHCO3的曲线。____
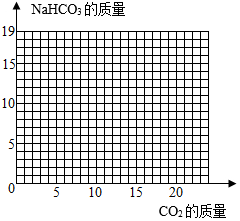
(3)现有三种溶液:①100g8%NaOH溶液、②100g8%NaOH溶液吸收CO2转化为Na2CO3溶液、③100g8%NaOH溶液吸收过量CO2转化为NaHCO3溶液,分别用相同质量分数的硫酸与上述三种溶液恰好完全反应,需要的硫酸的质量_____(选填“相等”或“不相等”),原因是_____。
(1)若用该溶液吸收CO2,最多可以生成Na2CO3多少克?____(写出详细计算过程)
(2)当NaOH全部转化成为Na2CO3后,Na2CO3还会继续与CO2、H2O发生反应:Na2CO3+CO2+H2O=2NaHCO3,直至Na2CO3完全反应完。请在如图画出利用l00g8%的NaOH溶液吸收CO2与生成NaHCO3的曲线。____

(3)现有三种溶液:①100g8%NaOH溶液、②100g8%NaOH溶液吸收CO2转化为Na2CO3溶液、③100g8%NaOH溶液吸收过量CO2转化为NaHCO3溶液,分别用相同质量分数的硫酸与上述三种溶液恰好完全反应,需要的硫酸的质量_____(选填“相等”或“不相等”),原因是_____。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】现有20g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的质量与加入的稀盐酸的质量关系如图所示(石灰石样品中的杂质不溶于水,也不发生反应)。
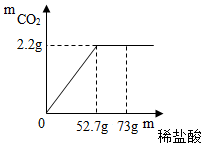
(1)该样品与稀盐酸反应产生二氧化碳的质量为 g。
(2)该石灰石样品中碳酸钙的质量分数是多少?
(3)恰好完全反应时所得溶液含溶质的质量分数?

(1)该样品与稀盐酸反应产生二氧化碳的质量为 g。
(2)该石灰石样品中碳酸钙的质量分数是多少?
(3)恰好完全反应时所得溶液含溶质的质量分数?
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】金属是一种重要的材料,人类在6000年前就会炼铜,在约2500年前就会炼铁,在约200年前会炼铝。根据你的化学知识回答
(1)你认为金属大规模开发、利用的先后顺序跟下列那些因素有关_______
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性 ④金属冶炼的难易程度
(2)钢铁生产和使用是人类文明和社会进步的重要标志,铁生锈也给人类带来巨大的损失,铁锈的主要成分是_____ ,把表面生锈的铁片浸入足量的稀硫酸中,首先观察到_____ 。过一会看到的现象是:_____ ,有关反应的化学方程式为:_______ 。
(3)黄铜是铜锌合金,外观很想黄金,不法分子常用黄铜冒充黄金行骗,请你说出一种鉴别二者的方法:______ 。
(4)为测定黄铜中铜的质量分数,取10g黄铜放入50g稀硫酸中恰好完全反应,生成氢气0.1g,试计算:黄铜中铜的质量分数。
(1)你认为金属大规模开发、利用的先后顺序跟下列那些因素有关
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性 ④金属冶炼的难易程度
(2)钢铁生产和使用是人类文明和社会进步的重要标志,铁生锈也给人类带来巨大的损失,铁锈的主要成分是
(3)黄铜是铜锌合金,外观很想黄金,不法分子常用黄铜冒充黄金行骗,请你说出一种鉴别二者的方法:
(4)为测定黄铜中铜的质量分数,取10g黄铜放入50g稀硫酸中恰好完全反应,生成氢气0.1g,试计算:黄铜中铜的质量分数。
您最近一年使用:0次
【推荐3】哈尔滨第156中学爱化学活动小组,用黄铜进行如下实验,实验过程及数据记录下:

(1)实验中发生反应的化学方程式为________ 。
(2)据已知条件列出求解A→B参加反应的稀硫酸溶质质量(x)的比例式为__________ ;
(3)该黄铜中铜和锌的质量比为_______ ;(最简整数比)
(4)用98%的浓硫酸配制实验中所用的稀硫酸,需要蒸馏水的体积为__________ mL;稀释操作过程中所用到的仪器有:烧杯、量筒、__________ 。
(5)E烧杯所得溶液中溶质的质量分数为_________ 。

(1)实验中发生反应的化学方程式为
(2)据已知条件列出求解A→B参加反应的稀硫酸溶质质量(x)的比例式为
(3)该黄铜中铜和锌的质量比为
(4)用98%的浓硫酸配制实验中所用的稀硫酸,需要蒸馏水的体积为
(5)E烧杯所得溶液中溶质的质量分数为
您最近一年使用:0次



