根据粗盐中难溶性杂质的去除和溶液的配制实验图示回答相关问题:
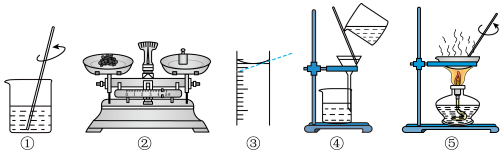
(1)操作④中玻璃棒的作用是________ 。
(2)若按照②③①步骤配制 50g16%的 NaCl 溶液,所配制溶液的溶质质量分数__________ (填“偏大”、“偏小”或“无影响”)。
(3)操作⑤中停止加热的时间是__________ 。
(4)除去粗盐中难溶性的杂质并计算精盐的产率,其正确操作步骤为__________ (填序 号)。
(5)以下操作中可能会导致精盐产率(产率=精盐质量/粗盐质量×100%)偏小的有__________ (填序号)。
a.操作①中有少量溶液溅出烧杯 b.操作③中仰视读数
c.操作④中液面高于滤纸边缘 d.操作⑤中没有使用玻璃棒搅拌
海水是宝贵的自然资源,某氯碱厂电解饱和食盐水溶液制取氢氧化钠的工艺流程示意图如下:
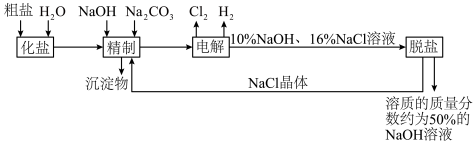
依据图示完成下列填空:
(6)如果粗盐中含 SO 量较高,必须添加钡试剂除去SO
量较高,必须添加钡试剂除去SO ,该钡试剂可以是
,该钡试剂可以是____________ 。
ABa(OH)2 BBa(NO3)2 C BaCl2 D BaSO4
(7)为了有效地除去Ca2+、Mg2+、SO ,加入试剂的合理顺序为
,加入试剂的合理顺序为_________________ 。
a.先加入NaOH,后加入Na2CO3,再加入钡试剂
b.先加入NaOH,后加入钡试剂,再加入Na2CO3
c.先加入钡试剂,后加入NaOH,再加入Na2CO3
d.先加入Na2CO3,后加入钡试剂,再加NaOH
(8)脱盐工序中,通过加热、浓缩、冷却、过滤的方法除去NaCl,该方法利用的是NaOH与NaCl这两物质在______________ 上的性质差异。
(9)检验脱盐是否完全的实验方法是___________ 。

(1)操作④中玻璃棒的作用是
(2)若按照②③①步骤配制 50g16%的 NaCl 溶液,所配制溶液的溶质质量分数
(3)操作⑤中停止加热的时间是
(4)除去粗盐中难溶性的杂质并计算精盐的产率,其正确操作步骤为
(5)以下操作中可能会导致精盐产率(产率=精盐质量/粗盐质量×100%)偏小的有
a.操作①中有少量溶液溅出烧杯 b.操作③中仰视读数
c.操作④中液面高于滤纸边缘 d.操作⑤中没有使用玻璃棒搅拌
海水是宝贵的自然资源,某氯碱厂电解饱和食盐水溶液制取氢氧化钠的工艺流程示意图如下:

依据图示完成下列填空:
(6)如果粗盐中含 SO
 量较高,必须添加钡试剂除去SO
量较高,必须添加钡试剂除去SO ,该钡试剂可以是
,该钡试剂可以是ABa(OH)2 BBa(NO3)2 C BaCl2 D BaSO4
(7)为了有效地除去Ca2+、Mg2+、SO
 ,加入试剂的合理顺序为
,加入试剂的合理顺序为a.先加入NaOH,后加入Na2CO3,再加入钡试剂
b.先加入NaOH,后加入钡试剂,再加入Na2CO3
c.先加入钡试剂,后加入NaOH,再加入Na2CO3
d.先加入Na2CO3,后加入钡试剂,再加NaOH
(8)脱盐工序中,通过加热、浓缩、冷却、过滤的方法除去NaCl,该方法利用的是NaOH与NaCl这两物质在
(9)检验脱盐是否完全的实验方法是
更新时间:2020-04-04 20:26:05
|
相似题推荐
综合应用题
|
较难
(0.4)
解题方法
【推荐1】水是生命之源,也是化学实验中的重要物质(常态下水的密度约为1g/cm3)。
(1)水的净化方法有沉淀、过滤、吸附、蒸馏等,其中净化程度最高的是______ 。活性炭用于净水是利用活性炭的______ 性。
(2)配制100g溶质质量分数为0.9%的氯化钠溶液,需要用到的玻璃仪器有______ 。
(3)20℃,将固体物质X溶于水并进行如下实验,如图所示。回答下列问题。
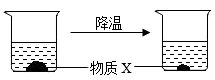
①物质X的溶解度随温度升高而______ (“增大”或“减小”)。
②20℃,物质X溶于不同质量的水中,溶液达到饱和状态时,溶质质量与水的质量关系如图所示。

a.20℃时,该物质的溶解度是______ g。
b.溶液A、B、C、D中溶质质量分数由大到小的关系是______ 。
c.20℃时,将溶液A转化为溶液C的方法有______ 。
(1)水的净化方法有沉淀、过滤、吸附、蒸馏等,其中净化程度最高的是
(2)配制100g溶质质量分数为0.9%的氯化钠溶液,需要用到的玻璃仪器有
(3)20℃,将固体物质X溶于水并进行如下实验,如图所示。回答下列问题。

①物质X的溶解度随温度升高而
②20℃,物质X溶于不同质量的水中,溶液达到饱和状态时,溶质质量与水的质量关系如图所示。

a.20℃时,该物质的溶解度是
b.溶液A、B、C、D中溶质质量分数由大到小的关系是
c.20℃时,将溶液A转化为溶液C的方法有
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】钠及其化合物是中学化学学习和研究的重要内容。

(1)图1是钠的原子结构示意图。下列说法不正确的是_____(填字母序号)。
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为_______ ;小苏打受热分解成碳酸钠、二氧化碳和水,化学方程式为______ 。
(3)配制一瓶如图2所示的溶液需氯化钠_____ g;配制50g6%的氯化钠溶液,若用量筒量取水时俯视读数(其他操作正确),则溶液的质量分数______ 6%(填“>”“<”或“=”)。
(4)已知 ;
;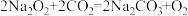 。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象:
。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象:_______ ;如何检验该水溶液中含有氢氧化钠:_______ 。(请简要写出实验的步骤和现象)
(5)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?

(1)图1是钠的原子结构示意图。下列说法不正确的是_____(填字母序号)。
| A.钠属于金属元素 | B.钠原子的质子数为11 |
| C.钠离子的符号为Na+ | D.钠在化学反应中易得到电子 |
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为
(3)配制一瓶如图2所示的溶液需氯化钠
(4)已知
 ;
;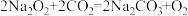 。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象:
。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象:(5)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】在一次实验操作考查时,教师制定了三个考签:① 的制取:②配制50gl0%的
的制取:②配制50gl0%的 溶液:③粗盐提纯。每个同学抽取一个考签进行实验。
溶液:③粗盐提纯。每个同学抽取一个考签进行实验。
I.甲同学抽签后来到实验室,发现本组实验桌上准备了下列仪器和药品:
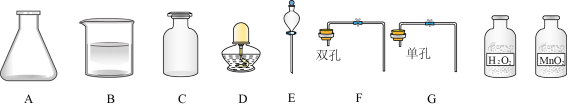
图中仪器A的名称_______ ,仪器C的名称_______ ,仪器E的名称___________ ,甲同学抽到的考签是 的制取,该实验的原理为
的制取,该实验的原理为_______ (用化学方程式表示),二氧化锰的作用___________ ,可选用的发生装置组合有_______ (填字母代号)。若用100g该双氧水溶液制取得到氧气16g,请求出该双氧水的溶质质量分数(列式计算)。_________
Ⅱ.乙同学抽到“配制50g10%的 溶液”。通过计算,需称量
溶液”。通过计算,需称量
______ g,量取水需要选取的合适量筒是_______ (填“ ”或“
”或“ ”或“
”或“ ”)。
”)。
Ⅲ.丙同学抽到的考签为粗盐提纯。
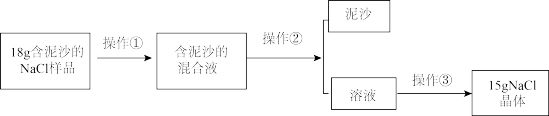
操作②的名称为______ ,该操作过程中玻璃棒的作用______ ,若提纯所得 晶体的质量比实际值偏低,则可能的原因是
晶体的质量比实际值偏低,则可能的原因是______ 。
 的制取:②配制50gl0%的
的制取:②配制50gl0%的 溶液:③粗盐提纯。每个同学抽取一个考签进行实验。
溶液:③粗盐提纯。每个同学抽取一个考签进行实验。I.甲同学抽签后来到实验室,发现本组实验桌上准备了下列仪器和药品:

图中仪器A的名称
 的制取,该实验的原理为
的制取,该实验的原理为Ⅱ.乙同学抽到“配制50g10%的
 溶液”。通过计算,需称量
溶液”。通过计算,需称量
 ”或“
”或“ ”或“
”或“ ”)。
”)。Ⅲ.丙同学抽到的考签为粗盐提纯。

操作②的名称为
 晶体的质量比实际值偏低,则可能的原因是
晶体的质量比实际值偏低,则可能的原因是
您最近一年使用:0次
【推荐1】浩瀚的大海为我们提供了丰富的资源。
(1)要使海水成为饮用水,可以采用的的操作方法是_______(填字母序号)。
(2)牡蛎等海产品中含有微量元素_______ ,缺少它容易能引起食欲不振、发育不良。
(3)探究学习小组以含有Ca2+,Mg2+,Cl﹣的卤水和石灰乳为主要原料在实验室制备无水CaCl2,流程如下图,请回答下列问题:____________ 。
②工业生产中,操作Ⅰ得到的滤渣可以用来_________________ 。
(4)海水晒盐制得的粗盐,可能含有CaCl2、MgCl2、Na2SO4等杂质。兴趣小组的同学将该粗盐配成溶液,并对粗盐溶液进行探究和除杂。
①配制溶液时,加速粗盐溶解的玻璃仪器是______ 。
【探究过程】②步骤1:向粗盐溶液中加入过量NaOH溶液,未出现明显现象,说明溶液中无______ 杂质,向溶液中继续滴加过量Na2CO3溶液,产生白色沉淀CaCO3固体,反应的化学方程式为____________ 。
③步骤2:向步骤1的滤液中滴加过量BaCl2溶液,产生白色沉淀,过滤,向滤液中滴加稀盐酸至溶液呈中性即得NaCl溶液。加稀盐酸除去的物质是_________ 。
【初步结论】杂质成分已确定,且已完全除去。
【反思交流】④小萍认为Na2SO4还不能确定是否存在,可向步骤2的沉淀中滴加过量稀盐酸,若观察到_________ 的现象,证明粗盐中确实存在Na2SO4。
⑤小涛认为杂质也未完全除去,可按照步骤1和步骤2重新实验,并对调其中两种试剂的位置就能达到除杂目的,这两种试剂为______ (填序号)。
A.Na2CO3溶液、BaCl2溶液 B.稀盐酸、BaCl2溶液 C.NaOH溶液、Na2CO3溶液
(1)要使海水成为饮用水,可以采用的的操作方法是_______(填字母序号)。
| A.沉降 | B.用普通滤纸过滤 | C.吸附 | D.蒸馏 |
(2)牡蛎等海产品中含有微量元素
(3)探究学习小组以含有Ca2+,Mg2+,Cl﹣的卤水和石灰乳为主要原料在实验室制备无水CaCl2,流程如下图,请回答下列问题:
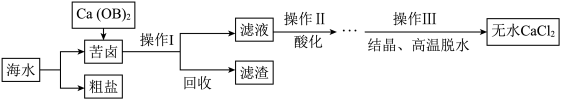
②工业生产中,操作Ⅰ得到的滤渣可以用来
(4)海水晒盐制得的粗盐,可能含有CaCl2、MgCl2、Na2SO4等杂质。兴趣小组的同学将该粗盐配成溶液,并对粗盐溶液进行探究和除杂。
①配制溶液时,加速粗盐溶解的玻璃仪器是
【探究过程】②步骤1:向粗盐溶液中加入过量NaOH溶液,未出现明显现象,说明溶液中无
③步骤2:向步骤1的滤液中滴加过量BaCl2溶液,产生白色沉淀,过滤,向滤液中滴加稀盐酸至溶液呈中性即得NaCl溶液。加稀盐酸除去的物质是
【初步结论】杂质成分已确定,且已完全除去。
【反思交流】④小萍认为Na2SO4还不能确定是否存在,可向步骤2的沉淀中滴加过量稀盐酸,若观察到
⑤小涛认为杂质也未完全除去,可按照步骤1和步骤2重新实验,并对调其中两种试剂的位置就能达到除杂目的,这两种试剂为
A.Na2CO3溶液、BaCl2溶液 B.稀盐酸、BaCl2溶液 C.NaOH溶液、Na2CO3溶液
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐2】学习化学离不开实验。
(1)结合下图回答问题。

①写出仪器甲的名称________ 。
②小明用装置A制备氧气,该反应的化学方程式为________ ,若用E作为收集装置,则验满的方法是_______ 。
③实验室制备二氧化碳的化学反应方程式为_________ ,上图装置B或C都可用作该反应的发生装置,与B相比,C装置的一个明显优点是________ ;若用D装置检验二氧化碳,D装置中使用试液名称为________ ,化学反应方程式为_______ 。
④实验室制备氢气的化学反应方程式为_______ ,若用E作为收集装置,应该从导管_______ 通入。
⑤某同学在50g的稀硫酸溶液加入过量的某金属来实验室制备氢气,经过精确测得到氢气质量为0.1g。计算该硫酸溶液的溶质质量分数________ ?(利用化学方程式计算并写出计算过程)
(2)市售浓盐酸溶质的质量分数为37%,小芳要配制50克溶质的质量分数为5%的稀盐酸。
①实验操作步骤为:计算、_______ 、稀释、转移贴标签。
②上述实验过程中会导致所配溶液的溶质质量分数偏小的是________ 。
A.将浓盐酸倒入烧杯时有少量洒出 B.小芳在量取浓盐酸时仰视读数
C.配制溶液的烧杯事先用少量蒸馏水润洗 D.转移已配好的溶液时,有少量液体溅出
(3)如图是某实验小组进行粗盐(含少量泥沙)中难溶性杂质去除的实验操作示意图,请回答下列问题。

【实验原理】
①除去粗盐中泥沙是利用氯化钠和泥沙的_______ 不同。
【实验步骤】(已知氯化钠在实验条件下溶解度为38g)
②溶解:称量5.0g粗盐,将其加入到20mL蒸馏水中并用玻璃棒不断搅拌,直到粗盐不再减少,玻璃棒的作用是________ ,如果此操作过程中加入水的量过多,对最终的得到的精盐产量影响是________ (偏大、不变和偏小)。
③过滤:过滤时用玻璃棒的作用_______ 。
④蒸发:蒸发结晶过程中,需用玻璃棒不断搅排,当观察到_______ ,停止加热,利用余热将剩余溶液蒸干,此时玻璃棒的作用是_______ 。
(1)结合下图回答问题。

①写出仪器甲的名称
②小明用装置A制备氧气,该反应的化学方程式为
③实验室制备二氧化碳的化学反应方程式为
④实验室制备氢气的化学反应方程式为
⑤某同学在50g的稀硫酸溶液加入过量的某金属来实验室制备氢气,经过精确测得到氢气质量为0.1g。计算该硫酸溶液的溶质质量分数
(2)市售浓盐酸溶质的质量分数为37%,小芳要配制50克溶质的质量分数为5%的稀盐酸。
①实验操作步骤为:计算、
②上述实验过程中会导致所配溶液的溶质质量分数偏小的是
A.将浓盐酸倒入烧杯时有少量洒出 B.小芳在量取浓盐酸时仰视读数
C.配制溶液的烧杯事先用少量蒸馏水润洗 D.转移已配好的溶液时,有少量液体溅出
(3)如图是某实验小组进行粗盐(含少量泥沙)中难溶性杂质去除的实验操作示意图,请回答下列问题。

【实验原理】
①除去粗盐中泥沙是利用氯化钠和泥沙的
【实验步骤】(已知氯化钠在实验条件下溶解度为38g)
②溶解:称量5.0g粗盐,将其加入到20mL蒸馏水中并用玻璃棒不断搅拌,直到粗盐不再减少,玻璃棒的作用是
③过滤:过滤时用玻璃棒的作用
④蒸发:蒸发结晶过程中,需用玻璃棒不断搅排,当观察到
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】酸、碱、盐是中学化学学习的重要内容,它们在生产、生活中具有广泛的用途。
(1)厨房中烘焙糕点常使用发酵粉,发酵粉的主要成分之一是小苏打,其化学式是_____________ 。
(2)实验室有一瓶长期放置的氢氧化钠溶液,某同学推测其发生了变质,请写出其变质的原因:__________________ (用化学方程式表示)。
(3)在用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示。当加入溶液的质量为bg时,所得溶液中的溶质为__________ (写化学式),反应的化学方程式为_____________________ 。_____________ 。
②请设计实验证明B溶液中还含有的两种杂质成分_____________ 。
③通过上述方案,无法得到氯化钠晶体,请将方案补充完整_______________ 。
(5)工业上常在可燃物建筑材料中添加阻燃剂以防止火灾,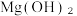 是一种常见的阻燃剂,受热时分解成水蒸气和耐高温的MgO,并吸收大量的热。若生成40kgMgO,需要Mg(OH)₂的质量是多少?
是一种常见的阻燃剂,受热时分解成水蒸气和耐高温的MgO,并吸收大量的热。若生成40kgMgO,需要Mg(OH)₂的质量是多少?
(1)厨房中烘焙糕点常使用发酵粉,发酵粉的主要成分之一是小苏打,其化学式是
(2)实验室有一瓶长期放置的氢氧化钠溶液,某同学推测其发生了变质,请写出其变质的原因:
(3)在用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示。当加入溶液的质量为bg时,所得溶液中的溶质为


②请设计实验证明B溶液中还含有的两种杂质成分
③通过上述方案,无法得到氯化钠晶体,请将方案补充完整
(5)工业上常在可燃物建筑材料中添加阻燃剂以防止火灾,
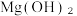 是一种常见的阻燃剂,受热时分解成水蒸气和耐高温的MgO,并吸收大量的热。若生成40kgMgO,需要Mg(OH)₂的质量是多少?
是一种常见的阻燃剂,受热时分解成水蒸气和耐高温的MgO,并吸收大量的热。若生成40kgMgO,需要Mg(OH)₂的质量是多少?
您最近一年使用:0次



