有一种管道疏通剂,主要成分为铝粉和氢氧化钠混合粉末。工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对毛发等淤积物的腐蚀,同时产生氢气增加管道内的气压,利于疏通。小柯利用如图装置测定疏通剂中铝的质量分数。

Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O
______ NaAlO2+3H2↑
(2)根据化学方程式计算样品中铝的质量分数。______
(3)以下情形会导致样品中铝的质量分数测量结果偏高的原因可能有______ 。
A向锥形瓶中倒入样品时,撒出了部分粉末
B在反应过程中有水蒸气逸出
C没有等装置中氢气全部排尽就称量

Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
| 反应前总质量m1 | 反应后总质量m2 |
| 371.84g | 371.24g |
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O

(2)根据化学方程式计算样品中铝的质量分数。
(3)以下情形会导致样品中铝的质量分数测量结果偏高的原因可能有
A向锥形瓶中倒入样品时,撒出了部分粉末
B在反应过程中有水蒸气逸出
C没有等装置中氢气全部排尽就称量
更新时间:2020-04-08 11:01:48
|
【知识点】 化学方程式与实验的计算解读
相似题推荐
实验题
|
适中
(0.65)
解题方法
【推荐1】下图是实验室制取气体常用的发生装置和收集装置。
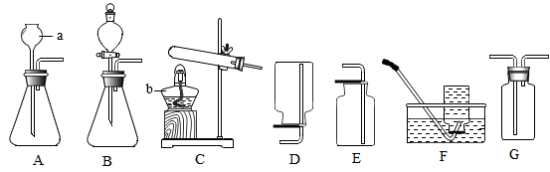
请你回答下列问题:
(1)写出标号仪器的名称:a__________ ,b_________ 。
(2)实验室用过氧化氢溶液制取氧气,若从控制反应速率和节约药品的角度考虑,应选择的发生装置是_________ (填字母编号)。实验室用高锰酸钾制取氧气,反应的化学方程式是________________________ ,反应后的固体剩余物属于_________ (填“混合物”或“纯净物”)。D、E、F、G都是气体的收集装置,其中不能用来收集氧气的是_________ (填字母编号)。
(3)6.32克高锰酸钾加热一段时间后,剩余固体中K、O原子个数比为2:7,则生成氧气的质量为________ 。
(4)某气体X可用D装置收集,若改用G装置收集,则气体X应从_________ (填“左”或“右”)端导管通入。
(5)某校兴趣小组在实验室做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物6.0g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表。
分析表中数据,完成下列问题:
①氯酸钾中钾、氯、氧三种元素的质量比为______ (最简整数比)
②生成氧气的质量为______ g.
③原混合物中二氧化锰的质量分数是多少?(写出计算过程,计算结果精确到0.1%)_____

请你回答下列问题:
(1)写出标号仪器的名称:a
(2)实验室用过氧化氢溶液制取氧气,若从控制反应速率和节约药品的角度考虑,应选择的发生装置是
(3)6.32克高锰酸钾加热一段时间后,剩余固体中K、O原子个数比为2:7,则生成氧气的质量为
(4)某气体X可用D装置收集,若改用G装置收集,则气体X应从
(5)某校兴趣小组在实验室做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物6.0g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表。
| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
| 剩余固体质量/g | 5.1 | 4.5 | 4.2 | 4.08 | 4.08 | 4.08 |
①氯酸钾中钾、氯、氧三种元素的质量比为
②生成氧气的质量为
③原混合物中二氧化锰的质量分数是多少?(写出计算过程,计算结果精确到0.1%)
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】化学兴趣小组的同学在实验室里进行了验证物质性质的实验并配制一种溶液,记录的数据及实验过程如下图所示:

其中第一步和第二步消耗的硫酸量相等。请回答下列问题:
(1)若配制上述实验中所用的稀硫酸,需20g 98%的浓硫酸和____________ 蒸馏水;
(2)请写出加入稀硫酸时发生反应的化学方程式_____________________________ ;
(3)m的数值为_________________________________________________________ ;
(4)列出求解与硫酸铜反应的铁粉质量(x)的比例式___________________________ ;
(5)12g 滤渣中含有__________________________________________ (填化学式);
(6)向滤液B中加入39.4g水后,所得溶液中溶质的质量分数为________________ 。

其中第一步和第二步消耗的硫酸量相等。请回答下列问题:
(1)若配制上述实验中所用的稀硫酸,需20g 98%的浓硫酸和
(2)请写出加入稀硫酸时发生反应的化学方程式
(3)m的数值为
(4)列出求解与硫酸铜反应的铁粉质量(x)的比例式
(5)12g 滤渣中含有
(6)向滤液B中加入39.4g水后,所得溶液中溶质的质量分数为
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】化学实验室常用3%的H2O2溶液来制取氧气,小亮和小君欲用3%的H2O2溶液来制取干燥的氧气,小亮使用的是左下装置图,小君使用的是右下装置图。试回答:
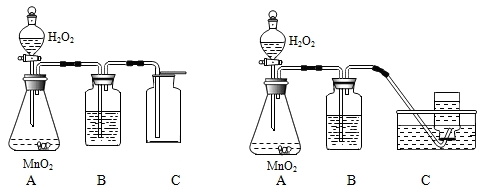
(1)小君同学使用的装置是不合理的,原因是_______ 。
(2)两装置的B仪器中应盛放的物质是________ 。
(3)从严格意义上说,小亮使用的收集装置也不尽合理,理由是_______ 。
(4)3%的H2O2溶液中,氢元素的质量分数为________ ,当H2O2完全分解时,液体中氢元素的质量分数增加_____ %。(保留到小数点后l位)

(1)小君同学使用的装置是不合理的,原因是
(2)两装置的B仪器中应盛放的物质是
(3)从严格意义上说,小亮使用的收集装置也不尽合理,理由是
(4)3%的H2O2溶液中,氢元素的质量分数为
您最近一年使用:0次



