解题方法
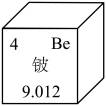
1 . 2023年11月3日,我国已完成最后一批全球最大“人造太阳”项目磁体支撑产品,按时兑现国际承诺。“人造太阳”产生的温度超过1亿摄氏度,其中的重要元素之一是铍,铍在元素周期表中的部分信息如图所示。回答下列问题。_______ 。
(2)画出铍离子的结构示意图:_______ 。
(3)铍原子的质子数为_______ 。
(2)画出铍离子的结构示意图:
(3)铍原子的质子数为
您最近一年使用:0次
名校
解题方法
2 . 下图是几种微粒的结构示意图,下列叙述错误的是
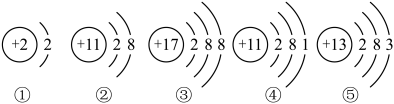
| A.属于同种元素的是②④ |
| B.具有稳定结构的微粒是①②③ |
| C.②是一种阳离子,③是一种阴离子 |
| D.⑤结构示意图中,能量最低的电子层上有3个电子 |
您最近一年使用:0次
解题方法
3 . 新型高导热镁合金常用作电动汽车和消费电子产品的散热器。下图为镁元素在元素周期表中的相关信息和镁原子的结构示意图,下列说法错误的是

| A.镁属于金属元素 |
| B.X的数值为12 |
| C.镁的相对原子质量为24.31g |
| D.镁元素在周期表中位于第三周期 |
您最近一年使用:0次
解题方法
4 . 我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量已成为国际标准。铟元素在元素周期表中的相关信息及铟和铝的原子结构示意图如图所示。下列说法不正确的是

| A.铟原子核内质子数为49 | B.铟元素在元素周期表中位于第五周期 |
| C.金属铟和铝的化学性质相似 | D.铟元素的相对原子质量为114.8g |
您最近一年使用:0次
5 . 建立“宏观—微观—符号”之间的联系是化学学习的重要方法。 ),高纯的单晶硅是重要的半导体材料。从微观角度分析,单晶硅由
),高纯的单晶硅是重要的半导体材料。从微观角度分析,单晶硅由_______ (填“分子”“原子”或“离子”)构成。硅片太阳能电池工作时,将太阳能转化成_______ 能。
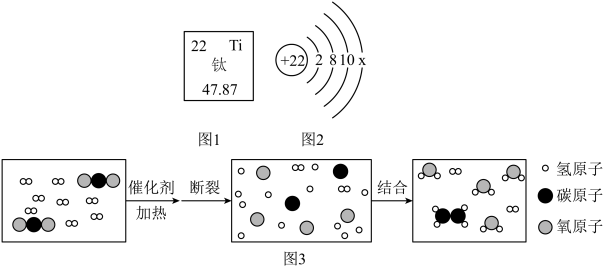
(2)我国长征二号丙运载火箭将遥感三十号08组卫星发射升空。制造运载火箭用到钛合金,下列图1和图2是钛元素( )在元素周期表中的部分信息、钛原子结构示意图。钛元素属于
)在元素周期表中的部分信息、钛原子结构示意图。钛元素属于_______ (填“金属”或“非金属”)元素,图2为钛原子结构示意图,在化学反应中,该原子容易_______ (填“得到”或“失去”)电子。
(3)二氧化碳和氢气在一定条件下转换为化工原料乙烯( ),是我国科学研究的又一重大突破,其反应微观过程如图3所示,请根据要求回答下列问题:
),是我国科学研究的又一重大突破,其反应微观过程如图3所示,请根据要求回答下列问题:
①从微观的角度分析,该反应的实质是_______ 。
②参加反应的二氧化碳和氢气的质量比为_______ 。
 ),高纯的单晶硅是重要的半导体材料。从微观角度分析,单晶硅由
),高纯的单晶硅是重要的半导体材料。从微观角度分析,单晶硅由(2)我国长征二号丙运载火箭将遥感三十号08组卫星发射升空。制造运载火箭用到钛合金,下列图1和图2是钛元素(
 )在元素周期表中的部分信息、钛原子结构示意图。钛元素属于
)在元素周期表中的部分信息、钛原子结构示意图。钛元素属于(3)二氧化碳和氢气在一定条件下转换为化工原料乙烯(
 ),是我国科学研究的又一重大突破,其反应微观过程如图3所示,请根据要求回答下列问题:
),是我国科学研究的又一重大突破,其反应微观过程如图3所示,请根据要求回答下列问题:①从微观的角度分析,该反应的实质是
②参加反应的二氧化碳和氢气的质量比为
您最近一年使用:0次
解题方法
6 . 敦煌壁画是中国古代艺术瑰宝,其中用到了古代矿物颜料石青【主要成分是碱式碳酸铜 ],下列说法正确的是
],下列说法正确的是
 ],下列说法正确的是
],下列说法正确的是A.碳酸根离子的符号为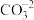 |
| B.碱式碳酸铜中含有四种非金属元素 |
C.氧原子的结构示意图为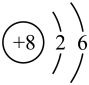 |
D.石青受热分解成氧化铜的化学式为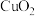 |
您最近一年使用:0次
解题方法
7 . 化学符号是重要的化学语言,下列化学用语表述正确的是
| A.一个镁离子Mg+2 | B.氧化铁Fe2O3 |
C.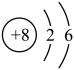 氧离子结构示意图 氧离子结构示意图 | D.两个氮原子N |
您最近一年使用:0次
解题方法
8 . 锶元素有预防动脉硬化的作用。锶元素在元素周期表中的信息及锶原子结构示意图如图所示。下列说法中正确的是
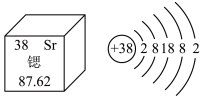
| A.锶元素属于金属元素 | B.锶元素的化学性质稳定 |
| C.锶原子的中子数为38 | D.锶原子的质量是87.62g |
您最近一年使用:0次
名校
解题方法
9 . 氯化钠作为食盐的主要成分,同时在工业、农业等领域也具有十分重要的意义。
(1)下图是钠原子的结构示意图,下列说法正确的是_______ (填字母)。
b.钠属于金属元素
c.钠元素位于第一周期
d.钠离子的符号为Na-
(2)农业上常用质量分数为16%的NaCl溶液选种,实验室欲配制100g该溶质质量分数的NaCl溶液(水的密度近似看做 ),量取水时,应选用量筒的量程为
),量取水时,应选用量筒的量程为_______ (填“25mL”“50mL”或“100mL”);将配制好的溶液装入试剂瓶时,若有少量液体溅出,则会使溶质的质量分数_______ (填“偏大”“偏小”或“不变”)。
(3)工业上饱和氯化钠溶液还可以作为侯氏制碱法的反应物之一,工业上以粗盐为原料制备氯化钠溶液时,首先要除去粗盐中的杂质CaCl2、MgCl2、Na2SO4和泥沙,为达到上述目的,某化学小组设计了如图实验。_______ 。
②写出除去Na2SO4时发生反应的化学方程式_______ 。
③请设计实验验证操作Ⅰ后所得滤液中除氯化钠外还含有的其他溶质成分_______ (简要写出实验步骤、现象和结论,写一种成分即可)。
(1)下图是钠原子的结构示意图,下列说法正确的是
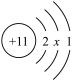
b.钠属于金属元素
c.钠元素位于第一周期
d.钠离子的符号为Na-
(2)农业上常用质量分数为16%的NaCl溶液选种,实验室欲配制100g该溶质质量分数的NaCl溶液(水的密度近似看做
 ),量取水时,应选用量筒的量程为
),量取水时,应选用量筒的量程为(3)工业上饱和氯化钠溶液还可以作为侯氏制碱法的反应物之一,工业上以粗盐为原料制备氯化钠溶液时,首先要除去粗盐中的杂质CaCl2、MgCl2、Na2SO4和泥沙,为达到上述目的,某化学小组设计了如图实验。
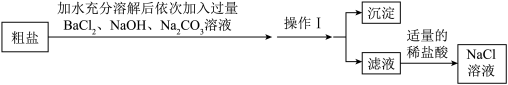
②写出除去Na2SO4时发生反应的化学方程式
③请设计实验验证操作Ⅰ后所得滤液中除氯化钠外还含有的其他溶质成分
您最近一年使用:0次
名校
解题方法
10 . 利用电池作为能量来源,在现代社会生活中的各个方面发挥了很大作用。某型号锂电池组分及含量的百分比如下图所示:________ 性。
(2)锂电池工作时能量转化的方式是________ 。
(3)电池的正极材料是钴酸锂( )。锂元素在元素周期表中的信息以及钴原子的结构示意图如图所示。
)。锂元素在元素周期表中的信息以及钴原子的结构示意图如图所示。________ ,核外电子数为________ 。
②X的值为________ 。
(4)回收锂电池的意义是________ (写一点)。

(2)锂电池工作时能量转化的方式是
(3)电池的正极材料是钴酸锂(
 )。锂元素在元素周期表中的信息以及钴原子的结构示意图如图所示。
)。锂元素在元素周期表中的信息以及钴原子的结构示意图如图所示。
②X的值为
(4)回收锂电池的意义是
您最近一年使用:0次



