1 . 在“碳达峰、碳中和”目标愿景下,氨气(化学式为NH3)作为一种零碳能源具有广泛的应用前景。
(1)氨气易液化、方便储存和运输,是较好的储氢介质。氨气液化的过程属于______ (选填“物理”或“化学”)变化;NH3中氮、氢原子的个数比为______ ;2molNH3中约含______ 个氮原子(用科学计数法表示)。
(2)工业烟气中含有SO2可用氢氧化钠溶液吸收,该反应的化学方程式为______ ;氨法脱硫是一种高效、低能耗的脱硫方式,最终产物(NH4)2SO4在农业上可作为______ (选填“氮”或“复合”)肥。
(3)火力发电设施可以通入氨气。氨气和氧气在一定条件下发生反应,微观示意图如图所示。该反应的化学方程式为______ ;根据上述信息,用氨气作为零碳能源可行性的理由是______ 。
(1)氨气易液化、方便储存和运输,是较好的储氢介质。氨气液化的过程属于
(2)工业烟气中含有SO2可用氢氧化钠溶液吸收,该反应的化学方程式为
(3)火力发电设施可以通入氨气。氨气和氧气在一定条件下发生反应,微观示意图如图所示。该反应的化学方程式为

您最近一年使用:0次
名校
解题方法
2 . 附加题:空气中 含量的控制和
含量的控制和 资源利用具有重要意义。
资源利用具有重要意义。
(1)燃煤烟气中 的捕集可通过如图所示的物质转化实现。
的捕集可通过如图所示的物质转化实现。______ 。
②“吸收”后所得的 溶液与石灰乳反应的生成物有水、
溶液与石灰乳反应的生成物有水、______ 、______ ;载人航天器内,常用LiOH固体而很少用KOH固体吸收空气中的 ,其原因是
,其原因是______ 。
(2)合成尿素 是利用
是利用 的途径之一。尿素
的途径之一。尿素 合成主要通过下列反应实现:
合成主要通过下列反应实现: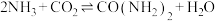 ,反应中,除尿素为液态,其余物质均为气态。已知:平衡常数
,反应中,除尿素为液态,其余物质均为气态。已知:平衡常数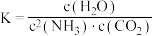 ,其中,c为物质的量浓度,单位为mol/L,K的大小反映了化学反应进行的程度,K值越大,表示反应进行得越完全。
,其中,c为物质的量浓度,单位为mol/L,K的大小反映了化学反应进行的程度,K值越大,表示反应进行得越完全。______ 反应(填“放热”或“吸热”)。
②某温度下,向容积为100L的密闭容器中通入 和
和 ,该反应进行到40s时达到平衡,此时
,该反应进行到40s时达到平衡,此时 的转化率为50%。该温度下此反应平衡常数K的值为
的转化率为50%。该温度下此反应平衡常数K的值为______ (只写数字)。
(3)催化电解吸收 的KOH溶液可将
的KOH溶液可将 还原为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。(电解池中,电源负极与阴极相连。)
还原为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。(电解池中,电源负极与阴极相连。)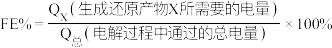 。其中,
。其中, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为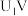 时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为
时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为______ (填化学式)。
②当电解电压为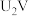 时,阴极由
时,阴极由 生成
生成 时,转移的电子的物质的量为
时,转移的电子的物质的量为______ mol。
③当电解电压为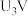 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为______ (只写结果)。
 含量的控制和
含量的控制和 资源利用具有重要意义。
资源利用具有重要意义。(1)燃煤烟气中
 的捕集可通过如图所示的物质转化实现。
的捕集可通过如图所示的物质转化实现。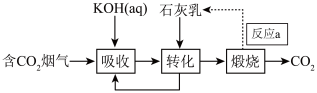
②“吸收”后所得的
 溶液与石灰乳反应的生成物有水、
溶液与石灰乳反应的生成物有水、 ,其原因是
,其原因是(2)合成尿素
 是利用
是利用 的途径之一。尿素
的途径之一。尿素 合成主要通过下列反应实现:
合成主要通过下列反应实现: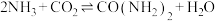 ,反应中,除尿素为液态,其余物质均为气态。已知:平衡常数
,反应中,除尿素为液态,其余物质均为气态。已知:平衡常数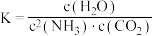 ,其中,c为物质的量浓度,单位为mol/L,K的大小反映了化学反应进行的程度,K值越大,表示反应进行得越完全。
,其中,c为物质的量浓度,单位为mol/L,K的大小反映了化学反应进行的程度,K值越大,表示反应进行得越完全。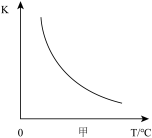
②某温度下,向容积为100L的密闭容器中通入
 和
和 ,该反应进行到40s时达到平衡,此时
,该反应进行到40s时达到平衡,此时 的转化率为50%。该温度下此反应平衡常数K的值为
的转化率为50%。该温度下此反应平衡常数K的值为(3)催化电解吸收
 的KOH溶液可将
的KOH溶液可将 还原为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。(电解池中,电源负极与阴极相连。)
还原为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。(电解池中,电源负极与阴极相连。)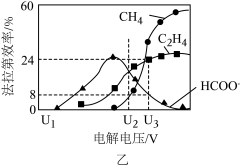
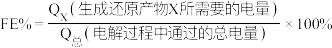 。其中,
。其中, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。①当电解电压为
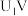 时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为
时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为②当电解电压为
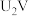 时,阴极由
时,阴极由 生成
生成 时,转移的电子的物质的量为
时,转移的电子的物质的量为③当电解电压为
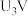 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
2024-06-08更新
|
33次组卷
|
2卷引用:山东省青岛大学附属中学2023-2024学年九年级下学期阶段性检测化学试卷
2024·上海·模拟预测
解题方法
3 . 根据所学化学知识回答下列问题。
(1)实验室用过氧化氢溶液和二氧化锰制取氧气,二氧化锰的作用是_______ ,其中锰元素以_______ (选填“游离”或“化合”)态存在,制取氧气的化学方程式是_______ 。
(2)自来水厂净水过程中除去色素和异味用到活性炭,主要利用其_______ 性。
(3)“中国芯”彰显中国“智”造。芯片的基材主要是高纯硅,工业上利用三氯硅烷( )制取高纯硅。
)制取高纯硅。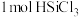 中约含
中约含_______ 个氯原子。
(4)某工业品盐酸的溶质质量分数为37%。“37%”的含义是_______ ;要配制 的稀盐酸,需要37%的盐酸
的稀盐酸,需要37%的盐酸_______ g。
(1)实验室用过氧化氢溶液和二氧化锰制取氧气,二氧化锰的作用是
(2)自来水厂净水过程中除去色素和异味用到活性炭,主要利用其
(3)“中国芯”彰显中国“智”造。芯片的基材主要是高纯硅,工业上利用三氯硅烷(
 )制取高纯硅。
)制取高纯硅。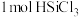 中约含
中约含(4)某工业品盐酸的溶质质量分数为37%。“37%”的含义是
 的稀盐酸,需要37%的盐酸
的稀盐酸,需要37%的盐酸
您最近一年使用:0次
解题方法
4 . 同学们马上升入高中,与初中相比,高中阶段知识容量增大,思维强度增加,但只要认真阅读,认真思考,高中的某些知识其实并不难掌握。
(1)家用罐装液化石油气的主要成分是丙烷(C3H8)、丁烷(C4H10)、丙烯(C3H6)和丁烯(C4H8)等,像这类只含有碳、氢两种元素的有机物称为烃。下列有机物中属于烃类的是_______(填字母)。
(2)化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1摩尔任何物质中含有构成它的微粒个数都是6.02×1023个,1摩尔任何物质的质量是以克为单位,数值上都等于该物质的化学式量(相对分子质量)。例如1摩尔水的各种量关系如下:_________ 个氢原子。
(3)初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-=H2O。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。
离子方程式的书写一般按以下步骤:(以K2SO4与BaCl2反应为例)
①写出K2SO4与BaCl2反应的化学方程式:K2SO4+BaCl2=BaSO4↓+2KCl
②把易溶于水、易离解的物质写成高子形式,把难溶的物质、气体和水等仍用化学式表示上述方程式可改写成:2K++ +Ba2++2Cl-=BaSO4↓+2K++2Cl-
+Ba2++2Cl-=BaSO4↓+2K++2Cl-
③删去方程式两边不参加反应的离子:Ba2++ =BaSO4↓
=BaSO4↓
④检查方程式两边各元素的原子个数和电荷总数是否相等
请写出:向硫酸铜溶液中滴加氢氧化钠溶液所发生反应的离子方程式:___________ 。
(1)家用罐装液化石油气的主要成分是丙烷(C3H8)、丁烷(C4H10)、丙烯(C3H6)和丁烯(C4H8)等,像这类只含有碳、氢两种元素的有机物称为烃。下列有机物中属于烃类的是_______(填字母)。
| A.甲烷CH4 | B.乙醇C2H5OH | C.乙炔C2H2 | D.正戊烯C5H10 |
(2)化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1摩尔任何物质中含有构成它的微粒个数都是6.02×1023个,1摩尔任何物质的质量是以克为单位,数值上都等于该物质的化学式量(相对分子质量)。例如1摩尔水的各种量关系如下:

(3)初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-=H2O。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。
离子方程式的书写一般按以下步骤:(以K2SO4与BaCl2反应为例)
①写出K2SO4与BaCl2反应的化学方程式:K2SO4+BaCl2=BaSO4↓+2KCl
②把易溶于水、易离解的物质写成高子形式,把难溶的物质、气体和水等仍用化学式表示上述方程式可改写成:2K++
 +Ba2++2Cl-=BaSO4↓+2K++2Cl-
+Ba2++2Cl-=BaSO4↓+2K++2Cl-③删去方程式两边不参加反应的离子:Ba2++
 =BaSO4↓
=BaSO4↓④检查方程式两边各元素的原子个数和电荷总数是否相等
请写出:向硫酸铜溶液中滴加氢氧化钠溶液所发生反应的离子方程式:
您最近一年使用:0次
名校
解题方法
5 . 某固体样品中含有的离子由Na+、Ca2+、Ba+、 、
、 、
、 、
、 中的若干种组成,取适量该固体进行如下实验:
中的若干种组成,取适量该固体进行如下实验:
【查阅资料】
标准状况下1mol气体的体积为22.4L。
回答下列问题:
(1)固体E中所含物质的化学式为____________ 。
(2)可用____________ 检验气体C,现象是____________ 。
(3)1.97gBaCO3在空气中高温充分灼烧得到1.69g固体,经检验没有产生有毒气体,写出高温灼烧时发生反应的化学方程式:_____________ 。
(4)100mL无色溶液A中c( )=
)=____________ mol/L,固体样品中n( )=
)=____________ mol。
(5)当m>___________ g时,100mL无色溶液A中会含有 ,此时c(
,此时c( )=
)=____________ mol/L(用含m的代数式表示)。
 、
、 、
、 、
、 中的若干种组成,取适量该固体进行如下实验:
中的若干种组成,取适量该固体进行如下实验: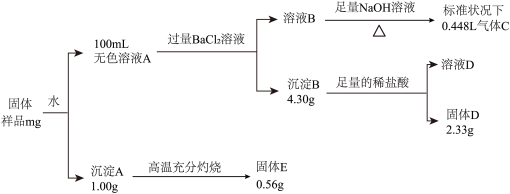
【查阅资料】
标准状况下1mol气体的体积为22.4L。
回答下列问题:
(1)固体E中所含物质的化学式为
(2)可用
(3)1.97gBaCO3在空气中高温充分灼烧得到1.69g固体,经检验没有产生有毒气体,写出高温灼烧时发生反应的化学方程式:
(4)100mL无色溶液A中c(
 )=
)= )=
)=(5)当m>
 ,此时c(
,此时c( )=
)=
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题
(1)在标准状况下,4.48L的NH3质量为_______ ,若将其溶于水配成500mL的溶液,其物质的量浓度为_______ 。
(2)同温同压下,二氧化硫气体(SO2)和三氧化硫气体(SO3)的体积比是3:2,则它们的物质的量之比是_______ ,密度之比是_______ 。
(3)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则该气体所含原子总数为______ 个,在标准状况下该气体的体积为_______ L。
(1)在标准状况下,4.48L的NH3质量为
(2)同温同压下,二氧化硫气体(SO2)和三氧化硫气体(SO3)的体积比是3:2,则它们的物质的量之比是
(3)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则该气体所含原子总数为
您最近一年使用:0次
名校
解题方法
7 . 中国药学家屠呦呦因发现青蒿素,开创了治疗疟疾的新方法,荣获了诺贝尔奖。已知青蒿素的分子式为C15H22O5。下列有关说法正确的是
| A.青蒿素的摩尔质量为282g•mol-1 |
| B.青蒿素中C、H、O的质量之比为15:22:5 |
| C.1mol青蒿素的体积约为22.4L |
| D.1mol青蒿素中含11molH2 |
您最近一年使用:0次
名校
解题方法
8 . 如图是向MgCl2、AlCl3混合液中依次加入M和N时生成沉淀的物质的量与加入的M和N的体积关系图(M、N各表示盐酸或氢氧化钠溶液中的一种),以下结论不正确的是

| A.混合溶液中c(AlCl3):c(MgCl2)=1:1 |
| B.混合溶液中c(AlCl3):c(MgCl2)=3:1 |
| C.V之前加NaOH溶液,V之后加盐酸 |
| D.这种盐酸与NaOH溶液中溶质的物质的量浓度相同 |
您最近一年使用:0次
解题方法
9 . 化学是研究物质的组成、结构、性质、转化及应用的一门基础学科。从化学视角认识“碳及其化合物”,回答下列问题。___________ 元素组成。
(2)结构角度:CO和CO2分子构成不同,1molCO中约含___________ 个氧原子。
(3)性质角度:CO具有可燃性,可以作燃料,CO2不可燃也不助燃,可以用于___________ 。
(4)转化角度:“价类二维图”反映的是元素化合价和物质类别之间的关系,构建“价类二维图”是学习物质转化的重要方法。图1是碳及其化合物的“价类二维图”。图中物质属于有机物的是____ 。X点对应的单质有多种,它们互称为________ ,CO转化为Y的化学方程式为________ (写一个即可)。利用某新型催化剂可将CO2和H2转化为甲烷(CH4)和Z,该反应的微观示意图如下图所示。Z的化学式为:________ 。

(2)结构角度:CO和CO2分子构成不同,1molCO中约含
(3)性质角度:CO具有可燃性,可以作燃料,CO2不可燃也不助燃,可以用于
(4)转化角度:“价类二维图”反映的是元素化合价和物质类别之间的关系,构建“价类二维图”是学习物质转化的重要方法。图1是碳及其化合物的“价类二维图”。图中物质属于有机物的是
您最近一年使用:0次
解题方法
10 . 有关叙述正确的是
| A.水中含氢分子 | B.二氧化碳中含有2个氧原子 |
C.1mol物质约含( 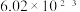 个分子) 个分子) | D.1molH2和1molO2所含原子个数相等 |
您最近一年使用:0次



