1 . 我国青海盐湖湖水中富含氯化钾。下列有关氯化钾溶液的叙述不正确的是( )
| A.氯化钾溶液能导电是因为溶液中含有较多自由移动的离子 |
| B.从质量分数为10%的氯化钾溶液中取出10mL,则剩余溶液的质量分数仍为10% |
| C.一定温度下的KCl饱和溶液中不能再溶解任何其他溶质 |
| D.配制氯化钾溶液时,用玻璃棒搅拌可加快溶解速率 |
您最近一年使用:0次
2 . 新疆引渤海水西调工程项目中亟待解决海水淡化问题,采用膜分离的新技术可将含盐浓度高达5.5%的海水进行淡化。如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水,对加压后右侧海水成分变化进行分析,正确的是( )


| A.溶质质量增加 |
| B.溶液质量不变 |
| C.溶剂质量减少 |
| D.溶质质量分数不变 |
您最近一年使用:0次
名校
3 . 下列说法中正确的是( )
| A.溶液一定是均一、无色、稳定的 | B.一种溶剂只能溶解一种溶质 |
| C.饱和溶液的溶质质量分数一定大于不饱和溶液 | D.海水晒盐属于蒸发结晶 |
您最近一年使用:0次
2020-04-13更新
|
201次组卷
|
3卷引用:2020年广东省深圳市南山区育才二中中考一模化学试题
2020年广东省深圳市南山区育才二中中考一模化学试题山东省临沂市费县第二中学2019-2020学年九年级下学期5月月考化学试题(已下线)6.3 物质的溶解性-2020-2021学年九年级化学下册课时同步练(沪教版)
4 . 研究物质的溶解对于生产、生活有着重要意义。A、B 两种物质的溶解度曲线如图 1 所示;20℃时,将 A、B 两种固体各 50g,分别加入到盛有 100g 水的烧杯中,充分搅拌后现象如图 2 所示;升温到 50℃时,A、B 两种固体在水中的溶解情况如图 3 所示。请回答下列问题
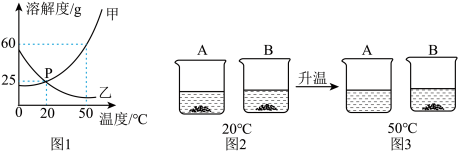
(1)图 1 中 P 点的含义____________ 。
(2)图 1 中能表示 A 物质溶解度随温度变化的曲线是____________ (填甲或乙)。
(3)从 20℃到 50℃的变化过程中,一直处于饱和状态的是____________ (填 A 或 B)溶液。
(4)50℃时向盛有 40g 物质甲固体的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为___________ 。

(1)图 1 中 P 点的含义
(2)图 1 中能表示 A 物质溶解度随温度变化的曲线是
(3)从 20℃到 50℃的变化过程中,一直处于饱和状态的是
(4)50℃时向盛有 40g 物质甲固体的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为
您最近一年使用:0次
名校
5 . (1)请根据下列实验和溶解度曲线回答问题(已知水的密度约为1 g/cm3)
①表中w的值为__________ 。
②一定属于不饱和溶液的是______ (填序号)。
③溶质的质量分数一定相等的溶液是B和___ (填序号),此时溶质的质量分数是___ (精确到0.01%)。
(2)许多果农用钼素去促进东魁杨梅优质丰产;金属元素钼(Mo)通常用作合金及不锈钢的添加剂。化工生产中制备金属钼的主要流程如下图:
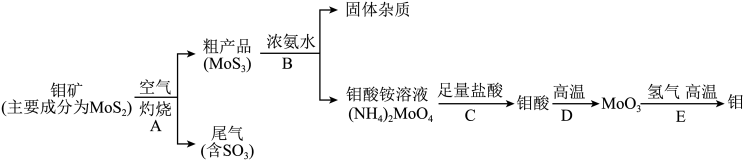
①步骤A中,灼烧钼矿通常会将矿石粉碎成小颗粒,其目的是__________________ 。
②现有:a烧杯b玻璃棒c漏斗d酒精灯等四种仪器,如果在实验室模拟步骤B,则不需要选用的是_____ (填字母序号)。
③写出步骤E的化学方程式______________________________ 。
| 实验操作 | 实验结果 |  |
| 取100 mL水,加入25 g硝酸钾,搅拌恢复至20℃ | 全部溶解,得溶液A | |
| 再加w g硝酸钾,搅拌,恢复到20℃ | 恰好饱和,得溶液B | |
| 再加25 g硝酸钾,搅拌,恢复到20℃ | 得溶液C | |
| 加热 | 全部溶解,得溶液D | |
| 冷却至20℃ | 析出晶体,得溶液E |
②一定属于不饱和溶液的是
③溶质的质量分数一定相等的溶液是B和
(2)许多果农用钼素去促进东魁杨梅优质丰产;金属元素钼(Mo)通常用作合金及不锈钢的添加剂。化工生产中制备金属钼的主要流程如下图:

①步骤A中,灼烧钼矿通常会将矿石粉碎成小颗粒,其目的是
②现有:a烧杯b玻璃棒c漏斗d酒精灯等四种仪器,如果在实验室模拟步骤B,则不需要选用的是
③写出步骤E的化学方程式
您最近一年使用:0次
6 . 下表是KNO3和Ca(OH)2在不同温度时的溶解度。下列说法错误的是( )
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
| Ca(OH)2 | 0.19 | 0.17 | 0.16 | 0.14 | 0.13 | 0.11 | |
| A.硝酸钾的溶解度随温度的升高而增大,氢氧化钙的溶解度随温度的升高而减小 |
| B.硝酸钾中含有少量氢氧化钙时,可以用冷却热饱和溶液的方法提纯硝酸钾 |
| C.氢氧化钙的不饱和溶液转化为饱和溶液可以采取升高温度的方法 |
| D.20℃时,氢氧化钙饱和溶液的溶质质量分数为 0.17% |
您最近一年使用:0次
7 . t1℃时,将 a、b 两种固体物质(均不含结晶水)各 25g,分别加入盛有 l00g 水的烧杯中,充分搅拌后现象如图甲所示;升温到 t2℃时,忽略水分蒸发,现象如图乙所示。图丙是 a、b 两种固体物质在水中的溶解度曲线。下列说法正确的是
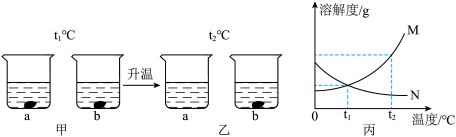

| A.图甲中两烧杯内 a、b 溶液的溶质质量分数不一定相等 |
| B.图乙中烧杯内 a 溶液的溶质质量分数为 20% |
| C.图丙中曲线 M 表示 a 物质的溶解度曲线 |
| D.若 a 中混有少量 b,可将其溶液蒸发结晶、趁热过滤以提纯 a |
您最近一年使用:0次
2020-04-10更新
|
102次组卷
|
2卷引用:江苏省镇江市2019-2020学年九年级下学期3月线上测试化学试题B
8 . 分析推理是化学学习中常用的思维方法,下列推理正确的是( )
| A.化学变化中一定有新物质生成,所以有新物质生成的变化一定是化学变化 |
| B.分子、原子都是不显电性的粒子,不显电性的粒子一定是分子或原子 |
| C.中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应 |
| D.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 |
您最近一年使用:0次
9 . 硝酸钾和氯化钾的溶解度曲线如图所示
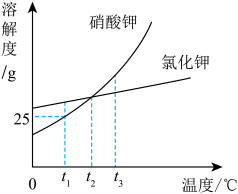
(1)t1℃时,硝酸钾的溶解度为______ g。
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为______ 。
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是______ 。
(4)在t3℃时将等质量的硝酸钾和氯化钾的饱和溶液降温至t2℃,析出晶体多的是______ 。

(1)t1℃时,硝酸钾的溶解度为
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是
(4)在t3℃时将等质量的硝酸钾和氯化钾的饱和溶液降温至t2℃,析出晶体多的是
您最近一年使用:0次
名校
10 . 如图是氯化钠、氯化铵和碳酸氢钠三种物质的溶解度曲线。分析曲线得到以下说法中,错误的是
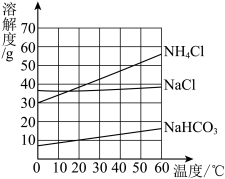

| A.氯化钠和碳酸氢钠溶解度都随温度升高而增大 |
| B.利用冷却结晶法从氯化钠、氯化铵混合物中分离出氯化铵 |
| C.在40℃ 时,氯化钠和氯化铵固体各20g溶于50g水,所得溶液都是饱和溶液 |
| D.在20℃ 时,三种物质饱和溶液的溶质质量分数为NH4Cl>NaCl>NaHCO3 |
您最近一年使用:0次



