1 . 下列物质敞口放置在空气中较长时间后,质量会增加且没有生成新物质的是
| A.浓硫酸 | B.浓盐酸 | C.烧碱 | D.生石灰 |
您最近一年使用:0次
解题方法
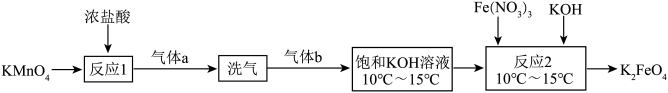
2 . 高铁酸钾(K2FeO4)是一种新型的多功能水处理剂,同时具备消毒和净水的功能。实验室合成高铁酸钾(K2FeO4),的流程如图所示。
信息2 在氧化还原反应中,除了从得失氧的角度分析外,还可从化合价的变化来判断氧化剂和还原剂,如CO+CuO Cu+CO2,该反应中Cu的化合价降低,CuO作氧化剂,C的化合价升高,CO作还原剂。
Cu+CO2,该反应中Cu的化合价降低,CuO作氧化剂,C的化合价升高,CO作还原剂。
(1)高锰酸钾是一种___________ 色的固体。
(2)操作“洗气”的目的是为了除去气体a中的__________ 得到较纯净气体b(Cl2)。
(3)K2FeO4中Fe的化合价为___________ 。
(4)反应2的化学方程式为:2Fe(NO3)3+10KOH+3KClO=2K2FeO4+3___ +6KNO3+5H2O
(5)K2FeO4在进行水处理后得到Fe(OH)3,请从化合价变化的角度分析,K2FeO4在该过程中作_______ 剂。
信息2 在氧化还原反应中,除了从得失氧的角度分析外,还可从化合价的变化来判断氧化剂和还原剂,如CO+CuO
 Cu+CO2,该反应中Cu的化合价降低,CuO作氧化剂,C的化合价升高,CO作还原剂。
Cu+CO2,该反应中Cu的化合价降低,CuO作氧化剂,C的化合价升高,CO作还原剂。(1)高锰酸钾是一种
(2)操作“洗气”的目的是为了除去气体a中的
(3)K2FeO4中Fe的化合价为
(4)反应2的化学方程式为:2Fe(NO3)3+10KOH+3KClO=2K2FeO4+3
(5)K2FeO4在进行水处理后得到Fe(OH)3,请从化合价变化的角度分析,K2FeO4在该过程中作
您最近一年使用:0次
名校
解题方法
3 . 由下列实验操作及现象所得到的结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 将存放已久的少量氢氧化钠固体配成溶液,滴加几滴稀盐酸,无气泡产生 | 氢氧化钠固体没变质 |
| B | 打开浓盐酸的瓶盖,看到瓶口有白雾冒出 | 浓盐酸有挥发性 |
| C | 在盛有2mL水的试管中滴入2~3滴红墨水,振荡,再加入2mL,乙醇,再振荡,溶液不分层 | 乙醇能溶解在水中 |
| D | 从布料的毛边抽一根丝,用火点燃,无气味 | 布料是羊毛织物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 实验室中的成员正在举办交流会,下列“发言”中不涉及化学变化的是
| A.浓盐酸:我挥发了 | B.酒精灯:我燃烧了 |
| C.铁架台:我生锈了 | D.熟石灰:我变质了 |
您最近一年使用:0次
解题方法
5 . 下列实验现象描述正确的是
| A.打开浓硫酸的瓶塞,在瓶口出现白雾 |
| B.在空气中点燃木炭,木炭燃烧,发红光,生成二氧化碳气体 |
| C.电解水实验:电极附近产生气泡,一段时间后,正、负极产生的气体质量比约为1:2 |
| D.将氧化铜粉末放入稀盐酸中,溶液由无色变为蓝色 |
您最近一年使用:0次
2024-05-13更新
|
50次组卷
|
2卷引用:2024年黑龙江省龙东地区部分学校中考二模化学试卷
解题方法
6 . 化学实验现象多种多样,以下是莉莉同学对现象的整理,不正确的是
| A.镁带在空气中燃烧,发出耀眼白光,生成白色固体 |
| B.打开装有浓盐酸的试剂瓶,产生大量白烟 |
| C.铜片在空气中加热,固体由红色变黑色 |
| D.将浓硫酸滴在白纸上,纸张变黑 |
您最近一年使用:0次
名校
解题方法
7 . 对比是学习化学的重要方法,下列关于盐酸和硫酸的比较中错误的是
| A.只要把试剂瓶的瓶塞打开,放在空气中观察,就可以鉴别浓盐酸和浓硫酸 |
| B.浓盐酸、浓硫酸敞口放置一段时间后,它们的溶质质量分数均会变小 |
| C.稀盐酸、稀硫酸中都含有氢离子 |
| D.实验室制取二氧化碳,用块状石灰石和稀盐酸或稀硫酸均可 |
您最近一年使用:0次
8 . 下列说法中错误的是
| A.在树木上涂刷含有硫磺粉等的石灰浆,可防止冻伤树木,并防止害虫生卵 |
| B.打开盛有浓硫酸的试剂瓶塞,瓶口出现白雾 |
| C.服用含氢氧化铝的药物可以治疗胃酸过多症 |
| D.磷肥可以促进作物生长,还可增强作物的抗寒、抗旱能力 |
您最近一年使用:0次
解题方法
9 . 下列关于盐酸的描述,错误的是
| A.盐酸具有强烈的吸水性 | B.浓盐酸有刺激性气味 |
| C.盐酸是氯化氢气体的水溶液 | D.打开装有浓盐酸的试剂瓶,瓶口处有白烟 |
您最近一年使用:0次
解题方法
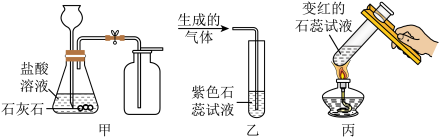
10 . 兴趣小组同学采用不同体积比的浓盐酸与水稀释而成的盐酸溶液进行“CO2的制取与性质”实验。实验如图所示,现象如下表所示。
(1)甲中CO2可采用向上排空气法收集的原因是______ 。
(2)乙中紫色石蕊试液均变红的原因可用化学方程式表示为______ 。
(3)丙中石蕊试液在①实验中,加热后不变紫的原因是______ 。
(4)比较表中数据可知:盐酸浓度越大,产生CO2的速率越______ (选填“快”或“慢”)。
(5)根据上述探究,配制实验室制取CO2的稀盐酸时,100mL浓盐酸中加水的体积较适宜的范围是______ mL。
(6)实验室现需收集4瓶(每瓶以125mL计算)CO2气体,至少需要多少克石灰石(含碳酸钙75%)与足量的稀盐酸反应才能制得______ ?(实验条件下CO2的密度为2g/L,写出计算过程,计算结果精确到0.01g)
| 序号 | 浓盐酸与水的体积比 | 集满一瓶的时间 | 乙溶液的是变化 | 丙溶液的是变化 |
| ① | 1:0 | 20秒 | 变红 | 不变色 |
| ② | 1:1 | 26秒 | 变红 | 变紫 |
| ③ | 1:2 | 1分6秒 | 变红 | 变紫 |
| ④ | 1:3 | 1分48秒 | 变红 | 变紫 |
| ⑤ | 1:4 | 2分32秒 | 变红 | 变紫 |
(1)甲中CO2可采用向上排空气法收集的原因是
(2)乙中紫色石蕊试液均变红的原因可用化学方程式表示为
(3)丙中石蕊试液在①实验中,加热后不变紫的原因是
(4)比较表中数据可知:盐酸浓度越大,产生CO2的速率越
(5)根据上述探究,配制实验室制取CO2的稀盐酸时,100mL浓盐酸中加水的体积较适宜的范围是
(6)实验室现需收集4瓶(每瓶以125mL计算)CO2气体,至少需要多少克石灰石(含碳酸钙75%)与足量的稀盐酸反应才能制得
您最近一年使用:0次



