第32届(2018年)化学奥林匹克竞赛北京地区预赛试题
北京
高二
竞赛
2021-07-23
431次
整体难度:
较难
考查范围:
化学反应原理、物质结构与性质、竞赛、认识化学科学、常见无机物及其应用、化学实验基础、有机化学基础
第32届(2018年)化学奥林匹克竞赛北京地区预赛试题
北京
高二
竞赛
2021-07-23
431次
整体难度:
较难
考查范围:
化学反应原理、物质结构与性质、竞赛、认识化学科学、常见无机物及其应用、化学实验基础、有机化学基础
一、解答题 添加题型下试题
解答题-原理综合题
|
较难(0.4)
1. (1)下列玻璃仪器的洗涤方法不涉及氧化还原反应的是_____
A.附有银镜的试管用稀硝酸清洗
B.附有油脂的烧杯用热纯碱溶液清洗
C.附有MnO2的烧瓶用热的浓盐酸清洗
D.附有硫的燃烧匙用热的烧碱溶液清洗
(2)室温下,某兴趣小组用下图装置在通风橱中进行如下实验:
下列说法正确的是_____
A.试管I中浅棕色气体为NO2,由硝酸还原生成
B.等量的Cu完全溶解时,I中消耗的HNO3更多
C.换成Fe之后重复实验,依然是试管II中反应更剧烈
D.试管II中反应后溶液颜色与试管I中的不同,是由于溶有NO2
(3)溶液的导电性与溶液中的离子的种类和浓度有关,下列各组实验过程的被滴加溶液导电性变化与如图对应的是_____
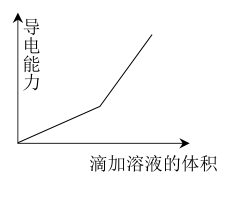
A.向Ba(OH)2溶液中滴加H2SO4溶液
B.向醋酸溶液中滴加NaOH溶液
C.向糖水中滴加NaCl溶液。
D.向盐酸中滴加氨水
(4)卤化钠(NaX)和四卤化钛(TiX4) 的熔点如图所示。下列判断不正确的是_____
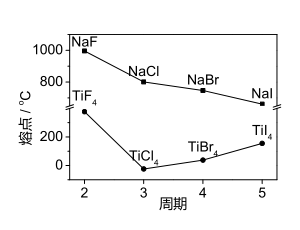
A. TiF4 的熔点反常升高是由于氢键的作用
B. NaX随X-半径增大,离子键减弱。
C. NaX均为离子化合物
D. TiCl4 为共价化合物
(5)如图所示,钠-氯化镍电池是以β-Al2O3(Al2O3· xNa2O)作为固体电解质构成的一种新型高能电池(2Na + NiCl2 Ni+2NaCl),下列关于该电池的叙述错误的是
Ni+2NaCl),下列关于该电池的叙述错误的是_____
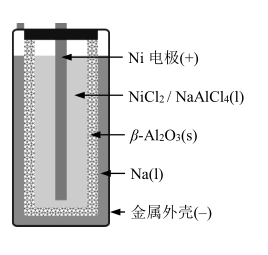
A.放电时NaCl在熔融电解质中生成
B.充电时阴极反应: Na++e-= Na 。
C.氯离子通过β-Al2O3 (s)在两电极间移动
D.如果电池过度放电,AlCl 可能被还原
可能被还原
(6)最近我国科学家预测并据此合成了新型碳材料: T-碳。可以看做金刚石结构中的一个碳原子被四个碳原子构成一个正四面体结构单元替代(如下图所示,所有小球都代表碳原子)。下列说法正确的是_____

A.T-碳与石墨、金刚石互为同素异形体
B.T-碳晶体与金刚石晶体类似,属于原子晶体。
C.T-碳晶体和金刚石晶体中含有的化学键不同
D.T-碳与金刚石中的碳原子都采取杂化方式不同
A.附有银镜的试管用稀硝酸清洗
B.附有油脂的烧杯用热纯碱溶液清洗
C.附有MnO2的烧瓶用热的浓盐酸清洗
D.附有硫的燃烧匙用热的烧碱溶液清洗
(2)室温下,某兴趣小组用下图装置在通风橱中进行如下实验:
| 实验 | 现象 |
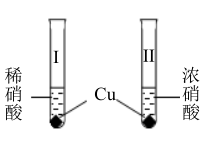 | 试管I中开始无明显现象,逐渐有微小气泡生成,越来越剧烈,液面上方出现浅棕色气体,溶液呈蓝色。 |
| 试管II中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色;之后向绿色溶液中持续通入N2,溶液变为蓝色。 |
下列说法正确的是
A.试管I中浅棕色气体为NO2,由硝酸还原生成
B.等量的Cu完全溶解时,I中消耗的HNO3更多
C.换成Fe之后重复实验,依然是试管II中反应更剧烈
D.试管II中反应后溶液颜色与试管I中的不同,是由于溶有NO2
(3)溶液的导电性与溶液中的离子的种类和浓度有关,下列各组实验过程的被滴加溶液导电性变化与如图对应的是

A.向Ba(OH)2溶液中滴加H2SO4溶液
B.向醋酸溶液中滴加NaOH溶液
C.向糖水中滴加NaCl溶液。
D.向盐酸中滴加氨水
(4)卤化钠(NaX)和四卤化钛(TiX4) 的熔点如图所示。下列判断不正确的是

A. TiF4 的熔点反常升高是由于氢键的作用
B. NaX随X-半径增大,离子键减弱。
C. NaX均为离子化合物
D. TiCl4 为共价化合物
(5)如图所示,钠-氯化镍电池是以β-Al2O3(Al2O3· xNa2O)作为固体电解质构成的一种新型高能电池(2Na + NiCl2
 Ni+2NaCl),下列关于该电池的叙述错误的是
Ni+2NaCl),下列关于该电池的叙述错误的是
A.放电时NaCl在熔融电解质中生成
B.充电时阴极反应: Na++e-= Na 。
C.氯离子通过β-Al2O3 (s)在两电极间移动
D.如果电池过度放电,AlCl
 可能被还原
可能被还原(6)最近我国科学家预测并据此合成了新型碳材料: T-碳。可以看做金刚石结构中的一个碳原子被四个碳原子构成一个正四面体结构单元替代(如下图所示,所有小球都代表碳原子)。下列说法正确的是

A.T-碳与石墨、金刚石互为同素异形体
B.T-碳晶体与金刚石晶体类似,属于原子晶体。
C.T-碳晶体和金刚石晶体中含有的化学键不同
D.T-碳与金刚石中的碳原子都采取杂化方式不同
【知识点】 原电池原理的综合应用解读 根据晶胞结构确定晶体化学式解读 晶体 电化学
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
困难(0.15)
2.
(1)质谱中同位素带来的特征峰可用来鉴定某些元素。某氯代烃或溴代烃的质谱中分子离子峰如图所示。

氯和溴的天然同位素丰度比分别为35Cl:37C1≈3: 1;79Br:8lBr≈1 : 1,该有机物是___________ 代烃;其分子式是___________ 。
(2)如下图是水的相图,每一条线表示两相共存,比如,OC表示冰-水共存。

I.冰-气共存线是___________ ;
II.夏天将衣服晾干,请在图中用虚线画出水的状态变化(g 点是湿衣服中水的起始状态,此时空气中水的蒸气压为fPa)___________ 。
(3)已知:配合物CuSO4·5H2O的结构式为Cu(H2O)4SO4·H2O。某同学测定下列在水中的摩尔电导率如下表所示,试从结构角度说明下列各配合物摩尔导电率变化的原因___________ 。
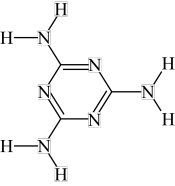
(4)多重氢键在生命体、分子自组装和响应型功能材料领域都有重要应用。三聚氰酸和三聚氰胺(1:1) 可以通过多重氢键自组装构成二维片状结构,被形象地称为“分子饼”。请用虚线在下图中直接画出两个分子间存在的氢键___________ ,并画出二维片状结构中的一个环的结构___________ (分别以× 和 表示三聚氰酸和三聚氰胺分子)。
表示三聚氰酸和三聚氰胺分子)。

(5)查文献知: 25 ℃时,PbCrO4在不同条件下的溶解度如下:
分别说明PbCrO4在三种溶液中的溶解度都比在水中的大的原因_______ 。
(1)质谱中同位素带来的特征峰可用来鉴定某些元素。某氯代烃或溴代烃的质谱中分子离子峰如图所示。

氯和溴的天然同位素丰度比分别为35Cl:37C1≈3: 1;79Br:8lBr≈1 : 1,该有机物是
(2)如下图是水的相图,每一条线表示两相共存,比如,OC表示冰-水共存。

I.冰-气共存线是
II.夏天将衣服晾干,请在图中用虚线画出水的状态变化(g 点是湿衣服中水的起始状态,此时空气中水的蒸气压为fPa)
(3)已知:配合物CuSO4·5H2O的结构式为Cu(H2O)4SO4·H2O。某同学测定下列在水中的摩尔电导率如下表所示,试从结构角度说明下列各配合物摩尔导电率变化的原因
| 配合物 | 摩尔电导率/ S·m2·mol-l |
| PtCl4·6NH3 | 523 |
| PtCl4·5NH3 | 404 |
| PtCl4·4NH3 | 229 |
| PtCl4·3NH3 | 97 |
| PtCl4·2NH3 | 0 |
(4)多重氢键在生命体、分子自组装和响应型功能材料领域都有重要应用。三聚氰酸和三聚氰胺(1:1) 可以通过多重氢键自组装构成二维片状结构,被形象地称为“分子饼”。请用虚线在下图中直接画出两个分子间存在的氢键
 表示三聚氰酸和三聚氰胺分子)。
表示三聚氰酸和三聚氰胺分子)。

(5)查文献知: 25 ℃时,PbCrO4在不同条件下的溶解度如下:
| 溶媒 | H2O | 0.1 mol·L-1的CH3COONH4 | 0.1 mol·L-1的HClO4. | 0.9 mol·L-1的KOH |
| 溶解度/ mol·L-1 | 5.3×10-7 | 4.3×10-6 | 1.3×10-4 | 3.7×10-2 |
分别说明PbCrO4在三种溶液中的溶解度都比在水中的大的原因
【知识点】 分子结构 酸碱理论和水溶液中的离子平衡 元素及其化合物的周期规律 有机化学
您最近一年使用:0次
填空题
|
适中(0.65)
3. 烟花爆竹常常在重大节日庆典中燃放。烟花的主要成分可以分成氧化剂、还原剂、发色剂、黏合剂等。
(1)爆竹的主要成分是黑火药,含有硝酸钾、硫黄和木炭。生成物中有一种单质,该单质分子的电子式是___________ 。
(2)用高氯酸钾代替硝酸钾,用糖类代替木炭和硫黄,可避免硫化钾、二氧化硫等有害物质的排放。请写出高氯酸钾(KClO4)与葡萄糖(C6H12O6)反应的化学方程式:___________ 。
(3)烟花中的发光剂,可用短周期金属的粉末,其燃烧时会发出白炽的强光。写出该金属的化学符号___________ 。
(4)烟花中还含有发色剂,利用焰色反应可使烟花放出五彩缤纷的色彩。焰色反应的原理是___________ 。
(1)爆竹的主要成分是黑火药,含有硝酸钾、硫黄和木炭。生成物中有一种单质,该单质分子的电子式是
(2)用高氯酸钾代替硝酸钾,用糖类代替木炭和硫黄,可避免硫化钾、二氧化硫等有害物质的排放。请写出高氯酸钾(KClO4)与葡萄糖(C6H12O6)反应的化学方程式:
(3)烟花中的发光剂,可用短周期金属的粉末,其燃烧时会发出白炽的强光。写出该金属的化学符号
(4)烟花中还含有发色剂,利用焰色反应可使烟花放出五彩缤纷的色彩。焰色反应的原理是
【知识点】 氧化还原反应方程式的配平解读 焰色试验解读 元素及其化合物的周期规律
您最近一年使用:0次
填空题
|
适中(0.65)
4. 土壤中的硫循环如图所示,回答下列问题。
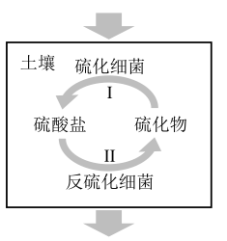
(1)土壤中的硫酸盐部分来自于降水,写出SO2转化为酸雨的化学方程式:___________ 。
(2) I中,土壤中的黄铁矿(FeS2)会转化成硫酸亚铁和硫酸,写出化学方程式:___________ 。
(3)某种反硫化细菌在过程II中要消耗乳酸,乳酸的作用是___________ 。
(4)某些硫酸盐溶液向地下深层渗透,遇到难溶硫化物时,缓慢转变为更难溶的硫化物。用离子方程式表示CuSO4遇ZnS的变化:___________ 。

(1)土壤中的硫酸盐部分来自于降水,写出SO2转化为酸雨的化学方程式:
(2) I中,土壤中的黄铁矿(FeS2)会转化成硫酸亚铁和硫酸,写出化学方程式:
(3)某种反硫化细菌在过程II中要消耗乳酸,乳酸的作用是
(4)某些硫酸盐溶液向地下深层渗透,遇到难溶硫化物时,缓慢转变为更难溶的硫化物。用离子方程式表示CuSO4遇ZnS的变化:
【知识点】 氧化还原反应方程式的配平解读 二氧化硫 氧化还原
您最近一年使用:0次
填空题
|
困难(0.15)
解题方法
5. 卡尔-费休(Karl-Fischer) 法是测定有机溶剂中的微量水含量的经典方法。所用试剂由碘、二氧化硫、吡啶(C5H5N,有机碱,与H+反应生成C5H5NH+)和无水甲醇按一定比例配制而成。该试剂与待测溶剂中的水反应后,产物的含量用库仑滴定法来测定。
(1)该方法的基本原理是利用碘与二氧化硫反应,反应方程式为___________ 。
(2)上述反应在测量条件下,是可逆反应,加入吡啶的作用是___________ 。
(3)加入甲醇可以进一步稳定产物,生成C5H5NHSO4CH3,请写出总反应。的化学方程式:___________ 。。
(4)测定20.0 mL有机溶剂含水量____ 。库仑滴定时,以24.8 mA恒定电流通电302s时达到反应终点(电极反应: 2I-- 2e = I2)。求该有机溶剂的含水量(mg·L-1) ____ 。已知: 1 mol电子的电量为9.65× 104C,电量计算公式Q=It
(1)该方法的基本原理是利用碘与二氧化硫反应,反应方程式为
(2)上述反应在测量条件下,是可逆反应,加入吡啶的作用是
(3)加入甲醇可以进一步稳定产物,生成C5H5NHSO4CH3,请写出总反应。的化学方程式:
(4)测定20.0 mL有机溶剂含水量
【知识点】 氧化还原反应有关计算 氧化还原反应方程式的配平解读 氧化还原
您最近一年使用:0次
三、计算题 添加题型下试题
计算题
|
适中(0.65)
6. 根据下列实验数据,写出CuSO4(s) 转化为CuSO4·5H2O(s)的热化学方程式________ (给出具体计算过程,保留整数)。
I.称取3.2 gCuSO4 (160g·mol-1) 置于盛有H2O的烧杯(33.5g) 中搅拌溶解,得到50 mL CuSO4溶液,溶液温度升高5.5 °C。
II.称取5.0 g CuSO4·5H2O (250 g·mol-1)置于盛有H2O的烧杯(33.5g)中搅拌溶解,得到50 mL CuSO4溶液,溶液温度降低1.0 °C。已知: 烧杯、CuSO4溶液的比热容分别为0.84J·g-1·K-1、4.2 J-1·mL-1·K-1。
I.称取3.2 gCuSO4 (160g·mol-1) 置于盛有H2O的烧杯(33.5g) 中搅拌溶解,得到50 mL CuSO4溶液,溶液温度升高5.5 °C。
II.称取5.0 g CuSO4·5H2O (250 g·mol-1)置于盛有H2O的烧杯(33.5g)中搅拌溶解,得到50 mL CuSO4溶液,溶液温度降低1.0 °C。已知: 烧杯、CuSO4溶液的比热容分别为0.84J·g-1·K-1、4.2 J-1·mL-1·K-1。
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
7. 文献记载,铁粉在稀硝酸中会放出氢气。某同学进行如下验证和对比实验。
实验I. 室温下 (20℃), 在恒压密闭容器内放入过量铁粉和 2.0 mL 0.5 mol·L–1 HNO3,立即有气体生成。充分反应后,所得溶液几乎无色,收集到无色气体 6.0 mL。将该气体通入有空气的试管,无明显变化。点燃气体,有尖锐爆鸣声,试管壁出现液滴。取反应后溶液,加入足量 NaOH 溶液得到灰绿色沉淀。煮沸时,蒸气略有刺激性气味并能使湿润红色石蕊试纸变蓝。
(1)气体产物为氢气的证据是______________________ 。
(2)根据实验现象, 写出铁粉与 0.5 mol·L–1 硝酸反应时还原反应的半反应方程式。① 2H+ + 2e– = H2↑; ②_____________ 。
(3)该同学对产生氢气的原因提出假设:
假设 1:该浓度的硝酸中 H+的氧化性大于NO3-;
假设 2: H+的还原速率大于NO3-的还原速率;
I. 验证假设 1:用____ (Cu或Mg)粉与_____ 硝酸反应,说明假设1不成立。实验证据是______________________ 。
II. 验证假设 2: 改变条件重复实验 I,结果如下(气体成分和溶液成分检验的现象与实验 I 相似)。
①根据实验现象,你认为假设2是否成立?简述理由。__________________________
②试分析温度对铁粉与硝酸反应生成氢气体积的影响。__________________________
(4)改用 3 mol·L–1 HNO3与过量铁粉反应, 有无色气体生成, 溶液变为深棕色。气体接触空气显红棕色,不可燃。 根据以上结论解释生成还原产物的原因__________________________
(5)综上所述,金属与硝酸生成氢气,需要控制哪些条件?__________________________________
实验I. 室温下 (20℃), 在恒压密闭容器内放入过量铁粉和 2.0 mL 0.5 mol·L–1 HNO3,立即有气体生成。充分反应后,所得溶液几乎无色,收集到无色气体 6.0 mL。将该气体通入有空气的试管,无明显变化。点燃气体,有尖锐爆鸣声,试管壁出现液滴。取反应后溶液,加入足量 NaOH 溶液得到灰绿色沉淀。煮沸时,蒸气略有刺激性气味并能使湿润红色石蕊试纸变蓝。
(1)气体产物为氢气的证据是
(2)根据实验现象, 写出铁粉与 0.5 mol·L–1 硝酸反应时还原反应的半反应方程式。① 2H+ + 2e– = H2↑; ②
(3)该同学对产生氢气的原因提出假设:
假设 1:该浓度的硝酸中 H+的氧化性大于NO3-;
假设 2: H+的还原速率大于NO3-的还原速率;
I. 验证假设 1:用
II. 验证假设 2: 改变条件重复实验 I,结果如下(气体成分和溶液成分检验的现象与实验 I 相似)。
| 序号 | 金属状态 | 反应温度 | 实验现象 |
| a | 铁粉 | 40℃ | 溶液略带黄色,气体 3.4 mL。 |
| b | 铁粉 | 60℃ | 黄色溶液,气体 2.6 mL。 |
②试分析温度对铁粉与硝酸反应生成氢气体积的影响。
(4)改用 3 mol·L–1 HNO3与过量铁粉反应, 有无色气体生成, 溶液变为深棕色。气体接触空气显红棕色,不可燃。 根据以上结论解释生成还原产物的原因
(5)综上所述,金属与硝酸生成氢气,需要控制哪些条件?
您最近一年使用:0次
2018-05-16更新
|
358次组卷
|
2卷引用:北京市门头沟区2018届高三5月综合练习(二)理综化学试题
解答题-结构与性质
|
困难(0.15)
解题方法
8. 类阴离子型层状化合物,其主体层板由二元(或多元)金属氢氧化物构成,最典型的例子是水滑石结构。
(1)下图代表了氢氧化镁的层板结构。图中黑线连接的菱形是一个最小二维晶胞,其中晶胞参数a=b=a0, α= 120°。一个晶胞中含有___________ 个OH- ,Mg2+的配位数是___________ 。

(2)将上图氢氧化镁的层板结构中的部分Mg2+用Al3+取代,可得化学式为Mg2Al(OH)6(CO3)x·H2O的一、种水滑石层板(结构如下图所示),x=______ ,其层板带 ____________ 电荷,____________ 进入层间平衡电荷。请在下图中画出最小二维晶胞(以图中Al为顶点) ______ 。每个镁氧八面体周围有_____ 个相邻铝氧八面体和 ______ 个相邻镁氧八面体。 忽略Al3+取代Mg2+对层板结构的影响,则天然的水滑石晶胞参数a'=_______ a0。
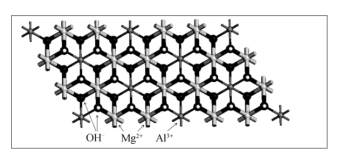
(3)层状复合金属氢氧化物在Z方向的堆积方式有两种,其中一种如下图所示。假设两个层板之间的距离为d0,层板厚度为田l0,则 此种堆积方式的晶胞参数c为___________ 。

(4)水滑石层间的阴离子可以被其他阴离子取代,因此水滑石可以作为离子交换剂,去除水体中阴离子。去除效果依次为: PO >CrO
>CrO > NO
> NO ,其原因是
,其原因是___________ 。
(1)下图代表了氢氧化镁的层板结构。图中黑线连接的菱形是一个最小二维晶胞,其中晶胞参数a=b=a0, α= 120°。一个晶胞中含有

(2)将上图氢氧化镁的层板结构中的部分Mg2+用Al3+取代,可得化学式为Mg2Al(OH)6(CO3)x·H2O的一、种水滑石层板(结构如下图所示),x=

(3)层状复合金属氢氧化物在Z方向的堆积方式有两种,其中一种如下图所示。假设两个层板之间的距离为d0,层板厚度为田l0,则 此种堆积方式的晶胞参数c为

(4)水滑石层间的阴离子可以被其他阴离子取代,因此水滑石可以作为离子交换剂,去除水体中阴离子。去除效果依次为: PO
 >CrO
>CrO > NO
> NO ,其原因是
,其原因是
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
9. EPR橡胶(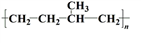 )和PC塑料(
)和PC塑料(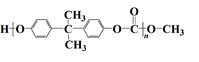 )的合成路线如下:
)的合成路线如下:

(1)A的名称是___________ 。
(2)C的结构简式____________ 。
(3)下列说法正确的是(选填字母)_______________ 。
A. 反应Ⅱ的原子利用率为100%
B. 反应Ⅲ为取代反应
C. 1 mol E与足量金属 Na 反应,最多可生成标准状况下22.4 L H2
D. CH3OH在合成PC塑料的过程中可以循环利用
(4)反应Ⅰ的化学方程式是_______________________________ 。
(5)反应Ⅳ的化学方程式是_______________________________ 。
(6)已知:

以D和乙酸为起始原料合成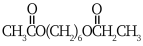 无机试剂任选,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明反应试剂和条件)。
无机试剂任选,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明反应试剂和条件)。______________
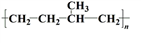 )和PC塑料(
)和PC塑料( )的合成路线如下:
)的合成路线如下:
(1)A的名称是
(2)C的结构简式
(3)下列说法正确的是(选填字母)
A. 反应Ⅱ的原子利用率为100%
B. 反应Ⅲ为取代反应
C. 1 mol E与足量金属 Na 反应,最多可生成标准状况下22.4 L H2
D. CH3OH在合成PC塑料的过程中可以循环利用
(4)反应Ⅰ的化学方程式是
(5)反应Ⅳ的化学方程式是
(6)已知:

以D和乙酸为起始原料合成
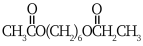 无机试剂任选,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明反应试剂和条件)。
无机试剂任选,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明反应试剂和条件)。
您最近一年使用:0次
2018-05-16更新
|
607次组卷
|
3卷引用:北京市门头沟区2018届高三5月综合练习(二)理综化学试题
解答题-有机推断题
|
困难(0.15)
10. 化合物I是一种抗癫痫药物,我国科学家近来发现I对消除由蜈蚣叮咬产生的严重临床症状有良好效果。I的两条合成路线如下图所示。___________ 。
(2) G的分子式是C9H11N3O4, 写出D、F、H、K、I的结构简式:_______
(3)由E生成F,和由B生成J的反应类型都是芳香取代反应,它们之间的不同之处是___________ 。
(4) 写出由B生成J反应中的中间体的各共振式(写出4个)_______ 。
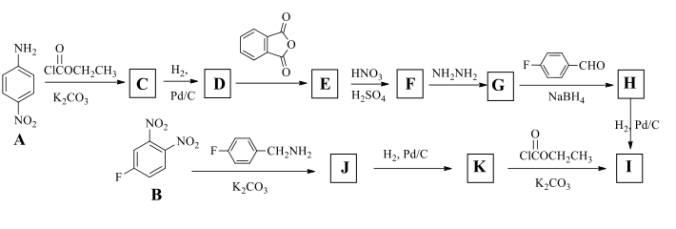
(2) G的分子式是C9H11N3O4, 写出D、F、H、K、I的结构简式:
(3)由E生成F,和由B生成J的反应类型都是芳香取代反应,它们之间的不同之处是
(4) 写出由B生成J反应中的中间体的各共振式(写出4个)
【知识点】 有机化学
您最近一年使用:0次
试卷分析
整体难度:较难
考查范围:化学反应原理、物质结构与性质、竞赛、认识化学科学、常见无机物及其应用、化学实验基础、有机化学基础
试卷题型(共 10题)
题型
数量
解答题
5
填空题
4
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、解答题 | |||
| 1 | 0.4 | 原电池原理的综合应用 根据晶胞结构确定晶体化学式 晶体 电化学 | 原理综合题 |
| 7 | 0.4 | 硝酸的强氧化性 物质性质的探究 | 实验探究题 |
| 8 | 0.15 | 物质结构与性质综合考查 晶胞的有关计算 离子配位数 晶体 | 结构与性质 |
| 9 | 0.65 | 有机合成综合考查 有机推断综合考查 | 有机推断题 |
| 10 | 0.15 | 有机化学 | 有机推断题 |
| 二、填空题 | |||
| 2 | 0.15 | 分子结构 酸碱理论和水溶液中的离子平衡 元素及其化合物的周期规律 有机化学 | |
| 3 | 0.65 | 氧化还原反应方程式的配平 焰色试验 元素及其化合物的周期规律 | |
| 4 | 0.65 | 氧化还原反应方程式的配平 二氧化硫 氧化还原 | |
| 5 | 0.15 | 氧化还原反应有关计算 氧化还原反应方程式的配平 氧化还原 | |
| 三、计算题 | |||
| 6 | 0.65 | 化学反应热的计算 化学热力学初步 | |



