2015届江苏省宿迁市高三上学期第一次摸底考试化学试卷
江苏
高三
阶段练习
2017-07-26
295次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、化学实验基础、物质结构与性质、化学反应原理、有机化学基础
一、单选题 添加题型下试题

下列关于碳纳米管的说法不正确的是
| A.碳纳米管属于一种有机合成纤维 |
| B.碳纳米管与金刚石互为同素异形体 |
| C.常温下,碳纳米管具有较好的稳定性 |
| D.碳纳米管比表面积大,可用作新型储氢材料 |
【知识点】 新型无机非金属材料 石墨、金刚石和C60解读
A.N2的电子式: |
B.CH4的比例模型: |
C.中子数为45的溴原子: Br Br |
D.对羟基苯甲酸的结构简式: |
【知识点】 化学用语
| A.0.1 mol·L-1 CH3COONa溶液:H+、Al3+、Cl-、NO3- |
| B.含有NaNO3的溶液:H+、Fe2+、SO42- 、Cl- |
| C.能使甲基橙变红的溶液:K+、Na+、NO3-、Cl- |
| D.由水电离产生的c(H+)=10-12 mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl- |
【知识点】 离子共存
| A.碳酸钠受热易分解,可用于生产食品发酵粉 |
| B.次氯酸钠具有强氧化性,可用于配制消毒液 |
| C.二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸 |
| D.二氧化硫有漂白、杀菌性能,可在食品生产中大量使用 |
A.称取样品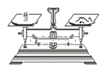 | B.样品溶解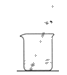 | C.氢氧化铝沉淀过滤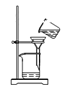 | D.灼烧氢氧化铝沉淀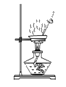 |
| A.常温常压下,11.2 L 乙烯所含碳原子数为NA |
| B.1L 0.1 mol•L-1的Al2(SO4)3溶液中,Al3+的数目为0.2 NA |
| C.32g O2和 O3的混合气体中含有的氧原子数为2NA |
| D.5.6 g铁粉在0.1 mol氯气中充分燃烧,转移电子数为0.3NA |
【知识点】 化学计量
| A.铜溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| B.氯气和水的反应:Cl2+H2O=2H++Cl-+ClO- |
| C.用氨水溶解氯化银沉淀:Ag++2 NH3·H2O=[Ag(NH3)2]++2H2O |
| D.将过量二氧化硫通入氨水中:SO2+NH3·H2O=HSO3-+NH+4 |
【知识点】 离子反应的发生及书写
 物质 物质组别 | 甲 | 乙 | 丙 |
| A | Mg | FeSO4 | O2 |
| B | Al2O3 | HCl | NaOH |
| C | CO2 | H2O | Na2O2 |
| D | NaHCO3 | Ca(OH)2 | Na2CO3 |
| A.A | B.B | C.C | D.D |
【知识点】 过氧化钠 碳酸钠与碳酸氢钠的相互转化解读 铝三角转化解读
| A.X与Y形成原子个数比为1∶1的化合物只有两种 |
| B.Y、W的氧化物均为酸性氧化物 |
| C.最高价氧化物对应水化物的酸性Y<W |
| D.X与Z形成的化合物中,各原子均满足8电子稳定结构 |
【知识点】 元素周期表 元素周期律
CuSO4(s)=Cu2+(aq)+SO42-(aq) ΔH2<0。
若CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)
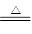 CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是| A.ΔH1<ΔH3 | B.ΔH2>ΔH3 | C.ΔH1+ΔH3=ΔH2 | D.ΔH1+ΔH2=ΔH3 |
【知识点】 盖斯定律及其有关计算
| A.在潮湿的环境中,铜容易发生析氢腐蚀形成铜绿 |
| B.常温下,将pH= 4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.反应SiO2(s)+ 3C(s)=SiC(s) + 2CO(g)室温下不能自发进行,则该反应的△H<0 |
| D.对于Ca(OH)2的沉淀溶解平衡,升高温度,Ca(OH)2的溶解速率增大,Ksp减小 |
【知识点】 沉淀溶解平衡
二、多选题 添加题型下试题

| A.有机物X的分子式为C12H15O3 |
| B.X分子中含有1个手性碳原子 |
| C.X在一定条件下能发生加成、取代、消去等反应 |
| D.在Ni作催化剂的条件下,1 mol X最多能与4 mol H2加成 |
【知识点】 烃的衍生物
三、单选题 添加题型下试题
| A.将一小块Na投入水中,钠浮于水面,说明钠密度比水小 |
| B.将一小块Na投入滴有酚酞的水中,溶液变红,说明反应生成了碱 |
| C.将一小块Na投入CuSO4溶液中,生成蓝色沉淀,说明Na没有Cu活泼 |
| D.点燃Na与肥皂水反应产生的气泡,有尖锐爆鸣声,说明有H2生成 |
四、多选题 添加题型下试题
A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液:c(SO42-)>c( )>c(Fe2+)>c(H+) )>c(Fe2+)>c(H+) |
B.0.1 mol·L-1 NaHCO3溶液:c(Na+)+c(H+)=c( )+c( )+c( )+c(OH-) )+c(OH-) |
| C.0.1 mol·L-1Na2S溶液:2c(Na+) =c(S2-)+c(HS-) +c(H2S) |
| D.0.01 mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
【知识点】 盐类的水解
 2NaNO3(s)+2NO(g)+ Cl2(g),ΔH。在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是
2NaNO3(s)+2NO(g)+ Cl2(g),ΔH。在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是| A.10min内NO浓度变化表示的速率v(NO)=0.01 mol·L-1·min-1 |
| B.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α |
| C.若升高温度,平衡逆向移动,则该反应的ΔH>0 |
| D.若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行 |
【知识点】 化学平衡的有关计算
五、填空题 添加题型下试题

(1)酸浸时发生的反应的离子方程式为
(2)配制TiCl4溶液时,通常将TiCl4溶于浓盐酸,目的是
(3)加入H2C2O4溶液时,发生反应的化学方程式为
(4)煅烧得到BaTiO3的同时,生成高温下的气体产物有CO、
【知识点】 化学实验基础
六、解答题 添加题型下试题

已知:乙酸酐的结构简式为

请回答下列问题:
(1)G物质中的含氧官能团的名称是
(2)反应A→B的化学方程式为
(3)上述④、⑤变化过程的反应类型分别是
(4)写出满足下列条件的C的同分异构体的结构简式:
Ⅰ.苯环上只有两种取代基。
Ⅱ.分子中只有4种不同化学环境的氢。
Ⅲ.能与NaHCO3反应生成CO2。
(5)根据已有知识并结合相关信息,写出以
 和乙酸酐为原料制备
和乙酸酐为原料制备 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:CH3CH2Br
 CH3CH2OH
CH3CH2OH CH3COOCH2CH3
CH3COOCH2CH3
①准确称取2.0120g样品配成100mL溶液A。
②准确量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.466g。
③准确量取25.00mL溶液A,加入足量的KI溶液,以淀粉为指示剂,用0.1250 mol·L-1的Na2S2O3溶液滴定,消耗8.00mL至终点(已知:I2+2Na2S2O3=2NaI+Na2S4O6)。
(1)要检验出A溶液中存在的Fe3+,可以加入
(2)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO42-)≤1.0×10-5 mol•L-1,应保持溶液中c(Ba2+)≥
(3)步骤③中判断滴定终点的方法是
(4)通过计算确定铁钾矾的组成(写出计算过程)
(1)同学甲设计实验检验废气A中含有CO2,应选择的试剂有
A.NaOH溶液 B.酸性KMnO4溶液 C.澄清石灰水 D.盐酸
(2)同学乙欲测定废气A中SO2的含量,取a L废气A并设计了如下装置进行实验。

①为了保证实验成功,装置A应具有的现象是
②同学丙认为A装置前后的质量差就是a L废气中含有的SO2的质量,然后进行含量计算。经小组讨论后,同学丁提出疑问,按照同学丙的实验,若废气中SO2完全被吸收,则最后测定的结果应该偏大,同学丁推断的理由是
(3)兴趣小组的同学查阅资料发现可利用硫酸工业废气A制备皓矾(ZnSO4·7H2O)。实验模拟制备皓矾工业流程如下:

①氧化中加入硫酸铁发生反应的离子方程式是
②加入Zn粉的目的是
③固体A主要成分是
④操作b得到纯净皓矾晶体,必要的操作是蒸发浓缩、
【知识点】 化学实验基础
(1)空气阴极法电解制备H2O2的装置如下图所示,主要原理是在碱性电解质溶液中,通过利用空气中氧气在阴极还原得到H2O2和稀碱的混合物。试回答:

①直流电源的a极名称是
②阴极电极反应式为
③1979年,科学家们用CO、O2和水在三苯膦钯的催化下室温制得了H2O2。相对于电解法,该方法具有的优点是安全、
(2)Fe3+对H2O2的分解具有催化作用。利用图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的

(3)用H2O2和H2SO4的混合溶液可溶解印刷电路板金属粉末中的铜。反应的离子方程式是
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| Cu的平均溶解速率 (×10-3mol·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
七、填空题 添加题型下试题
(1)Fe基态原子核外电子排布式为
(2)H、N、O的电负性从小到大的顺序是
(3)与NO
 互为等电子体的一种分子为
互为等电子体的一种分子为(4)1mol苯分子中含有σ键的数目为
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为

【知识点】 分子结构与性质
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 新型无机非金属材料 石墨、金刚石和C60 | |
| 2 | 0.64 | 化学用语 | |
| 3 | 0.64 | 离子共存 | |
| 4 | 0.65 | 二氧化硫的漂白性 二氧化硅的用途 硅酸钠的俗名和用途 | |
| 5 | 0.65 | 仪器使用与实验安全 物质分离、提纯的常见物理方法 物质分离、提纯综合应用 常见无机物的制备 | |
| 6 | 0.64 | 化学计量 | |
| 7 | 0.64 | 离子反应的发生及书写 | |
| 8 | 0.65 | 过氧化钠 碳酸钠与碳酸氢钠的相互转化 铝三角转化 | |
| 9 | 0.64 | 元素周期表 元素周期律 | |
| 10 | 0.65 | 盖斯定律及其有关计算 | |
| 11 | 0.64 | 沉淀溶解平衡 | |
| 13 | 0.65 | 钠的化学性质 钠与水反应原理 钠与盐溶液的反应 | |
| 二、多选题 | |||
| 12 | 0.64 | 烃的衍生物 | |
| 14 | 0.4 | 盐类的水解 | |
| 15 | 0.4 | 化学平衡的有关计算 | |
| 三、填空题 | |||
| 16 | 0.4 | 化学实验基础 | |
| 21 | 0.4 | 分子结构与性质 | |
| 四、解答题 | |||
| 17 | 0.4 | 根据题给物质选择合适合成路线 有机合成综合考查 有机推断综合考查 | 有机推断题 |
| 18 | 0.4 | 酸碱中和滴定原理的应用 溶度积常数相关计算 探究物质组成或测量物质的含量 | 实验探究题 |
| 19 | 0.4 | 化学实验基础 | 实验探究题 |
| 20 | 0.4 | 影响化学反应速率的因素 电解原理的应用 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |



