广东省四校2022届高三上学期第一次联考化学试题
广东
高三
阶段练习
2022-01-23
634次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学反应原理、化学实验基础
广东省四校2022届高三上学期第一次联考化学试题
广东
高三
阶段练习
2022-01-23
634次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学反应原理、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. 中华民族的发明创造为人类文明进步做出了巨大贡献。下列古代发明及应用中,不涉及 化学变化的是
| A.粮食酿酒 | B.陶瓷烧制 | C.铁的冶炼 | D.辘轳汲水 |
 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-19更新
|
185次组卷
|
2卷引用:广东省四校2022届高三上学期第一次联考化学试题
单选题
|
适中(0.65)
解题方法
2. 《中国诗词大会》是中央电视台制作的特别节目,以弘扬中华传统诗词之美,促进中华传统文化的传承和发扬。请你从化学视角分析,下列说法错误 的是
| A.“千锤万凿出深山,烈火焚烧若等闲”描述的是石灰石的煅烧 |
| B.“朝坛雾卷,曙岭烟沉”,雾、烟均能产生丁达尔效应 |
| C.“独忆飞絮鹅毛下,非复青丝马尾垂”,“飞絮”、“鹅毛”主要成分都是蛋白质 |
| D.“纷纷灿烂如星陨,赫赫喧豗似火攻”中烟花是某些金属的焰色反应,属于物理变化 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
3. 自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表的成员数目不断增加。2006年,科学家以钙离子撞击锎(Cf)钯,产生了一种超重元素: (Og),其反应可表示为:
(Og),其反应可表示为: +
+ →
→ +3
+3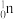 。下列说法正确的是
。下列说法正确的是
 (Og),其反应可表示为:
(Og),其反应可表示为: +
+ →
→ +3
+3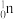 。下列说法正确的是
。下列说法正确的是A. 的核外电子数是118 的核外电子数是118 |
B. Ca与 Ca与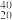 Ca互为同素异形体 Ca互为同素异形体 |
C. Cf原子核内有98个质子,249个中子 Cf原子核内有98个质子,249个中子 |
D.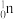 为一种新的核素 为一种新的核素 |
您最近一年使用:0次
2022-01-19更新
|
239次组卷
|
4卷引用:广东省四校2022届高三上学期第一次联考化学试题
广东省四校2022届高三上学期第一次联考化学试题(已下线)考点06 原子结构-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点06 原子结构(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)黑龙江省实验中学2023-2024学年高一上学期第二次阶段测试化学试题
单选题
|
较易(0.85)
解题方法
4. “科技创造价值,创新驱动发展”。下列有关科技成果解读错误 的是
| 选项 | 科技成果 | 相关知识 |
| A | 碳纤维具备“外柔内刚”的特性且密度小 | 可用于制造无人机外壳 |
| B | 我国首套吨级的氢液化系统研制成功 | 液氢气化时因断裂化学键而吸热 |
| C | 我国科学家首次利用CO2和H2人工合成淀粉 | 有助于实现碳达峰、碳中和 |
| D | 我国科学家首次成功以CO为原料合成蛋白质 | 可制造新型的饲料蛋白,确保国家粮食安全和实现绿色可持续发展 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 关于化合物 ,下列说法
,下列说法错误 的是
 ,下列说法
,下列说法| A.能与溴水反应 |
| B.该物质最多与4molH2反应 |
| C.能与碳酸钠的水溶液发生反应 |
| D.分子中所有原子均处同一平面 |
您最近一年使用:0次
单选题
|
较易(0.85)
6. “劳动是幸福的源泉”,下列劳动项目所涉及的化学知识错误 的是
| 选项 | 劳动项目 | 化学知识 |
| A | 使用纯碱溶液去油污 | NaHCO3水解使溶液显碱性 |
| B | 使用草木灰对蔬菜施肥 | 草木灰属于钾肥 |
| C | 白醋除水垢 | 醋酸酸性强于碳酸 |
| D | 侯德榜制碱法 | 利用了物质溶解度的不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
7. 在制备并纯化乙酸乙酯的实验中,下列操作未涉及 的是
A. | B. | C. | D. |
【知识点】 乙酸乙酯制备实验的装置及操作解读
您最近一年使用:0次
2022-01-19更新
|
144次组卷
|
2卷引用:广东省四校2022届高三上学期第一次联考化学试题
单选题
|
适中(0.65)
8. NA代表阿伏加德罗常数的数值。下列说法正确的是
| A.1molCl2与足量H2O充分反应后,转移电子数为NA个 |
| B.常温常压下,16gO3和O2的混合气体,所含质子数为8NA |
| C.0.5molSO3溶于1L水,可得到0.5mol·L-1的H2SO4溶液 |
| D.标准状况下,22.4LNO和11.2LO2充分反应后,所含的分子数为NA |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
9. 宏观辨识与微观探析是化学学科核心素养之一。下列事实与对应离子方程式均正确的是
| 选项 | 事实 | 离子方程式 |
| A | 用酸性高锰酸钾溶液滴定草酸 | 2MnO +6H++5H2C2O4=2Mn2++10CO2↑+8H2O +6H++5H2C2O4=2Mn2++10CO2↑+8H2O |
| B | H2SO3酸性强于HClO | SO2+H2O+2ClO-=2HClO+SO |
| C | 铁盐净水 | Fe3++3H2O=Fe(OH)3↓+3H+ |
| D | Na2O2与H2O反应,可用作供氧剂 | Na2O2+H2O=2Na++2OH-+O2↑ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10. 天然气因含有少量H2S等气体开采应用受限,T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法不正确的是
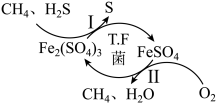

| A.该脱硫过程中Fe2(SO4)3可循环利用 |
| B.由脱硫过程可知,氧化性强弱Fe2(SO4)3<S<O2 |
| C.脱硫过程中O2间接氧化H2S |
| D.副产物硫单质可以用来制硫酸、化肥、火柴及杀虫剂等 |
您最近一年使用:0次
2020-03-09更新
|
309次组卷
|
7卷引用:山东省枣庄市2020届高三上学期期末考试化学试题
单选题
|
适中(0.65)
11. 价类二维图是学习元素及其化合物知识的重要模型,且体现了化学变化之美。下图为氯元素的价类二维图。下列说法正确的是


A.a的形成过程: |
| B.a与d,a与f在酸性情况下反应,均可以得到b |
| C.工业上可利用阴离子交换膜电解饱和e溶液制备烧碱 |
| D.c的水溶液能够杀菌消毒,为一种新型絮凝剂 |
您最近一年使用:0次
单选题
|
适中(0.65)
12. 一种由短周期主族元素组成的化合物(如下图所示),可用作新能源电池的优质电解质。其中元素M、X、Y、Z、W的原子序数依次增大,且总和为42;Y与W是同族元素。下列叙述正确 的是


| A.M单质应保存在煤油中 |
| B.氢化物沸点Y>Z>X |
| C.原子半径M>X>Y>Z |
| D.最高价氧化物对应水化物的酸性:Z>W>X |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
13. 根据下列实验操作和现象所得出的结论均正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向蔗糖溶液中加入1mL稀硫酸,充分水浴加热,然后加入银氨溶液 | 无银镜出现 | 蔗糖没有发生水解 |
| B | 常温下,测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向2mL0.1mol·L-1MgCl2溶液中加入5mL0.1mol·L-1NaOH溶液。出现白色沉淀后,继续滴入几滴FeCl3浓溶液,静置 | 出现红褐色沉淀 | 同温下,Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 在一块除去铁锈的铁片上面滴一滴含有酚酞的食盐水,静置一段时间 | 溶液边缘出现 红色 | 铁片上发生了吸氧腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-19更新
|
536次组卷
|
5卷引用:广东省四校2022届高三上学期第一次联考化学试题
广东省四校2022届高三上学期第一次联考化学试题(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)仿真卷01-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)黑龙江省牡丹江市第二高级中学2023-2024学年高三下学期考前热身卷化学(三)试题
二、多选题 添加题型下试题
多选题
|
适中(0.65)
14. 为减少对环境造成的影响,发电厂试图采用以下方法将废气排放中的CO进行合理利用,以获得重要工业产品。Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下:
①Cl2(g)⇌2Cl•(g) 快;
②CO(g)+Cl•(g)⇌COCl•(g) 快;
③COCl•(g)+Cl2(g)⇌COCl2(g)+Cl•(g) 慢。
反应②的速率方程v正=k正c(CO)×c(Cl•),v逆=k逆c(COCl•),k正、k逆是速率常数。下列说法错误 的是
①Cl2(g)⇌2Cl•(g) 快;
②CO(g)+Cl•(g)⇌COCl•(g) 快;
③COCl•(g)+Cl2(g)⇌COCl2(g)+Cl•(g) 慢。
反应②的速率方程v正=k正c(CO)×c(Cl•),v逆=k逆c(COCl•),k正、k逆是速率常数。下列说法
A.反应②的平衡常数K= |
| B.反应①的活化能大于反应③的活化能 |
| C.要提高合成COCl2的速率,关键是提高反应③的速率 |
| D.使用合适的催化剂可以增大该反应体系中COCl2(g)的体积分数 |
【知识点】 碰撞理论及活化能解读 活化能及其对反应速率的影响解读
您最近一年使用:0次
三、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
15. 科学家最近开发出一种新系统,“溶解”水中的二氧化碳,以触发电化学反应,生成电能和氢气,其工作原理如图所示。下列有关说法错误 的是
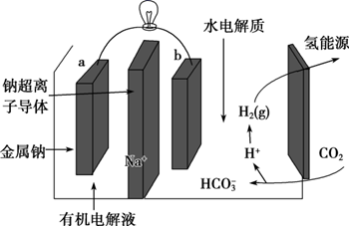

| A.a极为电源负极,电子从a极沿导线流向b极 |
| B.电解一段时间后b极区pH变小 |
| C.b极区可能会析出固体 |
D.b极区的电极反应式为2CO2+2H2O+2e﹣=2HCO +H2 +H2 |
您最近一年使用:0次
单选题
|
适中(0.65)
16. 乙二胺(H2NCH2CH2NH2)是二元弱碱(已知:25℃时,Kb1=10-4,Kb2=10-7),其水溶液与NH3水溶液的电离方式相似。现用锥形瓶装10 mL0.1 mol·L-1乙二胺溶液,用0.1 mol·L-1盐酸滴定。下列叙述错误 的是
| A.乙二胺在水溶液中的第一步电离方程式H2NCH2CH2NH2+H2O⇌[H2NCH2CH2NH3]++OH- |
| B.选用甲基橙作指示剂,可以很好地判断滴定终点 |
| C.滴入10.00 mL盐酸时,溶液呈碱性 |
| D.滴入20.00 mL盐酸时,混合溶液中有c(H2NCH2CH2NH2)+c([H2NCH2CH2NH3]+)+c([H3NCH2CH2NH3]2+)=c(Cl-) |
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
17. “证据推理”是化学实验的一般方法,某化学小组进行以下探究。
I.以亚硝酸钠(NaNO2)溶液为研究对象,探究HNO2的性质。(本实验稀硫酸均为1mol/LH2SO4)
II.探究HNO2和HNO3的氧化性
(1)写出实验4中溶液先变黄的离子方程式:_______ ,后变成棕色的离子方程式为:Fe2++NO⇌[Fe(NO)]2+。
(2)稍等片刻,实验5中溶液A中的棕色逐渐消失,请解释其原因:_______ 。
(3)根据实验4~7,可以得出有关HNO2和HNO3氧化性强弱的结论:
①不同浓度的HNO3溶液,浓HNO3氧化性强于稀HNO3。
②_______ 。
(4)另取试管甲,加入少量Cu粉,加入2mL1mol/L的NaNO2溶液,再滴入5滴稀硫酸,马上观察到Cu粉上和溶液里有大量气泡,溶液变浅蓝色,液面上方出现红棕色气体。再取试管乙,也加入少量Cu粉,加入2mL1mol/L的NaNO3,再滴入5滴稀硫酸,请预测实验现象:_______ 。
I.以亚硝酸钠(NaNO2)溶液为研究对象,探究HNO2的性质。(本实验稀硫酸均为1mol/LH2SO4)
 | 操作和现象 | 结论 |
| 实验1:滴入几滴 | 可推断HNO2为弱酸。 | |
| 实验2:滴入1mL0.1mol/LKMnO4溶液,开始仍为紫红色,再向溶液中滴加 | 可推断HNO2具有 | |
| 实验3:滴入5滴稀硫酸,溶液中很快就产生无色气泡,在液面上方出现红棕色气体。 | 可推断HNO2非常不稳定。写出此现象的化学方程式: |
 | 操作和现象 |  | 操作和现象 |
| 实验4:滴入5滴1mol/LFeSO4溶液(pH=0.5),溶液变黄,迅速变为棕色,再滴加KSCN溶液后溶液变红。(资料:[Fe(NO)]2+在溶液中呈棕色。) | 实验5:滴入5滴1mol/LFeSO4溶液(pH=0.5),几乎无现象。 将试管内溶液改为浓HNO3,重复上述操作,则溶液变黄,迅速变为棕色,得到溶液A。 | ||
| 实验6:滴入5滴淀粉碘化钾溶液,不变色,再滴入几滴稀硫酸,很快变蓝色。 | 实验7:滴入5滴淀粉碘化钾溶液,再滴入足量稀硫酸,仍然不变色。 将试管内溶液改为浓HNO3,滴入5滴淀粉碘化钾溶液,溶液很快变蓝。 |
(2)稍等片刻,实验5中溶液A中的棕色逐渐消失,请解释其原因:
(3)根据实验4~7,可以得出有关HNO2和HNO3氧化性强弱的结论:
①不同浓度的HNO3溶液,浓HNO3氧化性强于稀HNO3。
②
(4)另取试管甲,加入少量Cu粉,加入2mL1mol/L的NaNO2溶液,再滴入5滴稀硫酸,马上观察到Cu粉上和溶液里有大量气泡,溶液变浅蓝色,液面上方出现红棕色气体。再取试管乙,也加入少量Cu粉,加入2mL1mol/L的NaNO3,再滴入5滴稀硫酸,请预测实验现象:
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
18. 碳酸铝铵热解法是近几年发展起来的液相制备氧化铝超细粉末的新方法。由铝土矿(含Al2O3,Fe2O3及SiO2)制备超细氧化铝粉末的一种工艺流程如下:

回答下列问题:
(1)焙烧过程中,铝、铁的氧化物分别转化为NH4A1(SO4)2和NH4Fe(SO4)2。写出A12O3与(NH4)2SO4反应的化学方程式:_______ 。
(2)滤渣1的主要成分是_______ ,滤渣2的主要成分是_______ 。
(3)过滤3得到的固体为NH4A1(OH)2CO3,写出烧结的化学方程式:_______ 。
(4)本流程两次用到试剂X,则试剂X为:_______ 。
(5)本工艺的难点在于第一步焙烧环节,选取合适的条件提高铁和铝的提取率。科研人员把(NH4)2SO4和铝土矿按特定比例混合,做以下研究:

①图1显示,最佳焙烧温度为:_______ ℃,图2是在此温度下进一步研究,则最佳恒温时间为_______ min。
②请分析图1中,焙烧温度超过450℃,提取率迅速下降的可能原因是_______ 。
(6)该流程中可以循环利用的物质有_______ 。

回答下列问题:
(1)焙烧过程中,铝、铁的氧化物分别转化为NH4A1(SO4)2和NH4Fe(SO4)2。写出A12O3与(NH4)2SO4反应的化学方程式:
(2)滤渣1的主要成分是
(3)过滤3得到的固体为NH4A1(OH)2CO3,写出烧结的化学方程式:
(4)本流程两次用到试剂X,则试剂X为:
(5)本工艺的难点在于第一步焙烧环节,选取合适的条件提高铁和铝的提取率。科研人员把(NH4)2SO4和铝土矿按特定比例混合,做以下研究:

①图1显示,最佳焙烧温度为:
②请分析图1中,焙烧温度超过450℃,提取率迅速下降的可能原因是
(6)该流程中可以循环利用的物质有
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
19. 2021年9月,中科院研究所首次实现CO2到淀粉的合成。研究团队通过催化剂ZnO-ZrO2将酶促过程与CO2还原相结合,先合成甲醇再继续合成淀粉,其反应方程式如下:CO2(g)+3H2(g)→CH3OH(g)+H2O(g) ΔH
(1)可以通过燃烧热等数据的计算来求某反应的反应热,若已知CH3OH的燃烧热,则计算上述反应的ΔH,还需要查到的数据有:_______ 。
(2)在一定体积密闭容器中,通入CO2和H2,下表所列数据是上述反应在不同温度下的化学平衡常数数值,已知a>b>c:
①反应并达到平衡后,保持其他条件不变,升高温度,此反应的化学平衡应_______ 移动。(填“正向”、“逆向”或“不”)
②能判断该反应是否达到化学平衡状态的依据是_______ (填字母)
A.混合气体的密度不变
B.混合气体中H2浓度保持不变
C.混合气体的平均相对分子质量不变
D.3molH-H键断裂的同时有2molH-O键断裂
(3)在380K时,向1L的密闭容器中通入0.02molCO2和0.04molH2,测得其压强(p)随着时间(t)变化如下图曲线a所示:

①反应开始至达到平衡时时,v(H2)=_______ ;该温度下的平衡常数为K=_______ 。
②若只改变某一条件,其他条件相同时,曲线变化为b,则改变的条件是:_______ 。
(4)科学家一直从催化性能、电解能力等方面研究电催化还原CO2制备甲醇等高附加值类化工产品。电解CO2制甲醇的原理示意图如图所示。

①装置中的Pt电极应与电源的_______ 相连;
②反应时的阴极反应式为:_______ 。
(1)可以通过燃烧热等数据的计算来求某反应的反应热,若已知CH3OH的燃烧热,则计算上述反应的ΔH,还需要查到的数据有:
(2)在一定体积密闭容器中,通入CO2和H2,下表所列数据是上述反应在不同温度下的化学平衡常数数值,已知a>b>c:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | a | b | c |
①反应并达到平衡后,保持其他条件不变,升高温度,此反应的化学平衡应
②能判断该反应是否达到化学平衡状态的依据是
A.混合气体的密度不变
B.混合气体中H2浓度保持不变
C.混合气体的平均相对分子质量不变
D.3molH-H键断裂的同时有2molH-O键断裂
(3)在380K时,向1L的密闭容器中通入0.02molCO2和0.04molH2,测得其压强(p)随着时间(t)变化如下图曲线a所示:

①反应开始至达到平衡时时,v(H2)=
②若只改变某一条件,其他条件相同时,曲线变化为b,则改变的条件是:
(4)科学家一直从催化性能、电解能力等方面研究电催化还原CO2制备甲醇等高附加值类化工产品。电解CO2制甲醇的原理示意图如图所示。

①装置中的Pt电极应与电源的
②反应时的阴极反应式为:
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
20. 人体必需的元素包括常量元素与微量元素,常量元素包括碳、氢、氧、氮、钙、镁等,微量元素包括铁、铜、锌、氟、碘等,这些元素形成的化合物种类繁多,应用广泛。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出Fe2+的核外电子排布式___________ 。
(2)1个Cu2+与2个H2N—CH2—COO−形成含两个五元环结构的内配盐(化合物),其结构简式为___________ (用→标出配位键),在H2N—CH2—COO−中,属于第二周期的元素的第一电离能由大到小的顺序是___________ (用元素符号表示),N、C原子存在的相同杂化方式是___________ 杂化。
(3)碳酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径r(Mg2+)=66 pm,r(Ca2+)=99 pm,r(Sr2+)=112 pm,r(Ba2+)=135 pm;碳酸盐分解温度T(MgCO3)=402℃,T(CaCO3)=825℃,T(SrCO3)=1172℃,T(BaCO3)=1360℃。分析数据得出的规律是___________ ,解释出现此规律的原因是___________ 。
(4)自然界的氟化钙矿物为萤石或氟石,CaF2的晶体结构呈立方体形,其结构如下:

①两个最近的F−之间的距离是___________ pm(用含m的代数式表示)。
②CaF2晶胞体积与8个F−形成的立方体的体积比为___________ 。
③CaF2晶胞的密度是___________ g·cm−3(化简至带根号的最简式,NA表示阿伏加 德罗常数的值)。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出Fe2+的核外电子排布式
(2)1个Cu2+与2个H2N—CH2—COO−形成含两个五元环结构的内配盐(化合物),其结构简式为
(3)碳酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径r(Mg2+)=66 pm,r(Ca2+)=99 pm,r(Sr2+)=112 pm,r(Ba2+)=135 pm;碳酸盐分解温度T(MgCO3)=402℃,T(CaCO3)=825℃,T(SrCO3)=1172℃,T(BaCO3)=1360℃。分析数据得出的规律是
(4)自然界的氟化钙矿物为萤石或氟石,CaF2的晶体结构呈立方体形,其结构如下:

①两个最近的F−之间的距离是
②CaF2晶胞体积与8个F−形成的立方体的体积比为
③CaF2晶胞的密度是
您最近一年使用:0次
2020-03-21更新
|
231次组卷
|
4卷引用:理科综合化学-学科网3月第三次在线大联考(新课标Ⅲ卷)
(已下线)理科综合化学-学科网3月第三次在线大联考(新课标Ⅲ卷)学科网2020年3月第三次在线大联考(山东卷)化学试题河北省邯郸市肥乡区第一中学2022届高三开学考试化学试卷广东省四校2022届高三上学期第一次联考化学试题
解答题-有机推断题
|
适中(0.65)
21. 有机化合物F、I都是重要的化工产品,可用于航空、医药等领域,某研究小组的合成路线如下(部分试剂及反应条件省略):

已知:ⅰ.
ⅱ.
请回答以下问题:
(1)A是一种饱和一氯代烷,请写出A的名称_______ 。
(2)写出G中含氧官能团的名称_______ 。
(3)D→E的反应类型_______ ,E→F的化学反应方程式_______ 。
(4)写出I的结构简式_______ 。
(5)J是H的同分异构体,是一种芳香族化合物,满足下列2个条件:
①1molJ与足量的NaHCO3完全反应,放出标准状况下的气体44.8L
②苯环上有且仅有3条侧链
符合上述条件的J的同分异构体有_______ 种,其中核磁共振氢谱有五个峰,峰面积之比为3:2:2:2:1的结构简式为_______ 。(写出一种)
(6)以 ,
, 和1,3-丁二烯为原料,其他无机试剂任选,合成
和1,3-丁二烯为原料,其他无机试剂任选,合成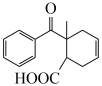 的路线(不需注明反应条件,但必要的反应物要写在“→”上方)
的路线(不需注明反应条件,但必要的反应物要写在“→”上方)_______ 。

已知:ⅰ.

ⅱ.

请回答以下问题:
(1)A是一种饱和一氯代烷,请写出A的名称
(2)写出G中含氧官能团的名称
(3)D→E的反应类型
(4)写出I的结构简式
(5)J是H的同分异构体,是一种芳香族化合物,满足下列2个条件:
①1molJ与足量的NaHCO3完全反应,放出标准状况下的气体44.8L
②苯环上有且仅有3条侧链
符合上述条件的J的同分异构体有
(6)以
 ,
, 和1,3-丁二烯为原料,其他无机试剂任选,合成
和1,3-丁二烯为原料,其他无机试剂任选,合成 的路线(不需注明反应条件,但必要的反应物要写在“→”上方)
的路线(不需注明反应条件,但必要的反应物要写在“→”上方)
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学反应原理、化学实验基础
试卷题型(共 21题)
题型
数量
单选题
15
多选题
1
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 物理变化与化学变化 | |
| 2 | 0.65 | 胶体的性质和应用 焰色试验 蛋白质的来源及作用 | |
| 3 | 0.85 | 原子中相关数值及其之间的相互关系 元素、核素、同位素 几组常见同素异形体 | |
| 4 | 0.85 | 蛋白质 化学科学对人类文明发展的意义 低碳经济 绿色化学与可持续发展 | |
| 5 | 0.65 | 含碳碳双键物质的性质的推断 有机分子中原子共面的判断 含有酚羟基的物质性质的推断 多官能团有机物的结构与性质 | |
| 6 | 0.85 | 碳酸钠 盐类水解的应用 乙酸具有酸的通性 | |
| 7 | 0.65 | 乙酸乙酯制备实验的装置及操作 | |
| 8 | 0.65 | 阿伏加德罗常数的求算 22.4L/mol适用条件 物质的量浓度概念、含义 二氧化氮与四氧化二氮的相互转化 | |
| 9 | 0.65 | 离子方程式的正误判断 氧化还原反应方程式的配平 过氧化钠与水的反应 水解的离子方程式书写 | |
| 10 | 0.65 | 氧化还原反应方程式的配平 氧化还原反应在生活、生产中的应用 | |
| 11 | 0.65 | 共价型分子结构式、电子式 次氯酸及其性质 电解池电极反应式及化学方程式的书写与判断 氯碱工业 | |
| 12 | 0.65 | 碱金属单质的保存 元素非金属性强弱的比较方法 微粒半径大小的比较方法 | |
| 13 | 0.65 | 沉淀转化 吸氧腐蚀 元素非金属性强弱的比较方法 物质性质实验方案的设计 | |
| 15 | 0.65 | 原电池原理理解 原电池电子流向判断及应用 原电池正负极判断 原电池电极反应式书写 | |
| 16 | 0.65 | 酸碱中和滴定原理的应用 电离平衡常数及影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐的水解常数 | |
| 二、多选题 | |||
| 14 | 0.65 | 碰撞理论及活化能 活化能及其对反应速率的影响 | |
| 三、解答题 | |||
| 17 | 0.65 | 氧化性、还原性强弱的比较 硝酸的强氧化性 Fe2+的鉴别及其应用 铁盐的检验 | 实验探究题 |
| 18 | 0.65 | 氨气 二氧化硅 常见无机物的制备 | 工业流程题 |
| 19 | 0.65 | 盖斯定律的应用 化学平衡常数 化学平衡状态的判断方法 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 20 | 0.4 | 物质结构与性质综合考查 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | 结构与性质 |
| 21 | 0.65 | 有机反应类型 根据要求书写同分异构体 有机物的推断 根据题给物质选择合适合成路线 | 有机推断题 |



