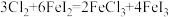2016届吉林省扶余市第一中学高三上学期第一次月考化学试卷
吉林
高三
阶段练习
2017-07-27
187次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、有机化学基础、化学反应原理、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
| A.煤经过气化和液化两个物理变化,可变为清洁能源 |
| B.葡萄糖可以制乙醇,两者都能与金属钠反应 |
| C.明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视 |
| D.合成纤维和光导纤维都是有机高分子化合物 |
【知识点】 化石能源
| A.Cu(OH)2+HCl;Cu(OH)2+CH3COOH |
| B.NaHCO3+H2SO4;KHCO3+HCl |
| C.NaHCO3+NaOH;Ca(HCO3)2+NaOH |
| D.BaCl2+H2SO4;Ba(OH)2+H2SO4 |
【知识点】 离子反应的发生及书写
| A.OH- | B.Na+ | C.HCO3- | D.Cl- |
【知识点】 离子反应
| A.18g D2O和18g H2O中含有的质子数均为10NA |
| B.2L 0.5 mol·L-1亚硫酸溶液中含有的H+离子数为2NA |
| C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |
| D.标准状况下,2.24L Cl2与过量的稀FeI2溶液反应,转移电子总数为0.1NA |
【知识点】 化学计量
①淀粉和纤维素的化学式都可用(C6H10O5)n表示,它们互为同分异构体
②聚乙烯、油脂、铜氨纤维、光导纤维都属于高分子
③氨水、冰醋酸、水都是电解质
④漂白粉、水玻璃、福尔马林都是混合物
⑤干馏、裂化、盐析都是化学变化
⑥植物油、直馏汽油、环己烷都可以用来萃取溴水中的溴单质
| A.1 | B.2 | C.3 | D.4 |
【知识点】 物质的分类
| A.利用一束强光照射明矾溶液,产生光亮的“通路”,说明明矾一定发生了水解 |
| B.向盛有Fe(NO3)2溶液的试管中加入0.1 mol·L-1 H2SO4溶液,试管口出现红棕色气体, 说明溶液中NO3-被Fe2+还原为NO2 |
| C.将某气体通入品红溶液中,品红褪色,说明该气体一定是SO2 |
| D.向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀生成,说明淀粉没有水解生成葡萄糖 |
| A.+4 | B.+3 | C.+2 | D.+1 |
【知识点】 基于氧化还原反应守恒规律的计算解读
| A.将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀 |
| B.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 |
| C.向AlCl3溶液中滴加氨水,产生白色沉淀;再加入NaHSO4溶液,沉淀消失 |
| D.纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量CuSO4固体,速率不改变 |
【知识点】 原电池原理的综合应用解读
| A.漂白粉溶液在空气中失效: ClO-+CO2+H2O=HClO+HCO3- |
| B.NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O =Al(OH)3↓+HCO3- |
C.用浓盐酸与MnO2反应制少量氯气:MnO2+2H++2Cl-  Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| D.强碱溶液中NaClO与Fe(OH)3制Na2FeO4:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ |
【知识点】 离子反应的发生及书写
| A.Na2O,NaOH,Na2CO3,NaCl,Na2SO4,Na2O2都属于钠的含氧化合物 |
| B.简单非金属阴离子只有还原性,而金属阳离子不一定只有氧化性 |
| C.一种元素可能有多种氧化物,但同种化合价只对应有一种氧化物 |
| D.物质发生化学变化一定有化学键断裂与生成,发生物理变化一定没有化学键断裂或生成 |
【知识点】 钠及其化合物

| A.CHCl3分子的空间构型为正四面体 |
| B.COCl2分子中中心C原子采用sp2杂化 |
| C.COCl2分子中所有原子的最外层电子都满足8电子稳定结构 |
| D.使用前可用硝酸银稀溶液检验氯仿是否变质 |
| A.2 | B.4 | C.6 | D.8 |
【知识点】 氧化还原反应方程式的配平解读
| A.苯酚溶液显弱酸性 |
| B.苯酚和乙醇中,分别加入金属钠,苯酚反应剧烈 |
| C.苯酚比苯容易发生溴代反应 |
| D.苯酚能与氢氧化钠溶液反应,而苯甲醇不能 |
【知识点】 酚类

① 取代反应 ② 加成反应 ③ 消去反应 ④ 酯化反应 ⑤ 水解反应 ⑥ 氧化反应⑦中和反应
| A.①②③④⑤⑥⑦ | B.②③④⑤⑥ | C.②③④⑤⑥⑦ | D.①②③⑤⑥ |
【知识点】 有机反应类型
| A.反应中每生成l mol N2O,转移4mol电子 |
| B.N2O只有氧化性,无还原性 |
| C.N2O和CO2互为等电子体 |
| D.NO2属于酸性氧化物 |
【知识点】 氧化还原反应
A.氯气:K+、Na+、 、 、 |
B.氨气:K+、Na+、 、 、 |
C.二氧化硫:Na+、 、 、 、C1- 、C1- |
D.乙烯:H+、K+、 、 、 |
【知识点】 离子共存
| A.HNO3 | B.KOH | C.BaCl2 | D.NaClO |
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | Na2S有强还原性 | 用于除去废水中的Cu2+和Hg2+ |
| B | CaCO3是难溶物 | CaCl2溶液中通入CO2产生白色沉淀 |
| C | 浓H2SO4有强氧化性 | 浓H2SO4可用于干燥SO2 |
| D | Zn具有还原性和导电性 | 可用作锌锰干电池的负极材料 |
| A.A | B.B | C.C | D.D |
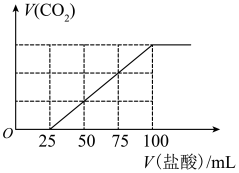
| A.原NaOH溶液的浓度为0.1mol·L-1 |
| B.通入CO2的体积为448mL(标准状况) |
| C.所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3 |
| D.所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3)=2∶1 |
二、填空题 添加题型下试题
①
②
③
(2)含硫化合物的种类很多,常见的有:SO2、Na2SO4、H2SO4、CuSO4等。
① 向含FeCl3和BaCl2的酸性溶液中通入SO2,有白色沉淀生成,此沉淀是
② 我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来减少SO2的污染,写出该反应的化学方程式
③ Na2SO3和KIO3在酸性溶液中发生的反应叫碘酸盐型“碘钟”反应,常用淀粉作指示剂,写出KIO3过量时该氧化还原反应的离子方程式
(3) 实验室用固体烧碱配制500 mL 0.1 mol•L―1的NaOH溶液。
① 需称量
② 配制过程中,不需要使用的仪器是(填写代号)
A 烧杯 B 漏斗
C 1000 mL容量瓶 D 托盘天平
E 药匙 F 500 mL容量瓶 G 胶头滴管
③ 除上述可使用的仪器,还缺少的仪器是
【知识点】 离子反应的发生及书写 二氧化硫的弱氧化性解读
HCO3-、NO3-。已知该溶液可与Al2O3反应,则:
① 若溶液与Al2O3反应,有Al3+生成,则溶液一定有
② 若溶液与 Al2O3反应,有AlO2-生成,则溶液一定有
(2)有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,
用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E产生沉淀,B与D、B与E产生沉淀,C与E、D与E产生气体,而C与D无反应现象。
由此,可判定各试剂瓶中所盛试剂为:
A
三、解答题 添加题型下试题
Ⅰ.查阅资料
K3[Fe(C2O4)3]·3H2O是翠绿色晶体,易溶于水,难溶于乙醇,具有光敏性,光照分解。
110℃失去结晶水,230℃时分解。K3[Fe(C2O4)3]·3H2O的摩尔质量是491g/moL
Ⅱ.制备产品
实验步骤如下:
① 取27.8gFeSO4·7H2O和K2C2O4反应生成草酸亚铁
② 将草酸亚铁(FeC2O4)和适量K2C2O4的混合溶液置于40℃的恒温水浴中,逐滴加入 6% H2O2,边加边搅拌,使Fe2+充分被氧化。反应体系中生成K3[Fe(C2O4)3]的同时还有部分Fe(OH)3沉淀
③ 向②所得浊液中加入1mol/LH2C2O4溶液,使溶液变为翠绿色
④ 加热浓缩,冷却结晶,过滤,洗涤,干燥,称量产品的质量为ag
请回答下列问题:
(1)第②步需要控制水浴40℃,温度不能太高的主要目的:
(2)第②步中,为检验Fe2+是否已完全被氧化,可选用
| A.NaOH溶液 | B.K3Fe(CN)6溶液 | C.苯酚溶液 | D.KSCN溶液 |
(4)步骤④中的实验操作需要下列仪器中的
①酒精灯 ②燃烧匙 ③烧杯 ④广口瓶 ⑤研钵 ⑥玻璃棒
(5)有同学为提高产率,避免第④步加热浓缩过程中K3[Fe(C2O4)3]的少量分解,依据查阅的资料提出新的结晶方案:将步骤③得到的溶液中加入
【知识点】 化学实验基础
四、填空题 添加题型下试题
L位于周期表第四周期、第12纵行且是六种元素中原子序数最大的。R是由M、L形成的化合物,其晶胞结构如图所示,

请回答下列问题:
(1)E元素的电负性
(2)G的第一电离能比它同周期前一族相邻元素的第一电离能
(3)M2E2广泛用于橡胶工业,在该化合物分子中,所有原子最外层均满足8电子稳定结构。则在M2E2分子中M原子的杂化类型是
(4)L的外围电子排布式为
(5)R的化学式为
已知R晶体的密度为ρ g.cm-3,则该晶胞的边长a
【知识点】 物质结构与性质
五、解答题 添加题型下试题

BAD的合成路线如下:
已知:G不能发生银镜反应,B遇FeCl3溶液显紫色,C到D的过程为引入羧基(—COOH)的反应。

试回答下列问题:
(1)写出结构简式:Y
(2)上述属于取代反应的有
(3)1molBAD最多可与含
(4)E有多种同分异构体,判断符合下列要求的同分异构体数目为
①能发生银镜反应 ②遇FeCl3溶液显紫色 ③核磁共振氢谱图中有四个吸收峰
(5)写出反应④方程式
【知识点】 同分异构体的数目的确定解读 有机物的推断
试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.64 | 化石能源 | |
| 2 | 0.85 | 离子反应的发生及书写 | |
| 3 | 0.85 | 离子反应 | |
| 4 | 0.64 | 化学计量 | |
| 5 | 0.64 | 物质的分类 | |
| 6 | 0.64 | 氮族元素及其化合物 氧族元素及其化合物 烃的衍生物 | |
| 7 | 0.65 | 基于氧化还原反应守恒规律的计算 | |
| 8 | 0.65 | 原电池原理的综合应用 | |
| 9 | 0.64 | 离子反应的发生及书写 | |
| 10 | 0.4 | 氧化还原反应的应用 氧化还原反应的规律 | |
| 11 | 0.64 | 钠及其化合物 | |
| 12 | 0.85 | 核磁共振氢谱 | |
| 13 | 0.65 | 共价键对分子构型、性质的影响 利用杂化轨道理论判断化学键杂化类型 | |
| 14 | 0.65 | 氧化还原反应方程式的配平 | |
| 15 | 0.64 | 酚类 | |
| 16 | 0.85 | 有机反应类型 | |
| 17 | 0.64 | 氧化还原反应 | |
| 18 | 0.85 | 烃的衍生物 有机物的结构特点 | |
| 19 | 0.64 | 离子共存 | |
| 20 | 0.65 | 碳酸钠 偏铝酸钠与盐酸的反应 无机物的检验 物质检验和鉴别的基本方法选择及应用 | |
| 21 | 0.65 | 浓硫酸的吸水性 沉淀的溶解与生成 原电池的结构 化学实验方案的设计与评价 | |
| 22 | 0.65 | 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 二、填空题 | |||
| 23 | 0.65 | 离子反应的发生及书写 二氧化硫的弱氧化性 | |
| 24 | 0.4 | 离子反应 无机综合推断 | |
| 26 | 0.15 | 物质结构与性质 | |
| 三、解答题 | |||
| 25 | 0.4 | 化学实验基础 | 实验探究题 |
| 27 | 0.65 | 同分异构体的数目的确定 有机物的推断 | 有机推断题 |

 在酸性溶液中易被还原成
在酸性溶液中易被还原成 ,且还原性:
,且还原性: 。下列反应在水溶液中不可能发生的是
。下列反应在水溶液中不可能发生的是