福建省三明市尤溪县第一中学2018-2019学年高一第二学期入学考试化学试题
福建
高一
开学考试
2019-03-13
331次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
| A.二氧化碳气体 | B.硫酸溶液 | C.蔗糖溶液 | D.固体氯化钠 |
【知识点】 电解质
| A.AlCl3 | B.FeCl3 | C.FeCl2 | D.CuCl2 |
【知识点】 氯气与金属单质的反应解读 铁与非金属单质反应解读 铜与非金属单质反应
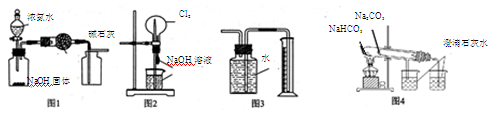
| A.图1装置可制取、收集干燥纯净的NH3 |
| B.图2装置可以完成“喷泉”实验 |
| C.图3装置可测量Cu 与浓硝酸反应产生气体的体积 |
| D.图4装置可用比较NaHCO3和Na2CO3的热稳定性 |
【知识点】 仪器使用与实验安全
| A.钠与硫酸铜溶液反应会置换出红色的铜 |
| B.常温下干燥氯气与铁不反应,可以用钢瓶储存液氯 |
| C.CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| D.C、N、S三种单质直接与O2反应都能生成两种氧化物 |
【知识点】 氯气的化学性质 氯气与金属单质的反应解读 硫酸
| A.Na+、Ba2+、Cl-、SO42- | B.Ca2+、HCO3-、C1-、K+ |
| C.MnO4-、K+、I-、H+ | D.H+、Cl-、Na+、CO32- |
【知识点】 离子共存
| A.1∶5 | B.1∶4 | C.5∶1 | D.4∶1 |
【知识点】 氧化还原反应有关计算 氧化还原反应的规律解读
| A.铁片投入稀硫酸中2Fe+6H+ = 2Fe 3++3H2↑ |
| B.食醋与氨水反应:NH3·H2O+H+= NH4++H2O |
| C.过量铁粉与稀硝酸反应:3Fe+8H++2NO3-= 3Fe 2++2NO↑+4H2O |
| D.向Ba(OH)2溶液滴加NaHSO4溶液至Ba2+恰好沉淀:Ba2++2H++2OH-+SO42- = BaSO4↓+2H2O |
【知识点】 离子方程式的正误判断解读

| A.①>② | B.①<② | C.①=② | D.不能确定 |
| A.A→B | B.B→C | C.C→D | D.D→E |
| A.1 mol Cl2与足量的铁反应转移的电子数是2 NA |
| B.常温常压下22.4 L HCl气体含有的分子数是NA |
| C.0.1 mol/L CuCl2溶液中Cl-数目是0.2 NA |
| D.7.8克过氧化钠投入足量的水中,转移电子数为0.2 NA |
| A.Na2CO3 | B.NaOH、Na2CO3 | C.Na2O2、 Na2CO3 | D.Na2O2、 NaOH 、Na2CO3 |
①过滤,②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量的BaCl2溶液,正确的操作顺序是
| A.①④⑤②③ | B.④①②⑤③ | C.②⑤④①③ | D.④⑤②①③ |
【知识点】 物质分离、提纯的常见化学方法解读
| A.KNO3是还原剂,其中氮元素被氧化 |
| B.生成物中的N2是氧化产物,K2O是还原产物 |
| C.每转移1 mol电子,可生成标准状况下N2的体积为35.84 L |
| D.若有65 g NaN3参加反应,则被氧化的N的物质的量为3.2 mol |
【知识点】 氧化还原反应有关计算
 全部转化成Cr3+,则K2Cr2O7溶液的物质的量浓度是
全部转化成Cr3+,则K2Cr2O7溶液的物质的量浓度是| A.0.05mol/L | B.0.1mol/L | C.0.2mol/L | D.0.3mol/L |
【知识点】 氧化还原反应有关计算
二、填空题 添加题型下试题
(1)金属镁在CO2中燃烧
(2)加热碳酸氢钠固体
(3)二氧化硫与氢氧化钠溶液反应
(4)KCl溶液与AgNO3溶液反应
(5)铜与稀硝酸反应制取NO气体
(1)实验室可用硫化亚铁固体与稀硫酸反应来制备H2S气体。
①该反应的化学方程式为
②多余的H2S气体可用
(2)用30% FeCl3溶液作吸收液也能吸收H2S气体,反应方程式为:2FeCl3+H2S = S↓+2FeCl2+2HCl,废吸收液经电解可循环使用。
①该反应中H2S显
a、不稳定性 b、弱酸性 c、氧化性 d、还原性
②检验废吸收液中是否含有Fe3+的适宜试剂是
③强酸性的废吸收液电解可生成FeCl3和一种分子量最小的气体,则化学方程式为
(3)已知:H2S在高温下分解生成硫蒸气和H2。现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示。
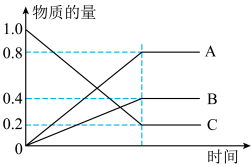
①表示H2的曲线是
②生成硫蒸气的分子式为
三、解答题 添加题型下试题
回答下列问题。
(1)实验室从含碘废液(除水外含CCl4、I2、I-等)中回收碘,其实验流程如下。

回答下列问题:
①物质X的名称为
②操作Ⅰ选用的装置为
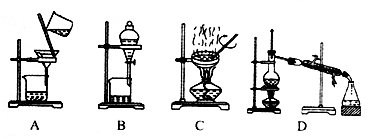
③含碘废液中加入稍过量的Na2SO3溶液将I2还原为I-,反应的离子方程式为
④氧化剂Y可用Cl2,也可以用H2O2。将同物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为
(2)某研究小组查阅资料知:氧化性的强弱顺序为:Cl2>IO3->I2。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。
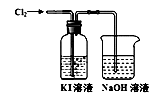
①NaOH溶液的作用是
②溶液由黄色最后变为无色所发生反应的离子方程式为
【知识点】 氧化还原反应的应用 氧化还原反应有关计算 物质分离、提纯综合应用解读
四、计算题 添加题型下试题
 MnCl2+Cl2↑+2H2O。取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O。取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。请回答下列问题:
(1)参加反应的二氧化锰的质量为
(2)反应中被氧化的HCl的物质的量为
(3)实验室备用的浓盐酸质量分数为36.5%,密度为1.19g·cm-3,请计算出该浓盐酸的物质的量浓度
试卷分析
试卷题型(共 22题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 电解质 | |
| 2 | 0.85 | 分类方法的应用 无机物质的分类 漂白粉和漂粉精 | |
| 3 | 0.64 | 化学计量 阿伏加德罗定律 | |
| 4 | 0.65 | 硝酸的不稳定性 | |
| 5 | 0.65 | 几组常见同素异形体 | |
| 6 | 0.85 | 氯气与金属单质的反应 铁与非金属单质反应 铜与非金属单质反应 | |
| 7 | 0.85 | 仪器使用与实验安全 | |
| 8 | 0.65 | 氯气的化学性质 氯气与金属单质的反应 硫酸 | |
| 9 | 0.64 | 离子共存 | |
| 10 | 0.65 | 氧化还原反应有关计算 氧化还原反应的规律 | |
| 11 | 0.85 | 离子方程式的正误判断 | |
| 12 | 0.65 | 阿伏加德罗定律 物质的量浓度的计算 氨的喷泉实验 氮氧化物溶解于水的相关计算 | |
| 13 | 0.94 | 物质的转化 次氯酸及其性质 氯气的实验室制法 氯气与碱溶液反应 | |
| 14 | 0.65 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 | |
| 15 | 0.85 | 过氧化钠的相关计算 碳酸氢钠的不稳定性 | |
| 16 | 0.65 | 物质分离、提纯的常见化学方法 | |
| 17 | 0.4 | 氧化还原反应有关计算 | |
| 18 | 0.4 | 氧化还原反应有关计算 | |
| 二、填空题 | |||
| 19 | 0.65 | 离子反应的发生及书写 硝酸的强氧化性 碳酸氢钠的不稳定性 镁的结构与化学性质 | |
| 20 | 0.65 | 物质的量有关计算 氧化还原反应方程式的配平 硫化氢 铁盐的检验 | |
| 三、解答题 | |||
| 21 | 0.65 | 氧化还原反应的应用 氧化还原反应有关计算 物质分离、提纯综合应用 | 实验探究题 |
| 四、计算题 | |||
| 22 | 0.85 | 化学计量 卤素及其化合物 | |



