甘肃省甘谷第一中学2020届高三上学期第一次检测化学试题
甘肃
高三
阶段练习
2019-09-12
374次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、化学反应原理、有机化学基础
一、单选题 添加题型下试题
| A.生活污水进行脱氮、脱磷处理可以减少水体富营养化 |
| B.食品袋中装有硅胶的小纸包的作用是防止食品受潮 |
| C.爆竹燃放过程中,硫燃烧直接生成三氧化硫 |
| D.碳酸钡不可用于胃肠X射线造影检查 |
【知识点】 硫 硅酸与硅酸盐 化学科学对人类文明发展的意义解读 水体污染来源及保护措施解读
| A.从组成元素上可以区别纯净物和混合物 |
| B.往Fe(OH)3胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解 |
| C.通过化学变化可以实现16O与18O间的相互转化 |
| D.鸡蛋清溶液中加入饱和(NH4)2SO4溶液生成白色沉淀,属于化学变化 |
| A.体积之比为13∶13∶14 | B.密度之比为14∶14∶13 |
| C.质量之比为1∶1∶1 | D.原子数之比为1∶1∶1 |
【知识点】 阿伏加德罗定律及其推论解读 物质的量有关计算
| A.标准状况下,22.4LCl2通入足量的NaOH溶液充分反应,有NA个电子转移 |
| B.常温下,pH=12的氢氧化钠溶液中OH-数目为0.01NA |
| C.lmolSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |
| D.84gNaHCO3固体含有CO32-离子的数目为NA |
| A.物质的量浓度 | B.溶质的物质的量 |
| C.溶液的体积 | D.质量分数 |
 固体既能溶于KOH溶液得到
固体既能溶于KOH溶液得到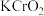 溶液,又能溶于硫酸得到
溶液,又能溶于硫酸得到 溶液;
溶液; 将
将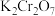 溶液滴加到淀粉和KI的混合溶液中,溶液变蓝;
溶液滴加到淀粉和KI的混合溶液中,溶液变蓝; 向
向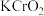 溶液中滴加
溶液中滴加 溶液,再酸化,可得
溶液,再酸化,可得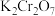 溶液.下列判断不正确的是
溶液.下列判断不正确的是A.化合物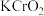 中Cr元素为 中Cr元素为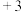 价 价 | B.实验 证明 证明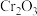 是两性氧化物 是两性氧化物 |
C.实验 证明氧化性: 证明氧化性: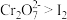 | D.实验 证明 证明 既有氧化性又有还原性 既有氧化性又有还原性 |
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与稀硝酸反应:2Fe3O4+18H+===6Fe3++H2↑+8H2O | 正确 |
| B | 向碳酸镁中加入稀盐酸:CO32-+2H+=CO2↑+H2O | 错误,碳酸镁不应写成离子形式 |
| C | 向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-===BaSO4↓ | 正确 |
| D | FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2===2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为1∶2 |
| A.A | B.B | C.C | D.D |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
①“84”消毒液的水溶液中:Fe2+、Cl-、Ca2+、Na+ ②加入KSCN显红色的溶液:K+、NH4+、Cl-、S2-③能够与金属Cu常温下反应放出气体的溶液:Fe3+、Al3+、SO42-、K+④pH=2的溶液中:NH4+、Na+、Cl-、Cu2+⑤无色溶液中:K+、CH3COO-、HCO3-、MnO4-
| A.②③ | B.①③ | C.①⑤ | D.③④ |
【知识点】 离子共存 限定条件下的离子共存解读

| A.反应中转移电子的物质的量是0.21 mol |
| B.ClO3-的生成是由于温度升高引起的 |
| C.苛性钾溶液中KOH的质量是16.8 g |
| D.氯气被还原成0.06 mol ClO-和0.03 mol ClO3- |
【知识点】 氧化还原反应有关计算
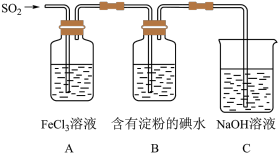
| A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色 |
| B.装置C的作用是吸收SO2尾气,防止污染空气 |
| C.为了验证A中发生了氧化还原反应,加入酸性KMnO4溶液,紫色褪去 |
| D.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀 |
【知识点】 二氧化硫与其他强氧化剂的反应解读 物质性质的探究解读
| A.电解质溶液的浓度越大,其导电能力一定越强 |
| B.强酸和强碱一定是强电解质,不管其水溶液浓度的大小,都能完全电离 |
| C.强极性共价化合物不一定都是强电解质 |
| D.多元酸、多元碱的导电性一定比一元酸、一元碱的导电能力强 |
| 选项 | 待提纯物质 | 杂质 | 除杂试剂及主要操作方法 |
| A | 乙烷 | 乙烯 | 酸性KMnO4溶液,洗气 |
| B | MgCl2溶液 | FeCl3 | MgO,过滤 |
| C | HCl气体 | Cl2 | 饱和食盐水,洗气 |
| D | 乙醇 | 水 | 生石灰,过滤 |
| A.A | B.B | C.C | D.D |
【知识点】 有机物分离提纯的几种常见操作 物质的分离、提纯
| A.2-甲基丁烷也称为异丁烷 |
| B.由乙烯生成乙醇属于加成反应 |
| C.C4H9Cl有3种同分异构体 |
| D.油脂和蛋白质都属于高分子化合物 |
【知识点】 烷烃的命名 同分异构体的数目的确定解读 油脂 蛋白质
| 选项 | 实验操作和现象 | 结论 |
| A | 常温下,0.1 mol/LCH3COOH溶液的pH大于1 | 乙酸是弱酸 |
| B | 向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀 | 该溶液中一定有SO42- |
| C | 向饱和NaHCO3溶液中加入足量氯水,有无色气体产生 | 氯水中含HClO |
| D | Cl2、SO2均能使品红溶液褪色 | 两者均有氧化性 |
| A.A | B.B | C.C | D.D |
| A.原混合物中n(Fe)∶n(Fe2O3)=2∶1 |
| B.向溶液中滴入无色的KSCN溶液,显红色 |
| C.无法计算出原混合物的质量 |
| D.此时溶液中Fe2+和Fe3+的物质的量之比为3∶1 |
【知识点】 铁及铁的氧化物混合物反应的相关计算解读
二、解答题 添加题型下试题
(1)氧化还原法消除NOx的转化如下:

①反应I为NO +O3===NO2+O2,生成标准状况下11.2 L O2时,转移电子的物质的量是
②反应Ⅱ中,当n( NO2):n[CO(NH2)2]=3:2时,氧化产物与还原产物的质量比为
(2)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。装置I中发生反应的离子方程式为

(3)装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-、NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式
(4)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得Ce4+再生,再生时生成的Ce4+在电解槽的
(5)取少量装置Ⅳ所得的产品溶于水,溶液中离子浓度由大到小的顺序为

试回答下列问题:
(1)滤液X中含有的金属阳离子是
(2)步骤Ⅲ中可选用
A.稀硝酸 B.氨水
C.氢氧化钠溶液 D.高锰酸钾溶液
(3)步骤Ⅳ中,FeCO3沉淀完全后,溶液中含有少量Fe2+,检验Fe2+的方法是
(4)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是
(5)在空气中煅烧FeCO3生成产品氧化铁的化学方程式为
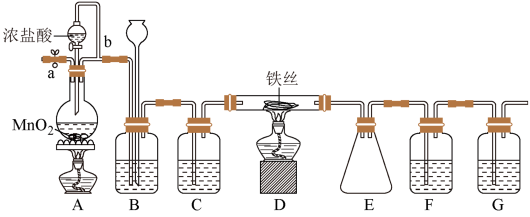
(1)装置A中反应的离子方程式为
(2)装置C中所加的试剂为
(3)导管b的作用为
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,是因为
(5)为检验所得产品为FeCl3,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入
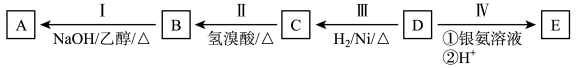
请回答:
(1)D的分子式为
(2)B中所含官能团的名称为
(3)Ⅲ的反应类型为
a. 还原反应 b.加成反应 c.氧化反应 d.消去反应
(4)写出下列反应的化学方程式:
I:
C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为
(5)A的同分异构体中有一对互为顺反异构,且结构中有2个-CH3,它们的结构简式为
(6)E有多种同分异构体,其中含有
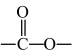 结构的有
结构的有【知识点】 有机物的推断 多官能团有机物的结构与性质解读 有机推断综合考查解读
三、填空题 添加题型下试题
(1)Pb与C同主族,化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物,已知PbO2具有强氧化性,与浓盐酸共热可生成一种黄绿色气体和PbCl2 。试写出Pb3O4与浓盐酸反应的化学方程式:
(2)过氧化钠可用于实验室制O2,其化学方程式为
(3)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
(4)Fe的一种含氧酸根FeO42-- 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
(5)向菱镁矿(主要成分为MgCO3,含少量FeCO3)中,首先加入稀硫酸,过滤后,再加入H2O2。写出加入H2O2氧化时发生反应的化学方程式:
试卷分析
试卷题型(共 20题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 硫 硅酸与硅酸盐 化学科学对人类文明发展的意义 水体污染来源及保护措施 | |
| 2 | 0.85 | 无机物质的分类 胶体的性质和应用 物理变化与化学变化 | |
| 3 | 0.65 | 阿伏加德罗定律及其推论 物质的量有关计算 | |
| 4 | 0.65 | 阿伏加德罗常数 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 | |
| 5 | 0.85 | 物质的量有关计算 物质的量浓度的计算 | |
| 6 | 0.85 | 氧化还原反应基本概念 常见氧化剂与还原剂 氧化性、还原性强弱的比较 氧化还原反应的应用 | |
| 7 | 0.65 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 8 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 9 | 0.4 | 氧化还原反应有关计算 | |
| 10 | 0.65 | 二氧化硫与其他强氧化剂的反应 物质性质的探究 | |
| 11 | 0.65 | 物质水溶液的导电性 强电解质与弱电解质 | |
| 12 | 0.65 | 有机物分离提纯的几种常见操作 物质的分离、提纯 | |
| 13 | 0.94 | 烷烃的命名 同分异构体的数目的确定 油脂 蛋白质 | |
| 14 | 0.65 | 氯水的性质 二氧化硫 硫酸根离子的检验 强电解质和弱电解质的判断 | |
| 15 | 0.65 | 铁及铁的氧化物混合物反应的相关计算 | |
| 二、解答题 | |||
| 16 | 0.65 | 盐溶液中离子浓度大小的比较 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 17 | 0.65 | 有关铁及其化合物转化的流程题型 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 18 | 0.85 | 氯气的实验室制法 铁盐与亚铁盐鉴别试剂的选择 化学实验探究 物质制备的探究 | 实验探究题 |
| 19 | 0.65 | 有机物的推断 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |
| 三、填空题 | |||
| 20 | 0.65 | 离子方程式的书写 氧化还原反应的规律 酸碱中和滴定原理的应用 | |



