某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取漂白粉。据此回答下列问题:

(1)在 A 装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为:___________ ,若产生 0.3 mol Cl2,则消耗的 HCl 中起还原作用的物质的量是___________ ,反应中转移的电子数是___________ 。
(2)漂白粉将在 U 形管中产生,其化学方程式是___________ 。
(3)C 装置的作用是___________ 。

(1)在 A 装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为:
(2)漂白粉将在 U 形管中产生,其化学方程式是
(3)C 装置的作用是
更新时间:2021-03-25 13:52:08
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】高中化学课本必修一中出现的部分物质间的转化关系如下图所示(部分物质已省略。已知A→B是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完成下列填空。
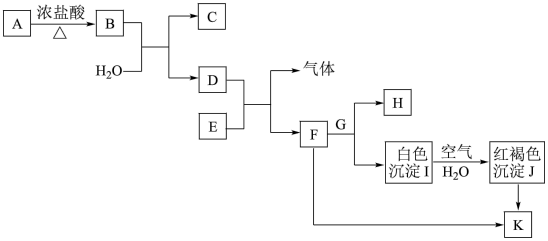
(1)E和H的化学式为:E_______ ;H_______ 。
(2)检验K溶液中阳离子的试剂是_______ 。在配制F溶液时,常向F溶液中加入少量E,其目的是_______ 。
(3)I转化为J的化学方程式为_______ 。
(4)K 饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
(5)当前,新冠病毒变异毒株奥密克戎来势汹汹,化学消毒剂在疫情防控中起着重要作用。
①目前,很多自来水厂用B的水溶液来杀菌、消毒,其消毒原理为_______ (用离子方程式表示)。
②将B通入G溶液中可得到一种漂白液,能杀菌、消毒,若用该漂白液漂白衣物,请写出一种增强漂白性的方法_______ 。
(6)ClO2不但能消毒杀菌,还对污水中CN-有明显的去除效果,主要是ClO2将CN-氧化生成CO2和N2两种无毒气体,某污水中含CN-a mg/L。其氧化的离子方程式为_______ ,处理1000 L这种污水,至少需要ClO2_______ mol(用含a的代数式表示)

(1)E和H的化学式为:E
(2)检验K溶液中阳离子的试剂是
(3)I转化为J的化学方程式为
(4)K
 饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。A.胶体L的分散质粒子直径为 | B.胶体L比K的饱和溶液颜色深 |
| C.胶体L是均一的分散系 | D.胶体L具有丁达尔效应 |
①目前,很多自来水厂用B的水溶液来杀菌、消毒,其消毒原理为
②将B通入G溶液中可得到一种漂白液,能杀菌、消毒,若用该漂白液漂白衣物,请写出一种增强漂白性的方法
(6)ClO2不但能消毒杀菌,还对污水中CN-有明显的去除效果,主要是ClO2将CN-氧化生成CO2和N2两种无毒气体,某污水中含CN-a mg/L。其氧化的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图是某位同学设计的实验装置,制取 并以
并以 为原料制备无水
为原料制备无水 。
。
已知: 升华,无水
升华,无水 遇水强烈反应。
遇水强烈反应。

(1)写出仪器A的名称:___________ 。
(2)a为氯气发生装置,写出反应的化学方程式:___________ 。
(3)实验开始先点燃___________ (“a”或“d”)处的酒精灯。
(4)装置b的作用是___________ ;c中试剂名称___________ ;装置f中反应的化学方程式:___________ 。
(5)某同学设计的上述实验装置示意图有一处不合理,会影响实验,请提出改进方案:___________ 。
 并以
并以 为原料制备无水
为原料制备无水 。
。已知:
 升华,无水
升华,无水 遇水强烈反应。
遇水强烈反应。
(1)写出仪器A的名称:
(2)a为氯气发生装置,写出反应的化学方程式:
(3)实验开始先点燃
(4)装置b的作用是
(5)某同学设计的上述实验装置示意图有一处不合理,会影响实验,请提出改进方案:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
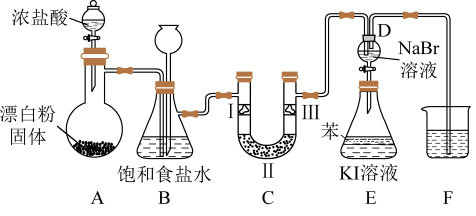
(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是___________ ,请写出该反应相应的化学方程式___________ 。
(2)装置B中饱和食盐水的作用是___________ ;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:___________ 。
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是___________ ,该现象___________ (填“能”或“不能")说明溴单质的氧化性强于碘,原因是___________ 。
(4)若向100mLFeBr2若液中通入2.24LCl2(标准状况下),若溶液中有 的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为___________ 。

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是
(2)装置B中饱和食盐水的作用是
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是
(4)若向100mLFeBr2若液中通入2.24LCl2(标准状况下),若溶液中有
 的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某实验小组用图1装置电解饱和食盐水制取氯气并进行实验探究,回答下列问题:

(1)电解饱和食盐水的化学方程式为:_______ 。
(2)检验氢氧化钠溶液中是否含有NaCl的实验操作是_______ 。
(3)利用图2装置验证氯气与烧碱溶液的反应。将A与B连接,打开止水夹,用注射器注入过量NaOH浓溶液,观察到的现象有_______ 。


(1)电解饱和食盐水的化学方程式为:
(2)检验氢氧化钠溶液中是否含有NaCl的实验操作是
(3)利用图2装置验证氯气与烧碱溶液的反应。将A与B连接,打开止水夹,用注射器注入过量NaOH浓溶液,观察到的现象有

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组利用如图装置制取氨气并探究氨气的有关性质。

(1).装置A中烧瓶内试剂可选用___________ (填序号)
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱固体
(2).氨气是一种极易溶于水的有害气体,为了防止多余的氨气扩散到空气中,则需要在K2的导管末端连接下表装置中的___________ (填序号)装置,如何检验收集的一瓶气体是氨气的实验操作___________ ,当装置D中集满氨气后,关闭K1、K2,打开K3引发喷泉的实验操作是___________ 。
(3).若探究氨气的还原性,需要打开K1、K3,K2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成的气体必须通过盛有___________ 试剂的洗气瓶。
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为___________ 。
③从K3处导管逸出的气体中含有量Cl2,则C 装置中应盛放___________ (填化学式)溶液,反应的离子方程式为:___________ 。

(1).装置A中烧瓶内试剂可选用
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱固体
(2).氨气是一种极易溶于水的有害气体,为了防止多余的氨气扩散到空气中,则需要在K2的导管末端连接下表装置中的
| 备选装置(水中含酚酞溶液) | ||
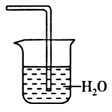 | 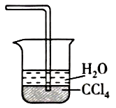 | 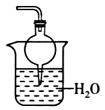 |
| I | Ⅱ | Ⅲ |
①用二氧化锰与浓盐酸制取氯气,生成的气体必须通过盛有
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为
③从K3处导管逸出的气体中含有量Cl2,则C 装置中应盛放
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
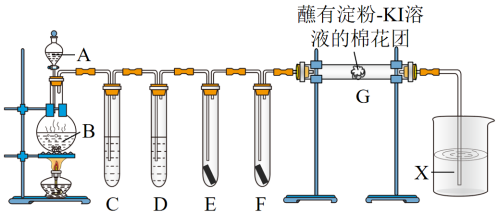
【推荐3】实验室用如下装置制取干燥纯净的氯气,并用氯气进行实验。
(1)装置连接完成后必须进行的操作是_____________________ 。
(2)实验室制氯气的反应方程式为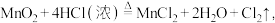 其中参加反应的还原剂与氧化剂的物质的量之比为
其中参加反应的还原剂与氧化剂的物质的量之比为______________________ 。
(3)E中为红色干布条,F 中为红色湿布条,对比 E 和F 中现象的差异可得出的结论__________ 。
(4)试管 D 中试剂的作用是______________________ 。
(5)装置G 处的现象是______________________ 。
(6)图中 X 可能为 。
(1)装置连接完成后必须进行的操作是
(2)实验室制氯气的反应方程式为
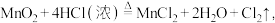 其中参加反应的还原剂与氧化剂的物质的量之比为
其中参加反应的还原剂与氧化剂的物质的量之比为(3)E中为红色干布条,F 中为红色湿布条,对比 E 和F 中现象的差异可得出的结论
(4)试管 D 中试剂的作用是
(5)装置G 处的现象是
(6)图中 X 可能为 。
| A.NaOH 溶液 | B.KOH 溶液 | C.饱和 NaCl溶液 | D.蒸馏水 |
您最近一年使用:0次



