某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并放出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知:Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如表所示:
(1)该同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理:___________ (填“合理”或“不合理”)。
(2)将铝与Fe2O3混合后放入漏斗中,然后引发铝热反应的实验操作是___________ 。
(3)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是___________ ,反应的离子方程式为___________ 。
(4)实验室溶解该熔融物,下列试剂中最好的是___________(填序号)。
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | —— |
(1)该同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理:
(2)将铝与Fe2O3混合后放入漏斗中,然后引发铝热反应的实验操作是
(3)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是
(4)实验室溶解该熔融物,下列试剂中最好的是___________(填序号)。
| A.浓硫酸 |
| B.稀硫酸 |
| C.稀硝酸 |
| D.氢氧化钠溶液 |
22-23高一上·全国·课时练习 查看更多[2]
更新时间:2022-09-06 21:46:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)为了防止氯化亚铁溶液氧化变质,常在其中加入____ ,反应的离子方程式是_____ ;
(2)除去铁粉中的铝粉,可用过量的_______ 溶液,然后过滤,反应化学方程式为_________ 。
(2)除去铁粉中的铝粉,可用过量的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液的化学方程式:__________________________ 。
(2)锌和氢氧化钠溶液反应后,溶液中锌元素的存在形式为_________ (用化学式表示)。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是_______________ 。
① 硫酸铝和氢氧化钠 ② 硫酸锌和氢氧化钠 ③硫酸铝和氨水 ④ 硫酸锌和氨水
(4)在火箭和导弹技术中,将铝粉与石墨、TiO2按一定比例混合均匀,涂在金属表面,在高温下煅烧,金属表面生成TiC和另一种耐高温的物质,写出该反应的化学方程式:__________ 。
(5)某混合物 ,含有
,含有 、
、 和
和 ,在一定条件下可实现如图所示的物质之间的变化:
,在一定条件下可实现如图所示的物质之间的变化:

据此回答下列问题:
①写出固体 的化学式:
的化学式:
__________ ;
②写出D与稀硫酸反应的化学方程式:___________________________________________ ;
写出反应①的离子方程式:_________________________________________ 。
(1)单质铝溶于氢氧化钠溶液的化学方程式:
(2)锌和氢氧化钠溶液反应后,溶液中锌元素的存在形式为
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是
① 硫酸铝和氢氧化钠 ② 硫酸锌和氢氧化钠 ③硫酸铝和氨水 ④ 硫酸锌和氨水
(4)在火箭和导弹技术中,将铝粉与石墨、TiO2按一定比例混合均匀,涂在金属表面,在高温下煅烧,金属表面生成TiC和另一种耐高温的物质,写出该反应的化学方程式:
(5)某混合物
 ,含有
,含有 、
、 和
和 ,在一定条件下可实现如图所示的物质之间的变化:
,在一定条件下可实现如图所示的物质之间的变化:
据此回答下列问题:
①写出固体
 的化学式:
的化学式:
②写出D与稀硫酸反应的化学方程式:
写出反应①的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】书写以下离子反应方程式(以下反应皆在溶液中进行)
(1)把食醋除水垢(CaCO3)中:_______
(2)铝与氢氧化钠反应:_______ ;
(3)铝盐和氨水反应制氢氧化铝:_______
(4)Na和水反应_______
(5)向氢氧化钠溶液通入足量二氧化碳气体_______
(6)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O_______
(1)把食醋除水垢(CaCO3)中:
(2)铝与氢氧化钠反应:
(3)铝盐和氨水反应制氢氧化铝:
(4)Na和水反应
(5)向氢氧化钠溶液通入足量二氧化碳气体
(6)MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图为铝热反应的实验装置,请回答下列问题:

(1)该实验装置中还缺___ ,在试剂使用正确且符合要求的情况下引发铝热反应的操作为___ ,写出铝热反应的化学方程式:___ 。
(2)若将氧化铁换成氧化镁,该反应___ (填“能”或“不能”)发生,理由是___ 。
(3)若将所得产品置于足量的NaOH溶液中,可能看到的现象是__ ,写出铝热反应的一种主要用途:___ 。
(4)假设铝足量且反应充分,设计一种实验方案,证明本实验中有单质铁生成:___ 。

(1)该实验装置中还缺
(2)若将氧化铁换成氧化镁,该反应
(3)若将所得产品置于足量的NaOH溶液中,可能看到的现象是
(4)假设铝足量且反应充分,设计一种实验方案,证明本实验中有单质铁生成:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属的用途和性质紧密相关。
(1)已知金属的物理性质有①导电性、②导热性、③延展性。请填表。
(2)铝是一种活泼金属,具有较强的还原性。
①金属铝在高温下与三氧化二铁反应,2Al+Fe2O3 Al2O3+2Fe,称为铝热反应。该反应中______是氧化剂,______是还原剂。
Al2O3+2Fe,称为铝热反应。该反应中______是氧化剂,______是还原剂。
②铝热反应不仅被用作焊接钢轨,还常用于冶炼熔点较高的金属,如钒、镉、锰等。用铝热反应原理从__________________。
(1)已知金属的物理性质有①导电性、②导热性、③延展性。请填表。
| 金属的用途 | 对应的金属物理性质 |
| 金可制成比纸还薄的金箔 | |
| 用铁、铝等做炊具 | |
| 用铜制作印刷电路 |
(2)铝是一种活泼金属,具有较强的还原性。
①金属铝在高温下与三氧化二铁反应,2Al+Fe2O3
 Al2O3+2Fe,称为铝热反应。该反应中______是氧化剂,______是还原剂。
Al2O3+2Fe,称为铝热反应。该反应中______是氧化剂,______是还原剂。②铝热反应不仅被用作焊接钢轨,还常用于冶炼熔点较高的金属,如钒、镉、锰等。用铝热反应原理从__________________。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铝(熔点660℃)是一种应用广泛的金属,工业上用 (熔点2045℃)和冰晶石(
(熔点2045℃)和冰晶石(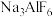 )混合熔融后电解制得。请回答下列问题:
)混合熔融后电解制得。请回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,其原因是__________ ,冶金工业上常用金属铝作还原剂冶炼钒、铬、锰等金属,请写出铝与V2O5在高温下反应的化学方程式:___________ 。
(2)将 液和
液和 溶液混合制取
溶液混合制取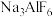 。该实验用于盛装NaF溶液的试剂瓶
。该实验用于盛装NaF溶液的试剂瓶_________ (填“能”或“不能”)用玻璃瓶,原因是_______ 。
(3)下列关于铝元素的叙述不正确的是__________ (填序号)。
A.铝是人类最早使用的金属
B.镁铝合金既可完全溶于过量的盐酸,又可完全溶于过量的NaOH溶液
C.氢氧化铝是一种两性氢氧化物,既能溶于盐酸又能溶于NaOH溶液
D.铝是人体必需的微量元素之一,因此在生活中人们应尽量使用铝制炊具和餐具更有利于身体健康
(4)某工厂排放出有毒物质NOCl,它遇水就会生成 。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为
。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______ ,水源中的 对人类健康会产生危害,为了降低水源中
对人类健康会产生危害,为了降低水源中 的浓度,有研究人员建议在碱性条件下用铝粉将
的浓度,有研究人员建议在碱性条件下用铝粉将 还原为N2,此时铝主要以
还原为N2,此时铝主要以 的形式存在于溶液中,请写出该反应的离子方程式:
的形式存在于溶液中,请写出该反应的离子方程式:_______ ,当该反应转移10mol电子时,产生的 在标准状况下的体积约为
在标准状况下的体积约为______ (写出计算过程)。
 (熔点2045℃)和冰晶石(
(熔点2045℃)和冰晶石(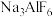 )混合熔融后电解制得。请回答下列问题:
)混合熔融后电解制得。请回答下列问题:(1)铝属于活泼金属却能在空气中稳定存在,其原因是
(2)将
 液和
液和 溶液混合制取
溶液混合制取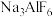 。该实验用于盛装NaF溶液的试剂瓶
。该实验用于盛装NaF溶液的试剂瓶(3)下列关于铝元素的叙述不正确的是
A.铝是人类最早使用的金属
B.镁铝合金既可完全溶于过量的盐酸,又可完全溶于过量的NaOH溶液
C.氢氧化铝是一种两性氢氧化物,既能溶于盐酸又能溶于NaOH溶液
D.铝是人体必需的微量元素之一,因此在生活中人们应尽量使用铝制炊具和餐具更有利于身体健康
(4)某工厂排放出有毒物质NOCl,它遇水就会生成
 。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为
。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为 对人类健康会产生危害,为了降低水源中
对人类健康会产生危害,为了降低水源中 的浓度,有研究人员建议在碱性条件下用铝粉将
的浓度,有研究人员建议在碱性条件下用铝粉将 还原为N2,此时铝主要以
还原为N2,此时铝主要以 的形式存在于溶液中,请写出该反应的离子方程式:
的形式存在于溶液中,请写出该反应的离子方程式: 在标准状况下的体积约为
在标准状况下的体积约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)用碳酸锂和_______ 反应可制备氯化锂,工业上可由电解LiCl-KCl的熔融混合物生产金属锂,阴极上的电极反应式为___________________ 。
(2)不可使用二氧化碳灭火器扑灭因金属锂引起的火灾,其原因是____________________________ 。
(3)硬脂酸锂是锂肥皂的主要成分,可作为高温润滑油和油脂的稠化剂。鉴别硬脂酸锂与硬脂酸钠、硬脂酸钾可采用的实验方法是_________________________ 。
(4)LiPF6易溶于有机溶剂,常用作锂离子电池的电解质。LiPF6受热易分解,其热分解产物为PF5和__________ 。
(1)用碳酸锂和
(2)不可使用二氧化碳灭火器扑灭因金属锂引起的火灾,其原因是
(3)硬脂酸锂是锂肥皂的主要成分,可作为高温润滑油和油脂的稠化剂。鉴别硬脂酸锂与硬脂酸钠、硬脂酸钾可采用的实验方法是
(4)LiPF6易溶于有机溶剂,常用作锂离子电池的电解质。LiPF6受热易分解,其热分解产物为PF5和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某小组为了探究硫酸的性质,设计如下实验:
回答下列问题:
(1)实验①没有明显现象的原因是___________ ;改变一个条件,为使实验①中的反应持续发生,改变条件是___________ 。
(2)为了引发实验②中的反应,宜采取的措施是___________ ;实验后,观察产物水溶液的颜色,其操作方法是___________ 。
(3)实验④产生的气体是___________ (填化学式),比较实验③和④可知,从氧化还原角度分析,H+的作用是___________ ;写出该反应的离子方程式:___________ 。
(4)向实验④所得溶液中加入过量NaOH溶液得到沉淀M,用元素分析仪分析,M为铜的氧化物,提纯干燥后的M在惰性气体氛围下加热,12 g M完全分解为10 g CuO。M的化学式为___________ ;M能与稀硫酸酸化的KI溶液反应生成白色沉淀CuI(碘化亚铜),在滤液中加入淀粉溶液,溶液变蓝色。写出M和稀硫酸酸化的KI溶液反应的离子方程式:___________ 。
| 序号 | 操作 | 现象 |
| ① | 常温下,在铁片中加入过量的浓硫酸 | 没有明显现象 |
| ② | 常温下,在铜片上加入过量的浓硫酸 | 没有明显现象 |
| ③ | 在铜和过量30%H2O2的混合溶液中加入Na2SO4溶液 | 没有明显现象 |
| ④ | 在铜和过量30%H2O2的混合溶液中加入稀硫酸 | 溶液变蓝色,并产生气泡 |
(1)实验①没有明显现象的原因是
(2)为了引发实验②中的反应,宜采取的措施是
(3)实验④产生的气体是
(4)向实验④所得溶液中加入过量NaOH溶液得到沉淀M,用元素分析仪分析,M为铜的氧化物,提纯干燥后的M在惰性气体氛围下加热,12 g M完全分解为10 g CuO。M的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氨气在工农业生产中有重要应用。
(1)①氮气用于工业合成氨,写出氮气的电子式:________ ;
②NH3的稳定性比PH3________ (填“强”或“弱”)。
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
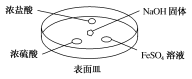
①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_________ 。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是________ (写化学式,一种即可)。
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O===Fe(OH)2↓+2NH 和
和________ 。
(3)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,用平衡移动原理解释其原因:____________________ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为_________________ ,若反应中有0.3 mol电子发生转移时,生成亚硝酸的质量为________ g(小数点后保留两位有效数字)。
(1)①氮气用于工业合成氨,写出氮气的电子式:
②NH3的稳定性比PH3
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O===Fe(OH)2↓+2NH
 和
和(3)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,用平衡移动原理解释其原因:
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
您最近一年使用:0次



