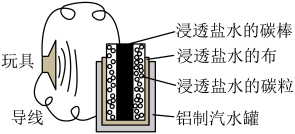
下列有关电极方程式或离子方程式错误的是
A.碱性锌锰电池的负极反应: |
B.用惰性电极电解氯化镁溶液时的阴极反应: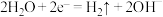 |
C. 溶液中通入少量 溶液中通入少量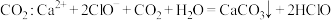 |
D.乙醛与新制的 碱性悬浊液共热: 碱性悬浊液共热: |
更新时间:2024-05-14 14:51:22
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式正确的是
| A.加热FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O= Fe(OH)3↓+3H+ |
| B.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O |
| C.碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++CO2↑+2H2O |
| D.铜与硝酸银溶液的反应:Cu+2Ag+= Cu2++2Ag |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列化学用语正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙: 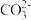 (aq)+CaSO4(s)=CaCO3(s)+ (aq)+CaSO4(s)=CaCO3(s)+  (aq) (aq) |
B.电解氯化镁水溶液:2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
C.向硫酸氢钠溶液中滴加氢氧化钡溶液至 恰好沉淀完全:Ba2++2OH-+2H++ 恰好沉淀完全:Ba2++2OH-+2H++ =BaSO4↓+2H2O =BaSO4↓+2H2O |
D.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3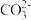 =Al2(SO4)3↓ =Al2(SO4)3↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一种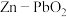 电池工作原理如装置图所示。下列说法正确的是
电池工作原理如装置图所示。下列说法正确的是

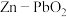 电池工作原理如装置图所示。下列说法正确的是
电池工作原理如装置图所示。下列说法正确的是
| A.电池工作时电能转化为化学能 |
B.放电过程中电极 区溶液的 区溶液的 增大 增大 |
C.电池工作一段时间后 浓度增大 浓度增大 |
D. 极区的反应为 极区的反应为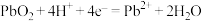 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】微生物燃料电池可净化废水,同时还能获得能源或有价值的化学产品,图1为其工作原理,图2为废水中Cr2O72-浓度与去除率的关系。下列说法不正确的是( )


| A.图1燃料电池工作一段时间后,N极附近的溶液pH增大 |
| B.外电路转移2 mol电子时,N极消耗标准状况下11.2 L O2 |
| C.图2中Cr2O72-浓度较大时,其去除率下降可能是Cr2O72-浓度较大造成还原菌失活所致 |
| D.M极为电池负极,发生的电极反应为CH3COOH+2H2O-8e-=2CO2↑+8H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】基于甲烷蒸汽重整工业制氢面临着大量的“碳排放”,我国科技工作者发明了一种电化学分解甲烷的方法,从而实现了碳和水的零排放方式生产氢气。电化学反应机理如图所示。下列说法错误的是


| A.Ni-YSZ电极为阳极,Ni电极为阴极 |
| B.阳极的电极反应式为CH4-4e-+2O2-=CO2+2H2 |
C.电解的总反应为CH4 C+2H2 C+2H2 |
| D.标准状况下,每分解33.6L的CH4,Ni电极产生O2-的物质的量为3mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在盛有饱和碳酸钠溶液的烧杯中插入惰性电极,保持温度不变,通电一定时间后
| A.溶液的PH将增大 |
| B.溶液中的钠离子与碳酸根离子的数目不变 |
| C.溶液的浓度增大并有晶体析出 |
| D.溶液的浓度不变并有晶体析出 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式正确的是
A.乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:CH3CHO+2Cu(OH)2+OH— Cu2O↓+3H2O+CH3COO— Cu2O↓+3H2O+CH3COO— |
B.强碱性溶液中NaClO将Fe(OH)3氧化为FeO :3ClO—+2Fe(OH)3=2 FeO :3ClO—+2Fe(OH)3=2 FeO +3Cl—+4H++H2O +3Cl—+4H++H2O |
C.苯酚钠溶液中通入少量CO2:2C6H5O—+CO2+H2O→2C6H5OH+CO |
D.NaClO溶液中通入少量SO2:2ClO—+SO2+H2O=2HClO+SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列方法或操作不能达到相应实验目的的是
| 选项 | 实验目的 | 方法或操作 |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 相同条件下,用金属钠分别与水和乙醇反应 |
| B | 证明蛋白质在某些无机盐溶液作用下发生变性 | 向鸡蛋清溶液中加入饱和硫酸钢溶液,有沉淀析出;再把沉淀加入蒸馏水中 |
| C | 验证苯和液溴在 的催化下发生取代反应 的催化下发生取代反应 | 将反应产生的混合气体通入 溶液中,观察是否有淡黄色沉淀生成 溶液中,观察是否有淡黄色沉淀生成 |
| D | 检验乙醛中的官能团 | 在试管中加入 10%的 10%的 溶液,滴入4~6滴2%的 溶液,滴入4~6滴2%的 溶液,振荡后加入 溶液,振荡后加入 乙醛溶液,加热,观察是否出现砖红色沉淀 乙醛溶液,加热,观察是否出现砖红色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次