现有下列九种物质:①HCl气体②Cu ③蔗糖 ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氯酸钾溶液 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)属于电解质的是________ ;属于非电解质的是________ 。
(2)②和⑧反应的化学方程式为:3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑+ 4H2O上述反应中氧化产物是____________ 。硝酸没有全部参加氧化还原反应,参加氧化还原反应的硝酸占总硝酸的_______ 。用双线桥法分析上述反应(只需标出电子得失的方向和数目)_____ 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑+ 4H2O
(3)上述九种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为________
(4)⑨在水中的电离方程式为______ ,
(5)2 g ⑨溶于水配成1000 mL溶液,SO42-的物质的量浓度为________ 。
(1)属于电解质的是
(2)②和⑧反应的化学方程式为:3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑+ 4H2O上述反应中氧化产物是
(3)上述九种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为
(4)⑨在水中的电离方程式为
(5)2 g ⑨溶于水配成1000 mL溶液,SO42-的物质的量浓度为
更新时间:2016-12-09 01:16:20
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求写出下列方程式。
有下列七种物质:①盐酸;②Fe;③CH3COOH;④SO2;⑤熔融的Al2(SO4)3;⑥NaHCO3固体;⑦NaOH溶液;
(1)属于非电解质的是___________ ;属于电解质的是___________ ;属于强电解质的是___________ ;所给状态能导电的是___________ 。(以上均填所给物质的序号)
(2)将⑥加入①中发生反应的离子方程式为:___________ 。
(3)将③加入⑦中,发生反应的离子方程式为:___________ 。
(4)过氧化钠可做呼吸面具的供氧剂,有关化学方程式___________ 。除去NaHCO3溶液中的Na2CO3的有关化学方程式为___________ 。
有下列七种物质:①盐酸;②Fe;③CH3COOH;④SO2;⑤熔融的Al2(SO4)3;⑥NaHCO3固体;⑦NaOH溶液;
(1)属于非电解质的是
(2)将⑥加入①中发生反应的离子方程式为:
(3)将③加入⑦中,发生反应的离子方程式为:
(4)过氧化钠可做呼吸面具的供氧剂,有关化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
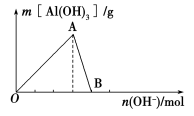
【推荐2】如图所示为一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线。
请回答下列问题:
(1)A点时已参加反应的AlCl3和NaOH的物质的量之比为________ 。
(2)AB段曲线所表示的反应的离子方程式为_________________________ 。
(3)向B处生成的溶液中通入二氧化碳,可观察到的现象是_______________________ 。
(4)向含有0.1 mol NH4Al(SO4)2的溶液中逐滴加入5 mol·L−1 NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图________ 。
请回答下列问题:
(1)A点时已参加反应的AlCl3和NaOH的物质的量之比为
(2)AB段曲线所表示的反应的离子方程式为
(3)向B处生成的溶液中通入二氧化碳,可观察到的现象是
(4)向含有0.1 mol NH4Al(SO4)2的溶液中逐滴加入5 mol·L−1 NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:

(1)补全上述①②④各步反应的离子方程式:
①Mg+2H+═Mg2++H2↑,_______ ;
②_______ ,_______ ,Mg2++2OH-═Mg(OH)2↓;
③OH﹣+CO2= ,CO2+2H2O+AlO
,CO2+2H2O+AlO ═Al(OH)3↓+
═Al(OH)3↓+  ;
;
④_______ 。
(2)该样品中铝的质量分数是_______ 。
(3)第②步中加入NaOH溶液不足时,会使测定结果_______ (填“偏高”、“ 偏低”、“无影响”,下同);第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果_______ ;第④步对沉淀灼烧不充分时,会使测定结果_______ 。

(1)补全上述①②④各步反应的离子方程式:
①Mg+2H+═Mg2++H2↑,
②
③OH﹣+CO2=
 ,CO2+2H2O+AlO
,CO2+2H2O+AlO ═Al(OH)3↓+
═Al(OH)3↓+  ;
;④
(2)该样品中铝的质量分数是
(3)第②步中加入NaOH溶液不足时,会使测定结果
您最近一年使用:0次
【推荐1】某试样含有 、
、 及㤢性物质。称取试样
及㤢性物质。称取试样 ,溶解后配制到
,溶解后配制到 容量瓶中。吸取
容量瓶中。吸取 ,在
,在 介质中用
介质中用 将
将 还原为
还原为 ,除去过量的
,除去过量的 后调至中性测定
后调至中性测定 ,消耗
,消耗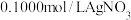 溶液
溶液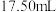 。另吸取
。另吸取 试液用
试液用 酸化后加热除去
酸化后加热除去 ,再调至中性,滴定过剩
,再调至中性,滴定过剩 时消耗了上述
时消耗了上述 溶液
溶液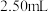 。计算试样中
。计算试样中 、
、 的质量分数
的质量分数_______ 、_______ 。
 、
、 及㤢性物质。称取试样
及㤢性物质。称取试样 ,溶解后配制到
,溶解后配制到 容量瓶中。吸取
容量瓶中。吸取 ,在
,在 介质中用
介质中用 将
将 还原为
还原为 ,除去过量的
,除去过量的 后调至中性测定
后调至中性测定 ,消耗
,消耗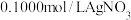 溶液
溶液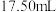 。另吸取
。另吸取 试液用
试液用 酸化后加热除去
酸化后加热除去 ,再调至中性,滴定过剩
,再调至中性,滴定过剩 时消耗了上述
时消耗了上述 溶液
溶液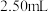 。计算试样中
。计算试样中 、
、 的质量分数
的质量分数
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有五种溶液,分别含下列离子:①Ag+、②Mg2+、③Fe2+、④Al3+、⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______ ,遇KSCN溶液显血红色的是______ ,加铁粉后溶液增重的是______ ;
(2)向③的溶液中滴加NaOH溶液,现象是______________________ ,写出此步操作属于氧化还原反应的化学方程式_____________________ 。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是
(2)向③的溶液中滴加NaOH溶液,现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁、钴(Co)、镍(Ni)是同族元素,主要化合价均为+2、+3价,都是较活泼的金属,它们的化合物在工业上有重要的应用。完成下列填空:
(1)Co2+和Fe3+均可与KSCN溶液发生相似的反应。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为_______________________ 。
(2)碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
第一步:向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+。
反应的离子方程式有:
①__________ ;
②___NiS+___ +___H+→___Ni2++___S+___Cl-+___H2O
+___H+→___Ni2++___S+___Cl-+___H2O
配平反应②。__________
第二步:再加入Na2CO3溶液,产生的沉淀即为碳酸镍。
检验Ni2+是否沉淀完全的方法是_____________________________________ 。
(1)Co2+和Fe3+均可与KSCN溶液发生相似的反应。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为
(2)碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
第一步:向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+。
反应的离子方程式有:
①
②___NiS+___
 +___H+→___Ni2++___S+___Cl-+___H2O
+___H+→___Ni2++___S+___Cl-+___H2O配平反应②。
第二步:再加入Na2CO3溶液,产生的沉淀即为碳酸镍。
检验Ni2+是否沉淀完全的方法是
您最近一年使用:0次



