名校
1 . Ⅰ. 可用作清洁剂、防腐剂等。请按要求回答下列问题:
可用作清洁剂、防腐剂等。请按要求回答下列问题:
(1)下列关于 的说法正确的是______。
的说法正确的是______。
(2)将 溶液滴加到
溶液滴加到 溶液中至溶液呈中性时,发生反应的离子方程式为
溶液中至溶液呈中性时,发生反应的离子方程式为______ 。
Ⅱ.请按要求回答下列问题:
(3) 溶液与
溶液与 溶液反应的离子方程为
溶液反应的离子方程为______ 。
(4)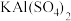 的电离方程式
的电离方程式______ 。
(5)工业上制取 用
用 与C、
与C、 在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是
在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是______ 。
(6)反应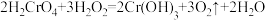 中
中 的变化
的变化
①该反应的氧化产物是______ (填化学式)。
②在该反应方程式中用单线桥法标明电子转移的方向和数目______ 。
 可用作清洁剂、防腐剂等。请按要求回答下列问题:
可用作清洁剂、防腐剂等。请按要求回答下列问题:(1)下列关于
 的说法正确的是______。
的说法正确的是______。A. 固体能导电 固体能导电 |
B. 溶液的导电性一定强于 溶液的导电性一定强于 溶液 溶液 |
C. 属于强电解质 属于强电解质 |
D. 溶液显酸性 溶液显酸性 |
 溶液滴加到
溶液滴加到 溶液中至溶液呈中性时,发生反应的离子方程式为
溶液中至溶液呈中性时,发生反应的离子方程式为Ⅱ.请按要求回答下列问题:
(3)
 溶液与
溶液与 溶液反应的离子方程为
溶液反应的离子方程为(4)
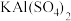 的电离方程式
的电离方程式(5)工业上制取
 用
用 与C、
与C、 在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是
在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是(6)反应
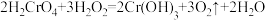 中
中 的变化
的变化
①该反应的氧化产物是
②在该反应方程式中用单线桥法标明电子转移的方向和数目
您最近一年使用:0次
名校
解题方法
2 . 用分类思想研究一类物质的通性和特殊性是学习化学的一种重要方法。下图是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。已知: ;
;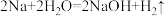 ;
; 。请根据你所学的知识,按要求填空:
。请根据你所学的知识,按要求填空:
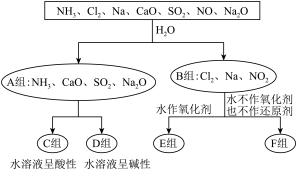
(1)上述第一级分类标准(分成A、B组的依据)是___________ 。
(2)F组物质中除了Cl2外还有___________ (填化学式,下同)。
(3)A组中属于电解质的是___________ 。
(4)已知Cl2可发生如下反应: 。
。
①该反应中氧化剂是___________ ,氧化产物是___________ 。
②用双线桥法标出电子转移的数目和方向:___________ 。
(5)氯化铵溶液常用于焊接。在焊接铜器时可用氯化铵除去铜器表面的氧化铜以便焊接,其反应如下:
___________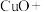 ___________
___________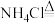 ___________
___________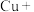 ___________
___________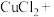 ___________
___________ ___________
___________
配平此氧化还原反应的化学方程式。___________
 ;
;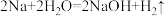 ;
; 。请根据你所学的知识,按要求填空:
。请根据你所学的知识,按要求填空:
(1)上述第一级分类标准(分成A、B组的依据)是
(2)F组物质中除了Cl2外还有
(3)A组中属于电解质的是
(4)已知Cl2可发生如下反应:
 。
。①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
(5)氯化铵溶液常用于焊接。在焊接铜器时可用氯化铵除去铜器表面的氧化铜以便焊接,其反应如下:
___________
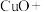 ___________
___________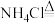 ___________
___________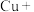 ___________
___________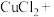 ___________
___________ ___________
___________
配平此氧化还原反应的化学方程式。
您最近一年使用:0次
名校
解题方法
3 . I.将下列化学方程式改写成离子方程式
(1)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O:
MnCl2+Cl2↑+2H2O:___________ 。
II.配平下面反应(化学计量数是1的也请填上)
(2)配平下面反应:___________ 。
___________KClO3+___________HCl=___________KCl+___________Cl2↑+___________H2O
III.下列反应属于分类中的氧化还原反应:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O。回答下列问题
(3)___________ 是氧化产物
(4)浓盐酸在反应中显示出来的性质是___________ 。
(5)用单线桥法标明电子转移的方向和数目___________ 。
(6)每生成1个Cl2,转移的电子数为___________ 。
IV.一定条件下,可用来消除NOx,生成两种对环境无害的物质。
(7)请写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。
(1)MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O:
MnCl2+Cl2↑+2H2O:II.配平下面反应(化学计量数是1的也请填上)
(2)配平下面反应:
___________KClO3+___________HCl=___________KCl+___________Cl2↑+___________H2O
III.下列反应属于分类中的氧化还原反应:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O。回答下列问题
(3)
(4)浓盐酸在反应中显示出来的性质是
(5)用单线桥法标明电子转移的方向和数目
(6)每生成1个Cl2,转移的电子数为
IV.一定条件下,可用来消除NOx,生成两种对环境无害的物质。
(7)请写出
 与
与 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 某同学做实验时白色衣服上沾了一些KMnO4,产生褐色斑点,如果用草酸(H2C2O4)的稀溶液洗涤马上可复原,其离子方程式为: +H2C2O4+H+→CO2↑+Mn2++___________(未配平)。关于此反应的叙述正确的是
+H2C2O4+H+→CO2↑+Mn2++___________(未配平)。关于此反应的叙述正确的是
 +H2C2O4+H+→CO2↑+Mn2++___________(未配平)。关于此反应的叙述正确的是
+H2C2O4+H+→CO2↑+Mn2++___________(未配平)。关于此反应的叙述正确的是| A.该反应的氧化产物是Mn2+ |
| B.离子方程式横线上的生成物是OH- |
| C.配平离子方程式,H+的计量数是6 |
| D.有1个CO2生成时,转移电子的个数为10 |
您最近一年使用:0次
名校
解题方法
5 . 写出下列化学反应方程
(1)氢气在氧气中燃烧___________ ;
(2)过氧化氢在二氧化锰的催化下分解___________ ;
(3)锌和硫酸反应制取氢气的反应方程式___________ 。
(1)氢气在氧气中燃烧
(2)过氧化氢在二氧化锰的催化下分解
(3)锌和硫酸反应制取氢气的反应方程式
您最近一年使用:0次
名校
解题方法
6 . 饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出:在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出:在碱性条件下用铝粉将 还原为
还原为 :
: 。请回答下列问题:
。请回答下列问题:
(1)请配平其化学方程式并用双线桥表示电子转移的方向和数目:___________ 。
(2)上述反应中,还原剂是___________ ,还原产物是___________ 。
(3)另一种去除污水中 的方法是在酸性污水中加入铁粉,最终生成铵根和FeO(OH),该反应的离子方程式为:
的方法是在酸性污水中加入铁粉,最终生成铵根和FeO(OH),该反应的离子方程式为:___________ 。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出:在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出:在碱性条件下用铝粉将 还原为
还原为 :
: 。请回答下列问题:
。请回答下列问题:(1)请配平其化学方程式并用双线桥表示电子转移的方向和数目:
(2)上述反应中,还原剂是
(3)另一种去除污水中
 的方法是在酸性污水中加入铁粉,最终生成铵根和FeO(OH),该反应的离子方程式为:
的方法是在酸性污水中加入铁粉,最终生成铵根和FeO(OH),该反应的离子方程式为:
您最近一年使用:0次
解题方法
7 .  在常温下就可以与
在常温下就可以与 反应,化学方程式如下:
反应,化学方程式如下: (白色固体)
(白色固体) (未配平),设阿伏加德罗常数的值为
(未配平),设阿伏加德罗常数的值为 ,回答下列问题。
,回答下列问题。
(1)配平化学方程式,并用单线桥法表示电子转移的方向和数目:___________ 。
___________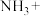 ___________
___________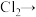 ___________
___________ ___________
___________
(2)上述反应中的氧化产物为___________ (填化学式),氧化剂与还原剂的物质的量之比为___________ 。
(3)当生成1mol氮气时,被氧化的物质的质量为___________ ,反应中转移电子数为___________  。
。
(4)下列说法中正确的是___________(填字母)。
(5)已知:CuO能够和 在加热条件下反应生成两种单质,写出在加热条件下CuO和
在加热条件下反应生成两种单质,写出在加热条件下CuO和 反应的化学方程式:
反应的化学方程式:___________ 。
 在常温下就可以与
在常温下就可以与 反应,化学方程式如下:
反应,化学方程式如下: (白色固体)
(白色固体) (未配平),设阿伏加德罗常数的值为
(未配平),设阿伏加德罗常数的值为 ,回答下列问题。
,回答下列问题。(1)配平化学方程式,并用单线桥法表示电子转移的方向和数目:
___________
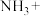 ___________
___________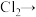 ___________
___________ ___________
___________
(2)上述反应中的氧化产物为
(3)当生成1mol氮气时,被氧化的物质的质量为
 。
。(4)下列说法中正确的是___________(填字母)。
| A.上述反应中能观察到有白烟产生 |
| B.上述反应中生成的气体有刺激性气味 |
C. 不含金属阳离子,不属于盐类 不含金属阳离子,不属于盐类 |
| D.可用浓氨水来检验氯气管道是否泄漏 |
 在加热条件下反应生成两种单质,写出在加热条件下CuO和
在加热条件下反应生成两种单质,写出在加热条件下CuO和 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
解题方法
8 . 常温下,向H2O2溶液中滴加少量Fe2(SO4)3溶液,反应原理如图所示,下列说法不正确的是


| A.该反应过程中,M是Fe3+,M' 是Fe2+ |
| B.当反应中有1molO2生成时,转移电子数为2mol |
C.该过程的总反应方程式为: |
| D.H2O2生产过程要严格避免混入Fe2+ |
您最近一年使用:0次
名校
解题方法
9 . 含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。某含氮废水中 浓度为
浓度为 ,现采用铝还原法来将
,现采用铝还原法来将 还原为
还原为 。
。
(1) 中氮元素的化合价为
中氮元素的化合价为___________ 。
(2)配平下列有关反应的化学方程式并用单线桥分析该反应的电子转移情况。_______

(3)上述反应中,还原剂是___________ ,被还原的元素是___________ 。
(4)有上述废水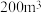 ,若要完全处理所含的
,若要完全处理所含的 ,则需消耗金属铝的质量为
,则需消耗金属铝的质量为___________ g。
(5)某强酸反应体系中发生的一个离子反应中,反应物和生成物共六种微粒: 和
和 ,已知NH
,已知NH 为该反应的还原产物,写出该反应的离子方程式:
为该反应的还原产物,写出该反应的离子方程式:___________ 。
 浓度为
浓度为 ,现采用铝还原法来将
,现采用铝还原法来将 还原为
还原为 。
。(1)
 中氮元素的化合价为
中氮元素的化合价为(2)配平下列有关反应的化学方程式并用单线桥分析该反应的电子转移情况。

(3)上述反应中,还原剂是
(4)有上述废水
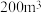 ,若要完全处理所含的
,若要完全处理所含的 ,则需消耗金属铝的质量为
,则需消耗金属铝的质量为(5)某强酸反应体系中发生的一个离子反应中,反应物和生成物共六种微粒:
 和
和 ,已知NH
,已知NH 为该反应的还原产物,写出该反应的离子方程式:
为该反应的还原产物,写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题:
I.KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(1)请用“双线桥”表示上述反应电子转移的方向和数目_______ 。
(2)请将上述反应改写成离子方程式________ 。
(3)浓盐酸在反应中体现出来的性质有______ (填序号)。
①还原性 ②酸性 ③氧化性 ④碱性
(4)若反应生成21.3g氯气,则消耗还原剂的质量为______ g。
II.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是______ 。(填化学式)
(6)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:________ 。
②每生成1个FeO 转移
转移______ 个电子。
I.KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(1)请用“双线桥”表示上述反应电子转移的方向和数目
(2)请将上述反应改写成离子方程式
(3)浓盐酸在反应中体现出来的性质有
①还原性 ②酸性 ③氧化性 ④碱性
(4)若反应生成21.3g氯气,则消耗还原剂的质量为
II.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(6)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成1个FeO
 转移
转移
您最近一年使用:0次



