解题方法
1 . A、B、C、D是中学化学常见的三种物质,它们之间的相互转化关系如下(反应条件及部分产物已略去):_______ 、_______ 、_______ 。
(2)若A是空气中体积分数最大的气体,C是红棕色气体,则反应①②③的化学方程式分别为_______ 、_______ 、_______ 。
(3)①②③三步反应中,一定属于氧化还原反应的是_______ (填序号)。
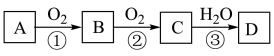
(2)若A是空气中体积分数最大的气体,C是红棕色气体,则反应①②③的化学方程式分别为
(3)①②③三步反应中,一定属于氧化还原反应的是
您最近一年使用:0次
解题方法
2 .  是一种安全高效灭菌消毒剂,我国从2000年起就逐渐用
是一种安全高效灭菌消毒剂,我国从2000年起就逐渐用 取代
取代 对饮用水进行消毒。下图是某实验室用于制备一定量较纯净的
对饮用水进行消毒。下图是某实验室用于制备一定量较纯净的 的装置(某些夹持装置和垫持用品省略)。已知:
的装置(某些夹持装置和垫持用品省略)。已知:
①实验室可用亚氯酸钠固体 与氯气反应来制备
与氯气反应来制备 ;
;
②通常情况下, 是一种有刺激性气味的黄绿色气体,熔点为
是一种有刺激性气味的黄绿色气体,熔点为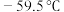 ,沸点为
,沸点为 。常温下
。常温下 水约溶解
水约溶解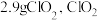 遇热水不稳定。
遇热水不稳定。
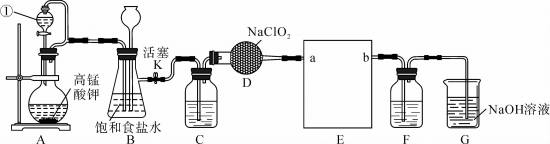
请回答下列问题:
(1)仪器①的名称为___________ 。
(2)检验装置A、B的气密性:___________ ,从长颈漏斗处加水至液面高于锥形瓶中的液面,若一段时间后长颈漏斗内液面不下降,则说明装置气密性良好。
(3)装置B的作用是___________ ,装置C中盛放的试剂是___________ 。
(4)写出装置D中制备 的化学方程式,并用单线桥法标出电子转移的方向和数目
的化学方程式,并用单线桥法标出电子转移的方向和数目_______ 。
(5)装置E采用下图所示装置,其作用是___________ ,正确的连接顺序为a→________ ________ →b。
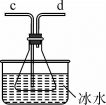
(6)尾气吸收装置中发生反应的离子方程式为___________ 。
 是一种安全高效灭菌消毒剂,我国从2000年起就逐渐用
是一种安全高效灭菌消毒剂,我国从2000年起就逐渐用 取代
取代 对饮用水进行消毒。下图是某实验室用于制备一定量较纯净的
对饮用水进行消毒。下图是某实验室用于制备一定量较纯净的 的装置(某些夹持装置和垫持用品省略)。已知:
的装置(某些夹持装置和垫持用品省略)。已知:①实验室可用亚氯酸钠固体
 与氯气反应来制备
与氯气反应来制备 ;
;②通常情况下,
 是一种有刺激性气味的黄绿色气体,熔点为
是一种有刺激性气味的黄绿色气体,熔点为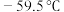 ,沸点为
,沸点为 。常温下
。常温下 水约溶解
水约溶解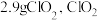 遇热水不稳定。
遇热水不稳定。
请回答下列问题:
(1)仪器①的名称为
(2)检验装置A、B的气密性:
(3)装置B的作用是
(4)写出装置D中制备
 的化学方程式,并用单线桥法标出电子转移的方向和数目
的化学方程式,并用单线桥法标出电子转移的方向和数目(5)装置E采用下图所示装置,其作用是

(6)尾气吸收装置中发生反应的离子方程式为
您最近一年使用:0次
名校
3 . 探究 与水的反应,实验如下(实验中加入的溶液均过量):
与水的反应,实验如下(实验中加入的溶液均过量):
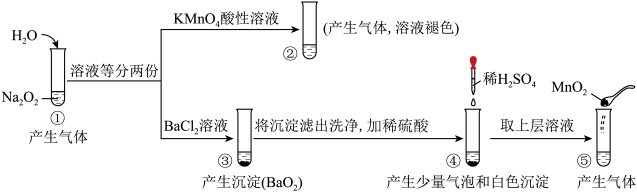
已知:i. 是二元弱酸,能电离出
是二元弱酸,能电离出 和
和
ii.②中发生反应: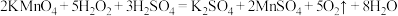
iii. 可以溶解在稀
可以溶解在稀 中
中
下列说法中不正确的是
 与水的反应,实验如下(实验中加入的溶液均过量):
与水的反应,实验如下(实验中加入的溶液均过量):
已知:i.
 是二元弱酸,能电离出
是二元弱酸,能电离出 和
和
ii.②中发生反应:
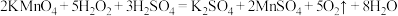
iii.
 可以溶解在稀
可以溶解在稀 中
中下列说法中不正确的是
A.③中生成 的离子反应方程式为 的离子反应方程式为 |
| B.①、⑤中产生的气体能使带火星的木条复燃 |
| C.①、④中均只发生了氧化还原反应 |
D.②、⑤中 与 与 的作用不相同,产生气体的量也不同 的作用不相同,产生气体的量也不同 |
您最近一年使用:0次
名校
4 . 某学习小组设计了如下实验,探究浓度和温度对反应的影响。
实验探究Ⅰ:
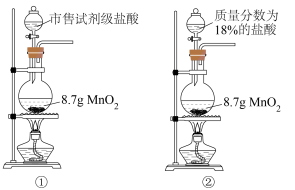
已知市售试剂级盐酸的密度为1.19g/mL,质量分数为37%;质量分数低于20%的盐酸为稀盐酸。
(1)装置①②同时加热,①中生成黄绿色气体,②中无明显变化,请从浓度和还原性的角度简要解释其原因:___________ ;①中发生反应的离子方程式为___________ ;8.7gMnO2与33.1mL市售试剂级盐酸在加热条件下反应,生成氯气的物质的量是否为0.1mol?______ (填“是"或“否),并简述其原因:___________ 。
实验探究Ⅱ:
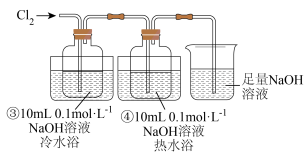
(2)通入氯气后,取出2mL装置③反应瓶中无色液体置于试管中,滴加2滴紫色石蕊溶液,溶液变蓝后褪色,请用简要的语言叙述其原因:___________ 。
(3)装置④中氧化产物和还原产物的物质的量之比为1:5,写出该反应的离子方程式并用双线桥表示电子转移的方向和数目:___________ 。
(4)装置③中所得溶液称之为“84”消毒液,其不能与洁厕灵(含盐酸)同时使用的原因为___________ (用离子方程式解释)。
实验探究Ⅰ:

已知市售试剂级盐酸的密度为1.19g/mL,质量分数为37%;质量分数低于20%的盐酸为稀盐酸。
(1)装置①②同时加热,①中生成黄绿色气体,②中无明显变化,请从浓度和还原性的角度简要解释其原因:
实验探究Ⅱ:

(2)通入氯气后,取出2mL装置③反应瓶中无色液体置于试管中,滴加2滴紫色石蕊溶液,溶液变蓝后褪色,请用简要的语言叙述其原因:
(3)装置④中氧化产物和还原产物的物质的量之比为1:5,写出该反应的离子方程式并用双线桥表示电子转移的方向和数目:
(4)装置③中所得溶液称之为“84”消毒液,其不能与洁厕灵(含盐酸)同时使用的原因为
您最近一年使用:0次
名校
解题方法
5 . 稀土元素被称为“工业维生素”,包括钇、铈等元素,稀土元素能显著提升建造航母及舰载机的材料性能。
Ⅰ.工业上吸收SO2和NO,以获得Na2S2O4和NH4NO3产品的流程图如图(Ce为铈元素)。

(1)装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO 、NO
、NO 。请写出生成相等数目的NO
。请写出生成相等数目的NO 和NO
和NO 时的离子方程式,并用单线桥表示电子转移
时的离子方程式,并用单线桥表示电子转移_______ 。
Ⅱ.含有稀土元素钇的氧化钇(Y2O3)被广泛应用于航空航天涂层材料。以富钇稀土矿(主要成分为Y2O3,含有少量的Fe2O3、CuO、SiO2等杂质)生产氧化钇的工艺流程如图,回答下列问题:

(2)在粉碎机中研磨粉碎的目的是_______ 。
(3)流程中操作Ⅰ、Ⅱ、Ⅲ的名称是_______ ,“酸溶”过程中,Y2O3发生反应的离子方程式为_______ 。
(4)向反应釜2中通入气体X使溶液呈碱性,调节溶液的pH除去滤液1中杂质,沉淀Ⅱ的主要成分是_______ (填化学式)。
(5)流程中可循环使用的物质为_______ (填名称)。
Ⅰ.工业上吸收SO2和NO,以获得Na2S2O4和NH4NO3产品的流程图如图(Ce为铈元素)。

(1)装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO
 、NO
、NO 。请写出生成相等数目的NO
。请写出生成相等数目的NO 和NO
和NO 时的离子方程式,并用单线桥表示电子转移
时的离子方程式,并用单线桥表示电子转移Ⅱ.含有稀土元素钇的氧化钇(Y2O3)被广泛应用于航空航天涂层材料。以富钇稀土矿(主要成分为Y2O3,含有少量的Fe2O3、CuO、SiO2等杂质)生产氧化钇的工艺流程如图,回答下列问题:

(2)在粉碎机中研磨粉碎的目的是
(3)流程中操作Ⅰ、Ⅱ、Ⅲ的名称是
(4)向反应釜2中通入气体X使溶液呈碱性,调节溶液的pH除去滤液1中杂质,沉淀Ⅱ的主要成分是
(5)流程中可循环使用的物质为
您最近一年使用:0次
名校
解题方法
6 . 制备某无机化合物的转化流程如图所示,下列说法错误的是


A.该转化流程中 均被循环使用,是催化剂 均被循环使用,是催化剂 |
| B.该循环过程中未涉及氧化还原反应 |
C.存在反应 |
| D.该工艺是利用食盐和石灰石制取纯碱 |
您最近一年使用:0次
2024-01-07更新
|
96次组卷
|
2卷引用: 云南省曲靖市罗平县第一中学2023-2024学年高一上学期期中考试化学试题
名校
7 . 高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种制备流程如图:
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种制备流程如图:

回答下列问题:
(1) 中
中 的化合价为
的化合价为______ 。
(2)写出 的电离方程式
的电离方程式______ 。
(3)“反应Ⅰ”不能在较高温度下进行的原因是______ 。
(4)“反应Ⅱ”为碱性条件下制备 ,配平该离子反应方程式并用单线桥标出电子转移的方向和数目:
,配平该离子反应方程式并用单线桥标出电子转移的方向和数目:______ 。
______ +______
+______ +______
+______ →______
→______ +______
+______ +______
+______
该反应中, 被
被______ 。(填“氧化”或“还原”)
(5)用高铁酸钠作水处理剂的原理如图所示。

【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
①过程i中活细菌表现了______ 。(填“氧化”或“还原”)性,过程ⅲ属于______ 。(填“物理”或“化学”)变化。
②根据上述原理分析,作水处理剂时, 的作用有
的作用有______ 。
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种制备流程如图:
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种制备流程如图:
回答下列问题:
(1)
 中
中 的化合价为
的化合价为(2)写出
 的电离方程式
的电离方程式(3)“反应Ⅰ”不能在较高温度下进行的原因是
(4)“反应Ⅱ”为碱性条件下制备
 ,配平该离子反应方程式并用单线桥标出电子转移的方向和数目:
,配平该离子反应方程式并用单线桥标出电子转移的方向和数目:______
 +______
+______ +______
+______ →______
→______ +______
+______ +______
+______
该反应中,
 被
被(5)用高铁酸钠作水处理剂的原理如图所示。

【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
①过程i中活细菌表现了
②根据上述原理分析,作水处理剂时,
 的作用有
的作用有
您最近一年使用:0次
名校
解题方法
8 . 某课外活动小组为了研究“干燥的CO2不能与Na2O2反应”和“潮湿的CO2才能与Na2O2反应”,设计了如下实验装置。
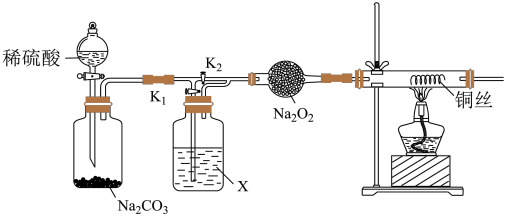
(1)写出过氧化钠与CO2反应的方程式,并用双线桥表示该反应的电子转移情况_____________________ 。
(2)如图装置,在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2。打开K1 关闭K2
关闭K2 加热铜丝,X是
加热铜丝,X是_________ 。
(3)若打开K2,关闭K1,出现____________________ 现象,可证明潮湿的CO2与Na2O2反应产生了O2。某同学提出质疑,认为不一定是CO2与Na2O2反应产生了O2导致该现象的产生,请用化学方程式解释该同学的提出质疑原因_____________________________ 。
(4)通过实验测得反应结束后,球形干燥管中仅有Na2CO3和未反应完的Na2O2固体,为测得固体混合物的组成,某实验小组将1.45g固体混合物溶于水中。然后向溶液中滴加盐酸,产生气体的体积随盐酸的加入量如图所示。

①加入盐酸0~100时间段,溶液中发生化学反应方程式有:_______________________________________ 。
②设计另外一种实验方案来测定Na2CO3和Na2O2固体混合物中Na2O2的质量分数,简单描述实验方案_____________________________________________ 。

(1)写出过氧化钠与CO2反应的方程式,并用双线桥表示该反应的电子转移情况
(2)如图装置,在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2。打开K1
 关闭K2
关闭K2 加热铜丝,X是
加热铜丝,X是(3)若打开K2,关闭K1,出现
(4)通过实验测得反应结束后,球形干燥管中仅有Na2CO3和未反应完的Na2O2固体,为测得固体混合物的组成,某实验小组将1.45g固体混合物溶于水中。然后向溶液中滴加盐酸,产生气体的体积随盐酸的加入量如图所示。

①加入盐酸0~100时间段,溶液中发生化学反应方程式有:
②设计另外一种实验方案来测定Na2CO3和Na2O2固体混合物中Na2O2的质量分数,简单描述实验方案
您最近一年使用:0次
解题方法
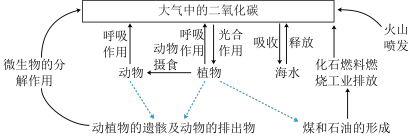
9 . 二氧化碳的捕捉与封存是未来实现低碳经济转型的重要途径。
(1)自然界中 主要循环方式如图所示,其中属于“二氧化碳的捕捉与封存”的除了“海水吸收”外,还有
主要循环方式如图所示,其中属于“二氧化碳的捕捉与封存”的除了“海水吸收”外,还有___________ (任写一点)。
(2)科学家设计出烧碱溶液捕捉 法,原理如图所示
法,原理如图所示

①该过程中能实现再生的反应为 和
和___________ 。
②若喷洒完 的
的 溶液后,测得吸收液中的
溶液后,测得吸收液中的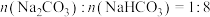 ,则被吸收的
,则被吸收的 在标况下的体积为
在标况下的体积为___________ L。
③下列溶液中,也能用作“捕捉”二氧化碳试剂的是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.稀硫酸
溶液 D.稀硫酸
(3)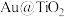 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如下左图所示。制得的甲烷
封存和能量储存双重效果,其原理如下左图所示。制得的甲烷 通过两步法可制取
通过两步法可制取 ,原理如下右图所示。
,原理如下右图所示。


①已知 中
中 为
为 价,则空心球催化剂技术中获得的
价,则空心球催化剂技术中获得的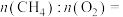
___________ 。
②写出步骤ii的化学方程式并用单线桥表示出电子转移的方向和数目___________ 。
③若不考虑过程中原料损失,则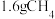 通过两步法最多可制得
通过两步法最多可制得 的物质的量为
的物质的量为___________ 。
(1)自然界中
 主要循环方式如图所示,其中属于“二氧化碳的捕捉与封存”的除了“海水吸收”外,还有
主要循环方式如图所示,其中属于“二氧化碳的捕捉与封存”的除了“海水吸收”外,还有
(2)科学家设计出烧碱溶液捕捉
 法,原理如图所示
法,原理如图所示
①该过程中能实现再生的反应为
 和
和②若喷洒完
 的
的 溶液后,测得吸收液中的
溶液后,测得吸收液中的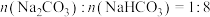 ,则被吸收的
,则被吸收的 在标况下的体积为
在标况下的体积为
③下列溶液中,也能用作“捕捉”二氧化碳试剂的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.稀硫酸
溶液 D.稀硫酸(3)
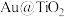 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如下左图所示。制得的甲烷
封存和能量储存双重效果,其原理如下左图所示。制得的甲烷 通过两步法可制取
通过两步法可制取 ,原理如下右图所示。
,原理如下右图所示。

①已知
 中
中 为
为 价,则空心球催化剂技术中获得的
价,则空心球催化剂技术中获得的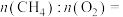
②写出步骤ii的化学方程式并用单线桥表示出电子转移的方向和数目
③若不考虑过程中原料损失,则
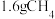 通过两步法最多可制得
通过两步法最多可制得 的物质的量为
的物质的量为
您最近一年使用:0次
10 . I.实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题。
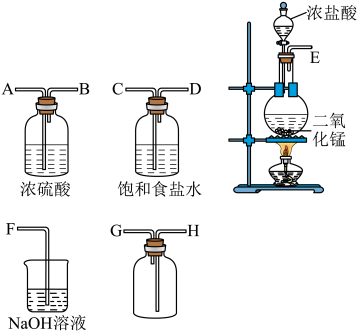
(1)连接上述仪器的正确顺序(填各接口处的字母):_______ 。
II.用如下装置制取氯气,并用氯气进行实验。回答下列问题:
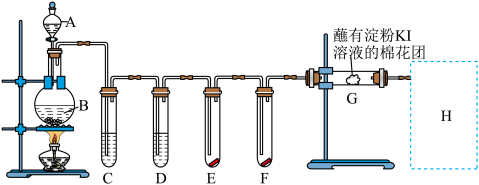
(2)A中盛有浓盐酸,B中盛有MnO2,写出反应方程式并用双线桥表示该反应中电子转移的方向和数目_______ 。反应中,如果有17.4g纯MnO2被还原,那么被氧化的氯化氢的质量为_______ 。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是_______ 。
(4)G处的现象是_______ 。
(5)H处装置的作用为_______ ,反应的离子方程式为_______ 。

(1)连接上述仪器的正确顺序(填各接口处的字母):
II.用如下装置制取氯气,并用氯气进行实验。回答下列问题:

(2)A中盛有浓盐酸,B中盛有MnO2,写出反应方程式并用双线桥表示该反应中电子转移的方向和数目
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(4)G处的现象是
(5)H处装置的作用为
您最近一年使用:0次



