1 . 金属钛(Ti)具有许多优异的性能,是航空、军工、电力等领域的必需材料。以金红石为原料制取金属钛,其中发生的化学反应之一:

(1)作还原剂的物质是_______ ,钛元素的化合价_______ (填“升高”或“降低”)。
(2)若反应中消耗了2molMg,则生成Ti的物质的量为_______ mol,转移电子的物质的量为_______ mol。

(1)作还原剂的物质是
(2)若反应中消耗了2molMg,则生成Ti的物质的量为
您最近一年使用:0次
名校
解题方法
2 . 以柠檬酸、硫酸亚铁、氨水等为原料制备食品添加剂—柠檬酸铁铵[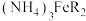 ,M=488g·mol-1]的流程如下所示:
,M=488g·mol-1]的流程如下所示:_______ 。
(2)欲检验FeSO4溶液是否被完全氧化,选用的试剂为_______。
(3)上述流程中,以13.90g绿矾(FeSO4·7H2O)配制FeSO4溶液,经各步骤后,最终制取得19.52g柠檬酸铁铵,则柠檬酸铁铵的产率为_______ 。
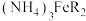 ,M=488g·mol-1]的流程如下所示:
,M=488g·mol-1]的流程如下所示: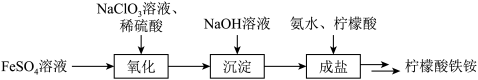
(2)欲检验FeSO4溶液是否被完全氧化,选用的试剂为_______。
| A.NaOH溶液 | B.KSCN溶液 | C.酸性KMnO4溶液 | D.新制氯水 |
(3)上述流程中,以13.90g绿矾(FeSO4·7H2O)配制FeSO4溶液,经各步骤后,最终制取得19.52g柠檬酸铁铵,则柠檬酸铁铵的产率为
您最近一年使用:0次
解题方法
3 . 现藏于河北博物院的透雕龙凤纹铜铺首如图所示,是出土于易县燕下都遗址的战国时期燕国的青铜器,其表面铜绿的主要成分为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是
| A.铜能导电,属于电解质 | B. 属于碱 属于碱 |
| C.铜器表面的铜绿可与稀硫酸反应 | D.铜绿受热分解发生氧化还原反应 |
您最近一年使用:0次
4 . 次磷酸 是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
(1)次磷酸中 的化合价为
的化合价为___________ ,画出 的原子结构示意图:
的原子结构示意图:___________ 。
(2)写出 与足量
与足量 溶液反应的化学方程式:
溶液反应的化学方程式:___________ 。
(3)工业上次磷酸 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: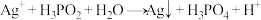 (方程式未配平)
(方程式未配平)
①该反应中___________ (填化学式)被还原。
②配平该反应方程式并标出电子转移的方向和数目:___________ 。
 。
。
③据该反应判断,还原性:___________ >___________ (填化学式)。
④若有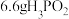 参加该反应,则反应中转移电子的物质的量为
参加该反应,则反应中转移电子的物质的量为___________  。
。
(4)若将氯气通入 溶液中,也发生
溶液中,也发生 的转化,写出该反应的化学方程式:
的转化,写出该反应的化学方程式:___________ 。
 是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:(1)次磷酸中
 的化合价为
的化合价为 的原子结构示意图:
的原子结构示意图:(2)写出
 与足量
与足量 溶液反应的化学方程式:
溶液反应的化学方程式:(3)工业上次磷酸
 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: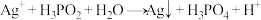 (方程式未配平)
(方程式未配平)①该反应中
②配平该反应方程式并标出电子转移的方向和数目:
 。
。③据该反应判断,还原性:
④若有
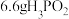 参加该反应,则反应中转移电子的物质的量为
参加该反应,则反应中转移电子的物质的量为 。
。(4)若将氯气通入
 溶液中,也发生
溶液中,也发生 的转化,写出该反应的化学方程式:
的转化,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
5 . 下列反应既是氧化还原反应,又是吸热反应的是
| A.碳和二氧化碳在高温下的反应 | B.碳酸钙高温分解 |
| C.氢氧化钠和盐酸的反应 | D.铝片和稀硫酸反应 |
您最近一年使用:0次
名校
6 . 1828年,德国化学家维勒在制备无机盐氰酸铵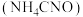 时得到了尿素
时得到了尿素 ,第一次通过人工的方法将无机物转变成有机物,打破了无机物和有机物的界限.下列关于尿素的叙述
,第一次通过人工的方法将无机物转变成有机物,打破了无机物和有机物的界限.下列关于尿素的叙述不正确 的是
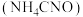 时得到了尿素
时得到了尿素 ,第一次通过人工的方法将无机物转变成有机物,打破了无机物和有机物的界限.下列关于尿素的叙述
,第一次通过人工的方法将无机物转变成有机物,打破了无机物和有机物的界限.下列关于尿素的叙述| A.尿素是人体新陈代谢的一种产物 | B.尿素与氰酸铵均属于共价化合物 |
| C.尿素与氰酸铵互为同分异构 | D.工业上用氨气和二氧化碳在高温高压下合成尿素的反应是非氧化还原反应 |
您最近一年使用:0次
名校
7 . 某铵盐X不含氧元素,盐X溶液能发生如图所示的转化关系(部分反应的反应条件已略),相对分子质量:c比b大16,f比e大16.下列推断不正确的是

| A.X既含离子键又含共价键 | B.将b通入a的水溶液中可能生成沉淀 |
| C.a、b、c、d、e、f都是极性分子 | D.反应①、②均为氧化还原反应 |
您最近一年使用:0次
名校
解题方法
8 . NaClO2是一种重要的杀菌消毒剂,其一种生产工艺如图:

(1)NaClO2中Cl的化合价为_______ 。
(2)“反应”步骤中的氧化剂是_______。
(3)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O。
①用单线桥表示电子转移方向和数目_______ 。
②此吸收反应中,氧化产物是_______ ,氧化剂与还原剂的物质的量之比为_______ 。
③比较氧化性:ClO2_______ O2(填“>”、“<”或“=”)。
(4)硫代硫酸钠可作为脱氯剂,已知25.0mL0.1mol/LNa2S2O3溶液恰好把224mL(标准状况)Cl2完全转化为Cl-离子,则S2O 将转化成_______。
将转化成_______。
(5)往100mL溴化亚铁溶液中缓慢通入2.24L(标准状况)氯气,反应完成后溶液中有1/4的溴离子被氧化成溴单质。则原溴化亚铁溶液的物质的量浓度为_______ mol·L-1。

(1)NaClO2中Cl的化合价为
(2)“反应”步骤中的氧化剂是_______。
| A.硫酸 | B.SO2 | C.NaClO3 | D.ClO2 |
(3)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O。
①用单线桥表示电子转移方向和数目
②此吸收反应中,氧化产物是
③比较氧化性:ClO2
(4)硫代硫酸钠可作为脱氯剂,已知25.0mL0.1mol/LNa2S2O3溶液恰好把224mL(标准状况)Cl2完全转化为Cl-离子,则S2O
 将转化成_______。
将转化成_______。| A.S2- | B.S | C.SO | D.SO |
(5)往100mL溴化亚铁溶液中缓慢通入2.24L(标准状况)氯气,反应完成后溶液中有1/4的溴离子被氧化成溴单质。则原溴化亚铁溶液的物质的量浓度为
您最近一年使用:0次
解题方法
9 . 下列反应中, 只作为氧化剂的是
只作为氧化剂的是
 只作为氧化剂的是
只作为氧化剂的是A. | B. |
C. | D. |
您最近一年使用:0次
2024-03-29更新
|
169次组卷
|
2卷引用:2023年6月福建省普通高中学业水平合格性考试化学试题
10 . Ⅰ.氢气是一种绿色能源,我国目前是全球最大的产氢国。
(1)氢元素有1H、2H和3H三种核素,它们含有相同的________。(双选)
| A.中子数 | B.质量数 | C.质子数 | D.核外电子数 |
A.氢分子中含有共价键
B. 氢分子的空间填充模型可表示为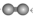
C. 氢气液化时,氢分子间平均距离变小
Ⅱ.“人靠田养,苗靠肥长”,粮食增产离不开氮肥。NH3是制备氮肥的原料之一。
(3)写出NH3的电子式
(4)下列关于 NH3的说法错误的是________。
| A.极易溶于水 | B.可用作制冷剂 | C.属于电解质 | D.属于共价化合物 |
Ⅲ.尿素[CO(NH2)2]是使用量最多的氮肥之一。
(5)尿素属于________。
| A.铵态氮肥 | B.硝态氮肥 | C.有机氮肥 | D.复合肥 |
Ⅳ.氮化硅(Si3N4)陶瓷材料可应用于原子反应堆。氮化硅可由下列反应制得:3SiO2+6C+2N2
 Si3N4+ 6CO,Si3N4中氮元素的化合价为-3。
Si3N4+ 6CO,Si3N4中氮元素的化合价为-3。(7)用单线桥标出上述反应中电子转移的方向和数目
(8)该反应的氧化剂是
(9)若生成0.25mol Si3N4,则反应过程中转移
您最近一年使用:0次



