1 . 某化学兴趣小组同学按图示装置进行实验,产生足量的气体通入c中,最终出现浑浊。下列所选物质组合符合要求的是
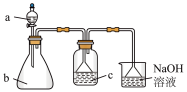
| 选项 | a中试剂 | b中试剂 | c中试剂 | |
| A | 浓硫酸 | 浓盐酸 | 饱和食盐水 | |
| B | 浓硫酸 | Cu |  溶液 溶液 | |
| C | 稀盐酸 | 大理石 |  溶液 溶液 | |
| D | 浓硫酸 | 亚硫酸钠 |  溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 将 9.2g 铜和铁的混合物放入一定体积的稀硝酸溶液中,充分反应后得到标准状况下1.12LNO ,有金属剩余;向所得溶液中继续加入足量的稀硫酸,金属完全溶解且又得到标准状况下1.12LNO 。若向反应后的溶液中加入 KSCN 溶液,溶液不变红,则下列说法中正确的是
| A.原混合物中铜和铁各 0.1mol |
| B.第一次剩余金属全部为铜 |
| C.反应后的溶液中溶质为硝酸亚铁和硝酸铜 |
| D.若向反应后的溶液中再加入足量稀硝酸,又可得到约标准状况下 0.37LNO |
您最近一年使用:0次
解题方法
3 . 根据实验操作及现象所得结论错误的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向氨水中滴加酚酞溶液,溶液变红 | 氨水显碱性 |
| B | 向浓硝酸中加入铜片,产生红棕色气体 | 浓硝酸具有强氧化性 |
| C | 向蔗糖中滴加浓硫酸,蔗糖变黑 | 浓硫酸具有吸水性 |
| D | 向品红溶液中通入 ,溶液褪色 ,溶液褪色 |  具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . I、回答下列问题
(1)以太阳能为热源,利用纳米级 可获得氢气,过程如图所示,整个过程的催化剂为
可获得氢气,过程如图所示,整个过程的催化剂为___________ (填名称);过程I的化学方程式为___________ ;反应中生成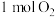 ,则同时生成
,则同时生成
___________ L(标准状况下)。
(2)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为___________ 。
②装置A中发生反应的化学方程式为___________ ;装置B的作用为___________ 。
③装置D中的现象为___________ ;C中盛放的试剂为___________ 。
(3)在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为___________ 。
(1)以太阳能为热源,利用纳米级
 可获得氢气,过程如图所示,整个过程的催化剂为
可获得氢气,过程如图所示,整个过程的催化剂为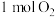 ,则同时生成
,则同时生成

(2)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
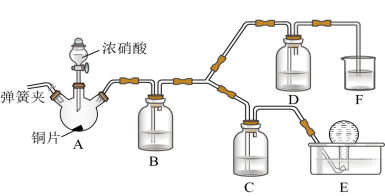
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为
②装置A中发生反应的化学方程式为
③装置D中的现象为
(3)在碱性条件下,
 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为
您最近一年使用:0次
解题方法
5 . 氮氧化物(NOx)是大气污染物之一,处理工业废气中的NOx对于环境保护具有重要的意义。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。_______ ;装置B内的试剂是______ 。
②装置D中发生反应的离子方程式是_______ ,铜丝可抽动的优点是________ 。
③在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,该反应中NH3和NO2的物质的量之比为______ 。
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O。
用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图(α表示NOx中NO2的含量):_____ ,c(NaOH)=_____ 。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。

②装置D中发生反应的离子方程式是
③在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,该反应中NH3和NO2的物质的量之比为
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O。
用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图(α表示NOx中NO2的含量):

您最近一年使用:0次
解题方法
6 . 某化学小组按下图所示实验流程比较浓硝酸和稀硝酸的氧化性强弱,其中B为一种紫红色金属,C为红棕色气体。
(1)A与B反应的化学方程式是_________________________ ;A与B反应迅速,实验中需要采取措施控制气体放出的快慢及多少,则装置I可以选择的装置为_________________________ 。 气体,该操作的目的是
气体,该操作的目的是___________ 。
(3)装置Ⅱ中发生反应的化学方程式是_______________ 。
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸______________ (填“强”或“弱”),判断的依据是___________________ 。

(1)A与B反应的化学方程式是

 气体,该操作的目的是
气体,该操作的目的是(3)装置Ⅱ中发生反应的化学方程式是
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸
您最近一年使用:0次
解题方法
7 . 实践中一些反应器内壁的污垢。可选用针对性的试剂溶解除去。下表中污垢处理试剂的选用,能达到目的且符合安全环保理念的是
| 选项 | A | B | C | D |
| 污垢 | 银镜反应的银垢 | 锅炉内的石膏垢 | 石化设备内的硫垢 | 皂化反应器材表面的油渍 |
| 试剂 | 稀硝酸溶液 | 饱和Na2SO4溶液; 5%柠檬酸溶液 | 5%NaOH溶液; 3%H2O2溶液 | 苯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列做法错误的是
| A.用聚四氟乙烯塑料瓶储存氢氟酸 |
| B.用氨水去除试管内壁附着的银镜 |
C.检验 是否被氧化时,先加足量盐酸再加 是否被氧化时,先加足量盐酸再加 溶液 溶液 |
| D.铝热反应非常剧烈,操作时戴上石棉手套和护目镜 |
您最近一年使用:0次
名校
9 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 可用 坩埚熔融NaOH固体 坩埚熔融NaOH固体 |  的熔点高 的熔点高 |
| B | 将浓硫酸加入蔗糖中形成多孔炭 | 浓硫酸具有氧化性和脱水性 |
| C | 可用稀硝酸制备 | 硝酸的酸性比 的酸性强 的酸性强 |
| D | 装有 的密闭烧瓶冷却后气体颜色变浅 的密闭烧瓶冷却后气体颜色变浅 |  转化为 转化为 的反应吸热 的反应吸热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下列实验的设计、现象和结论对应正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 在稀H2SO4中加入少量Cu2O(s) | 溶液由无色变为蓝色并有红色固体生成 | 反应中Cu2O既作氧化剂又作还原剂 |
| B | 向可能含苯酚的苯中加入适量浓溴水 | 未出现白色沉淀 | 说明苯中不含有苯酚 |
| C | 加热浓硝酸,并将产生的气体通入淀粉-KI溶液中 | 溶液变蓝 | 浓硝酸分解产生NO2 |
| D | 向Al2(SO4)3溶液和CaCl2溶液中分别加入Na2CO3溶液 | 均出现白色沉淀 | Al2(SO4)3溶液和CaCl2溶液均可使 的水解平衡正向移动 的水解平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



