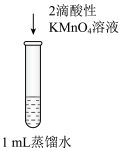
1 . 小组同学探究 与水的反应。
与水的反应。
在注射器中充入 ,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。
,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。_______ 。
(2)进一步探究无色气体增多的原因。
【查阅资料】
ⅰ. 与水反应:
与水反应: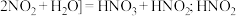 不稳定,分解产生气体。
不稳定,分解产生气体。
ⅱ. 能与KI反应生成
能与KI反应生成 。
。
【提出猜想】溶液A中含有 。
。
【进行实验】
①实验Ⅰ的目的是_______ 。
②实验Ⅱ中选择 溶液的依据是
溶液的依据是_______ (填字母)。
a. 具有氧化性,
具有氧化性, 具有还原性
具有还原性
b. 溶液有颜色,反应前后溶液颜色有变化
溶液有颜色,反应前后溶液颜色有变化
③甲同学认为,实验Ⅲ不能证明溶液A中含有 ,理由是
,理由是_______ 。
【实验反思】
本实验条件下, 与水反应生成了
与水反应生成了 ;
; 分解产生气体,且速率较小。
分解产生气体,且速率较小。
 与水的反应。
与水的反应。在注射器中充入
 ,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。
,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。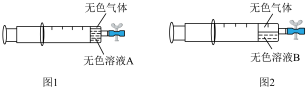
(2)进一步探究无色气体增多的原因。
【查阅资料】
ⅰ.
 与水反应:
与水反应: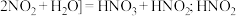 不稳定,分解产生气体。
不稳定,分解产生气体。ⅱ.
 能与KI反应生成
能与KI反应生成 。
。【提出猜想】溶液A中含有
 。
。【进行实验】
实验序号 | Ⅰ | Ⅱ | Ⅲ |
实验操作 |
|
|
|
实验现象 | 液体颜色变为浅红色 | 溶液颜色仍为无色 | 溶液颜色变为蓝色 |
②实验Ⅱ中选择
 溶液的依据是
溶液的依据是a.
 具有氧化性,
具有氧化性, 具有还原性
具有还原性b.
 溶液有颜色,反应前后溶液颜色有变化
溶液有颜色,反应前后溶液颜色有变化③甲同学认为,实验Ⅲ不能证明溶液A中含有
 ,理由是
,理由是【实验反思】
本实验条件下,
 与水反应生成了
与水反应生成了 ;
; 分解产生气体,且速率较小。
分解产生气体,且速率较小。
您最近一年使用:0次
名校
2 . “变化观念和平衡思想”是高中化学核心素养的重要组成部分,对于下列事实,分析正确的是
| 选项 | 事实 | 分析 |
| A | 高炉炼铁中,增加炉高发现并不能降低尾气中CO含量 | 化学反应是有限度的 |
| B | 密闭容器中反应 达到平衡,缩小容器体积,容器内气体颜色加深 达到平衡,缩小容器体积,容器内气体颜色加深 | 增大压强,该平衡逆向移动 |
| C | 常温下,铜与浓硝酸反应比与稀硝酸反应速率快 | 同一反应,反应物浓度越大,速率越快 |
| D | 反应 (aq,橙色) (aq,橙色) (aq,黄色) (aq,黄色)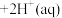 平衡后,升温溶液橙色减弱,黄色加深 平衡后,升温溶液橙色减弱,黄色加深 | 该反应正反应吸热,升温正反应速率加快,逆反应速率减小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列实验操作正确且能够达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 向某无色溶液中加入铜片和稀硫酸,观察试管口是否有红棕色气体出现 | 检验该无色溶液中是否存在 |
| B | 将酒精与碘水在分液漏斗中充分振荡混匀、静置 | 萃取 单质 单质 |
| C | 将澄清石灰水滴入可能混有 的 的 溶液中,观察是否产生白色沉淀 溶液中,观察是否产生白色沉淀 | 检验是否存在 |
| D | 将 固体溶于适量浓盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的铁粉 固体溶于适量浓盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的铁粉 | 配制 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 简要回答下列问题
(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:___________ 。
(2)写出Cu在Cl2中燃烧的化学方程式:___________ 。
(3)如何用化学方法辨别溶液中是否含氯离子:___________ 。
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是______ (用化学方程式表示)。

(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:
(2)写出Cu在Cl2中燃烧的化学方程式:
(3)如何用化学方法辨别溶液中是否含氯离子:
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是
您最近一年使用:0次
5 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确 的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究 和浓 和浓 反应后溶液呈绿色的原因 反应后溶液呈绿色的原因 | 将 通入下列溶液至饱和: 通入下列溶液至饱和:①浓  ②  和HNO3,混合溶液 和HNO3,混合溶液 | ①无色变黄色 ②蓝色变绿色 |  和浓 和浓 反应后溶液呈绿色的主要原因是溶有 反应后溶液呈绿色的主要原因是溶有 |
| B | 比较 与 与 结合 结合 的能力 的能力 | 向等物质的量浓度的 和 和 混合溶液中滴加几滴 混合溶液中滴加几滴 溶液,振荡 溶液,振荡 | 溶液颜色无明显变化 | 结合 的能力: 的能力: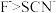 |
| C | 比较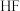 与 与 的酸性 的酸性 | 分别测定等物质的量浓度的 与 与 溶液的 溶液的 | 前者 小 小 | 酸性: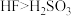 |
| D | 探究温度对反应速率的影响 | 等体积、等物质的量浓度的 与 与 溶液在不同温度下反应 溶液在不同温度下反应 | 温度高的溶液中先出现浑浊 | 温度升高,该反应速率加快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-02更新
|
2801次组卷
|
5卷引用:浙江省余姚中学2023-2024学年高二下学期3月质量检测化学试题
浙江省余姚中学2023-2024学年高二下学期3月质量检测化学试题山东省青岛一中2023-2024学年高二下学期第二次月考化学试卷 2024年浙江高考真题化学(1月)(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)选择题11-16
6 . Ⅰ.无水 与
与 作用会生成
作用会生成 。现有
。现有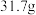 无水
无水 ,吸收
,吸收 后变成
后变成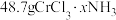 ,试回答下列问题:
,试回答下列问题:
(1) 中
中
______ 。
(2) 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到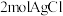 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为______ 。
Ⅱ.将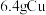 溶于
溶于 过量的硝酸溶液中,假设硝酸的还原产物只有
过量的硝酸溶液中,假设硝酸的还原产物只有 和
和 。反应结束后,将所得的溶液加水稀释至
。反应结束后,将所得的溶液加水稀释至 ,测得
,测得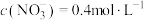 。(假设生成气体完全逸出)。请计算:
。(假设生成气体完全逸出)。请计算:
(3)稀释后溶液中 的物质的量浓度
的物质的量浓度______ 
(4)生成的气体中 物质的量
物质的量______  (用含有
(用含有 的表达式表示)
的表达式表示)
 与
与 作用会生成
作用会生成 。现有
。现有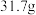 无水
无水 ,吸收
,吸收 后变成
后变成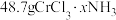 ,试回答下列问题:
,试回答下列问题:(1)
 中
中
(2)
 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到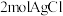 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为Ⅱ.将
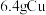 溶于
溶于 过量的硝酸溶液中,假设硝酸的还原产物只有
过量的硝酸溶液中,假设硝酸的还原产物只有 和
和 。反应结束后,将所得的溶液加水稀释至
。反应结束后,将所得的溶液加水稀释至 ,测得
,测得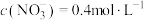 。(假设生成气体完全逸出)。请计算:
。(假设生成气体完全逸出)。请计算:(3)稀释后溶液中
 的物质的量浓度
的物质的量浓度
(4)生成的气体中
 物质的量
物质的量 (用含有
(用含有 的表达式表示)
的表达式表示)
您最近一年使用:0次
名校
解题方法
7 . 铜与硝酸反应的装置如图所示,实验步骤如下:
步骤1:向试管 中加入
中加入 浓硝酸,塞上带有铜丝的橡胶塞。观察到铜丝逐渐变细,溶液变绿,试管
浓硝酸,塞上带有铜丝的橡胶塞。观察到铜丝逐渐变细,溶液变绿,试管 中充满红棕色气体。
中充满红棕色气体。
步骤2:一段时间后,试管 中反应变平缓,溶液逐渐变成蓝色,同时气体颜色从下方开始变浅,最终变成无色。
中反应变平缓,溶液逐渐变成蓝色,同时气体颜色从下方开始变浅,最终变成无色。
步骤3:反应停止后,用注射器向试管 中注入少量稀硫酸,铜丝继续溶解,产生无色气体。
中注入少量稀硫酸,铜丝继续溶解,产生无色气体。不正确 的是
步骤1:向试管
 中加入
中加入 浓硝酸,塞上带有铜丝的橡胶塞。观察到铜丝逐渐变细,溶液变绿,试管
浓硝酸,塞上带有铜丝的橡胶塞。观察到铜丝逐渐变细,溶液变绿,试管 中充满红棕色气体。
中充满红棕色气体。步骤2:一段时间后,试管
 中反应变平缓,溶液逐渐变成蓝色,同时气体颜色从下方开始变浅,最终变成无色。
中反应变平缓,溶液逐渐变成蓝色,同时气体颜色从下方开始变浅,最终变成无色。步骤3:反应停止后,用注射器向试管
 中注入少量稀硫酸,铜丝继续溶解,产生无色气体。
中注入少量稀硫酸,铜丝继续溶解,产生无色气体。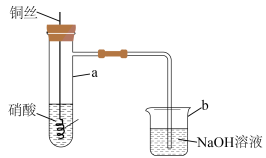
A.步骤1观察到试管 中充满红棕色气体,说明铜和浓硝酸反应生成 中充满红棕色气体,说明铜和浓硝酸反应生成 |
| B.步骤2观察到反应变平缓而且气体颜色从下方开始变浅,说明浓硝酸已经变成稀硝酸 |
C.步骤3固体继续溶解,说明此时 被 被 氧化 氧化 |
D.相对于步骤2,步骤1中溶液显绿色可能是 溶解在硝酸铜中所致 溶解在硝酸铜中所致 |
您最近一年使用:0次
2024-01-29更新
|
250次组卷
|
2卷引用:江苏省南通市海安市2023-2024学年高二上学期1月期末化学试题
名校
解题方法
8 . 下列有关说法不正确的是
| A.高压钠灯透雾能力强,是因为Na的金属性非常强 |
| B.铜片溶于稀硝酸,体现了稀硝酸的强氧化性和酸性 |
| C.Si可用作光电池,是因为Si为一种半导体材料 |
| D.明矾可净水,是因为A13+发生水解形成了胶体 |
您最近一年使用:0次
2024-01-09更新
|
78次组卷
|
2卷引用:广东省东莞市东莞中学2023-2024学年高二上学期期中考试化学试题
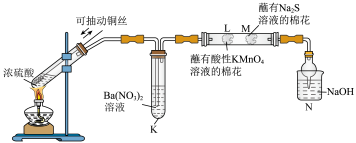
9 . 为探究 的相关性质,某课外小组的同学设计如图所示装置进行实验(省略部分夹持装置)。下列实验事实与结论正确的是
的相关性质,某课外小组的同学设计如图所示装置进行实验(省略部分夹持装置)。下列实验事实与结论正确的是
 的相关性质,某课外小组的同学设计如图所示装置进行实验(省略部分夹持装置)。下列实验事实与结论正确的是
的相关性质,某课外小组的同学设计如图所示装置进行实验(省略部分夹持装置)。下列实验事实与结论正确的是
| 选项 | 实验事实 | 解释 |
| A | K处试管中有白色沉淀生成 | 白色沉淀为 |
| B | L处蘸有酸性 溶液的棉花褪色 溶液的棉花褪色 |  具有漂白性 具有漂白性 |
| C | M处蘸有 溶液的棉花上出现黄色固体 溶液的棉花上出现黄色固体 |  具有氧化性 具有氧化性 |
| D | N中滴有酚酞的NaOH溶液褪色 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 氮元素以 分子形式存在于空气中,通过化学方法可将其转变为人类需要的各种氮肥(如
分子形式存在于空气中,通过化学方法可将其转变为人类需要的各种氮肥(如 、
、 )和其他含氮化合物(如
)和其他含氮化合物(如 、
、 )。N、P、K是植物生长必需的营养元素;K与Na都位于元素周期表ⅠA族K位于Na的下一周期都可与水发生反应。下列反应的离子方程式正确的是
)。N、P、K是植物生长必需的营养元素;K与Na都位于元素周期表ⅠA族K位于Na的下一周期都可与水发生反应。下列反应的离子方程式正确的是
 分子形式存在于空气中,通过化学方法可将其转变为人类需要的各种氮肥(如
分子形式存在于空气中,通过化学方法可将其转变为人类需要的各种氮肥(如 、
、 )和其他含氮化合物(如
)和其他含氮化合物(如 、
、 )。N、P、K是植物生长必需的营养元素;K与Na都位于元素周期表ⅠA族K位于Na的下一周期都可与水发生反应。下列反应的离子方程式正确的是
)。N、P、K是植物生长必需的营养元素;K与Na都位于元素周期表ⅠA族K位于Na的下一周期都可与水发生反应。下列反应的离子方程式正确的是A.K与水反应: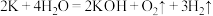 |
B.Cu与稀 反应: 反应: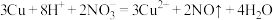 |
C.少量 通入氨水中: 通入氨水中: |
D.氯化铵溶液与澄清石灰水混合加热: |
您最近一年使用:0次