1 . 下图的每一方格中表示有关的一种反应物或生成物,其中A、C、D、E为无色气体,F为红棕色气体。下列说法错误的是
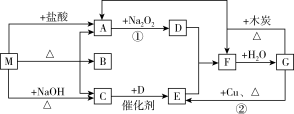
| A.D在一定条件下可以与C发生置换反应 |
| B.用蘸有浓盐酸的玻璃棒靠近瓶口可以检验C气体是否收集满 |
| C.M可能是纯净物或混合物 |
| D.F与水的反应中氧化剂与还原剂的物质的量之比为2∶1 |
您最近一年使用:0次
名校
2 . “增蓝天,保碧水,护净土”,江苏省正加快推进生态环境治理现代化建设。下列叙述正确的是
| A.推广使用煤气化和液化技术,获得清洁燃料和化工原料 |
| B.在一定条件下,选择合适的催化剂将CO2氧化为甲酸 |
| C.铵态氮肥使用时要深施覆土,是因为铵态氮肥易氧化变质 |
| D.纳米铁粉可以通过吸附作用高效地除去被污染水体中的Cu2+、Ag+等重金属离子 |
您最近一年使用:0次
2023-05-22更新
|
473次组卷
|
2卷引用:2023年第37届中国化学奥林匹克竞赛(江苏赛区)初赛试题
3 . 氮及其化合物是我们熟悉的典型非金属元素及化合物,研究它们的性质对于生产、生活、科研具有重要意义,请回答以下问题:
(1)下图为制取氨气的装置和选用的试剂,其中错误的是_______ (填字母)。
A.①② B.②③ C.③④ D.①③
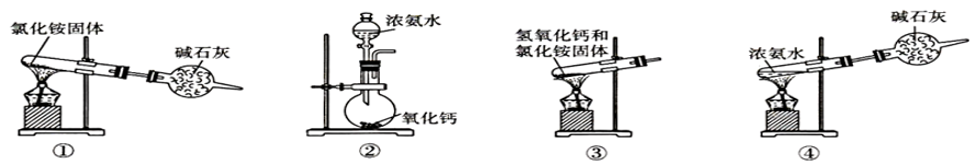
(2)实验室制备氨气的化学反应方程式是_______ ,为了得到干燥的NH3,可用_______ 做干燥剂。若有5.35g氯化铵参加反应,则产生的气体在标准状况下的体积为_______ L。
(3)铵盐受热易分解,如图所示。
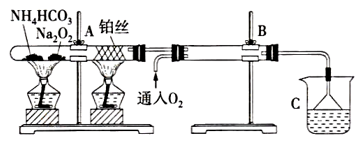
被加热的铂丝处发生反应的化学方程式为_______ 。
(1)下图为制取氨气的装置和选用的试剂,其中错误的是
A.①② B.②③ C.③④ D.①③

(2)实验室制备氨气的化学反应方程式是
(3)铵盐受热易分解,如图所示。

被加热的铂丝处发生反应的化学方程式为
您最近一年使用:0次
4 . 工业制硫酸吸收塔排出的尾气需要处理才能排放到大气中,其处理方法为:先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。
为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
部分测定结果:
铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
请计算:
(1)该铵盐中氮元素的质量分数是____ %。
(2)若铵盐质量为15.00g,浓硫酸增加的质量为____ 。(计算结果保留两位小数)
为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
部分测定结果:
铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
请计算:
(1)该铵盐中氮元素的质量分数是
(2)若铵盐质量为15.00g,浓硫酸增加的质量为
您最近一年使用:0次
5 . 已知:A为正盐,常温、常压下,B、C、D、E、G、H、I均为气体,其中D、G、H为单质,气体B能使湿润红色石蕊试纸变蓝,气体E本身为无色气体,但是与空气接触会生成一种红棕色气体I,H为黄绿色气体。F在常温下是一种无色液体。C、J的水溶液分别为两种强酸。图中反应条件(除加热外)均已略去。
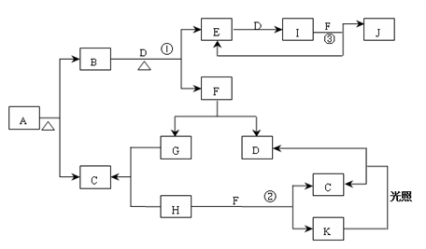
⑴写出它们的化学式: A________ 、C________ 、J________ ;
⑵实验室制备气体B的化学反应方程式为______ ;
⑶写出B+D→E+F的化学反应方程式:______ ;
⑷ J的浓溶液与单质Ag反应的离子方程式为:______ ;

⑴写出它们的化学式: A
⑵实验室制备气体B的化学反应方程式为
⑶写出B+D→E+F的化学反应方程式:
⑷ J的浓溶液与单质Ag反应的离子方程式为:
您最近一年使用:0次



