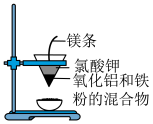
1 . 金属铝质轻且具有良好的抗腐蚀性,在日常生活与工业生产中有非常重要的作用。请回答下列问题:
(1)31号元素镓(Ga)与铝同主族。镓的原子结构示意图为___________ ,写出金属镓与盐酸反应的化学方程式:___________ 。铍的单质、化合物与铝的单质、化合物分别具有相似的化学性质,写出 溶液与过量NaOH溶液反应的离子方程式:
溶液与过量NaOH溶液反应的离子方程式:___________ 。
(2)人类最早使用的金属材料的主要成分是铜。下列说法中正确的是___________(填字母)。
(3)向稀 溶液中加入适量
溶液中加入适量 溶液至
溶液至 恰好完全沉淀,此时铝元素的存在形式主要为(用化学式表示)
恰好完全沉淀,此时铝元素的存在形式主要为(用化学式表示)___________ 。
(4)某同学对铝与 发生铝热反应的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。
发生铝热反应的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。
①上述置换反应的化学方程式为___________ 。
②该同学推测铝热反应得到的熔融物中还含有 ,他设计了如下方案来验证:取一块该熔融物,冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含
,他设计了如下方案来验证:取一块该熔融物,冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含 。该同学的实验方案是否合理?
。该同学的实验方案是否合理?___________ (填“合理”或“不合理”)。理由是___________ 。
(1)31号元素镓(Ga)与铝同主族。镓的原子结构示意图为
 溶液与过量NaOH溶液反应的离子方程式:
溶液与过量NaOH溶液反应的离子方程式:(2)人类最早使用的金属材料的主要成分是铜。下列说法中正确的是___________(填字母)。
| A.青铜和黄铜均是合金 | B.铜表面易形成致密的氧化膜 |
C.铜绿[ ]属于碱式盐 ]属于碱式盐 | D.金属铜能与 溶液发生置换反应 溶液发生置换反应 |
 溶液中加入适量
溶液中加入适量 溶液至
溶液至 恰好完全沉淀,此时铝元素的存在形式主要为(用化学式表示)
恰好完全沉淀,此时铝元素的存在形式主要为(用化学式表示)(4)某同学对铝与
 发生铝热反应的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。
发生铝热反应的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。①上述置换反应的化学方程式为
②该同学推测铝热反应得到的熔融物中还含有
 ,他设计了如下方案来验证:取一块该熔融物,冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含
,他设计了如下方案来验证:取一块该熔融物,冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含 。该同学的实验方案是否合理?
。该同学的实验方案是否合理?
您最近一年使用:0次
2 . 下列实验装置能达到实验目的的是
| 选项 | A | B |
| 实验装置 |
|
|
| 目的 | 制备氢氧化铁胶体 | 铝热反应 |
| 选项 | C | D |
| 实验装置 |
|
|
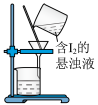
| 目的 | 分离含碘的悬浊液 | 测定氯水的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 铝及其合金是生产生活中常用的一种金属材料。
(1)铝合金用于加工门窗,是因为其硬度比纯金属___________ (填“大”或“小”)。
(2)生活中不宜用铝制品盛装碱性溶液,某同学在实验中模拟该过程,将一块铝箔投入过量 溶液中,观察到的实验现象为:
溶液中,观察到的实验现象为:___________ ,其中涉及到的离子方程式为:___________ 、___________ 。
(3)工业上常利用金属Al与 在高温下反应冶炼金属Fe,该反应的化学方程式为
在高温下反应冶炼金属Fe,该反应的化学方程式为___________ ,将可以恰好完全发生该反应的Al与 均匀混合,分成两等份,一份先完全发生该反应,反应产物再与足量盐酸反应,另一份直接与足量
均匀混合,分成两等份,一份先完全发生该反应,反应产物再与足量盐酸反应,另一份直接与足量 溶液反应,生成气体在相同条件下体积比为
溶液反应,生成气体在相同条件下体积比为___________ 。
(1)铝合金用于加工门窗,是因为其硬度比纯金属
(2)生活中不宜用铝制品盛装碱性溶液,某同学在实验中模拟该过程,将一块铝箔投入过量
 溶液中,观察到的实验现象为:
溶液中,观察到的实验现象为:(3)工业上常利用金属Al与
 在高温下反应冶炼金属Fe,该反应的化学方程式为
在高温下反应冶炼金属Fe,该反应的化学方程式为 均匀混合,分成两等份,一份先完全发生该反应,反应产物再与足量盐酸反应,另一份直接与足量
均匀混合,分成两等份,一份先完全发生该反应,反应产物再与足量盐酸反应,另一份直接与足量 溶液反应,生成气体在相同条件下体积比为
溶液反应,生成气体在相同条件下体积比为
您最近一年使用:0次
解题方法
4 . 下列物质制备方法可用于大规模工业生产的是
| A.铝与氧化铁发生置换反应制铁 |
| B.加热分解氯化钠制金属钠和氯气 |
| C.硫黄与空气中的氧气反应制二氧化硫 |
| D.金属钾与熔融氯化钠反应制金属钠 |
您最近一年使用:0次
5 . 下列选项所示的物质间转化不能实现的是
A.NaCl(aq)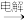 Cl2 Cl2 漂白液 漂白液 |
B.Cu2S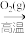 SO2(g) SO2(g) H2SO4 H2SO4 |
C.Fe2O3 Fe Fe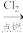 FeCl3 FeCl3 |
D.CO2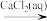 CaCO3 CaCO3 CaO(s) CaO(s) |
您最近一年使用:0次
解题方法
6 . 劳动创造美好生活,下列劳动项目与所述化学知识没有关联的是
| 选项 | 劳动项目 | 化学知识 |
| A | 用洁厕灵清洗马桶 | 含氯化合物具有杀菌消毒功能 |
| B | 焊接两根铁棒 | 铝粉与氧化铁发生的铝热反应 |
| C | 用卤水点热豆浆制豆腐 | 卤水中的电解质能使豆浆胶体聚沉 |
| D | 宣传废旧电池分类回收 | 电池中重金属可造成土壤和水体污染 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 下列基于事实做出的分析不正确 的是
A. 与Al发生铝热反应的条件为高温,说明该反应需吸收能量 与Al发生铝热反应的条件为高温,说明该反应需吸收能量 |
B.反应 在高温时才能自发进行,说明该反应熵变 在高温时才能自发进行,说明该反应熵变 |
| C.碳酸氢钠稀溶液与稀盐酸混合后溶液温度降低,说明该反应需吸收能量 |
| D.某浓度碳酸钠溶液升温时pH减小,说明水的电离程度比碳酸根离子的水解程度增大得更多 |
您最近一年使用:0次
2024-03-12更新
|
48次组卷
|
2卷引用:浙江省强基联盟2023-2024学年高二上学期12月月考化学试题
解题方法
8 . 铝是一种重要金属,从铝土矿(主要成分为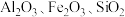 等)中冶炼Al的工业生产流程如下图:
等)中冶炼Al的工业生产流程如下图:
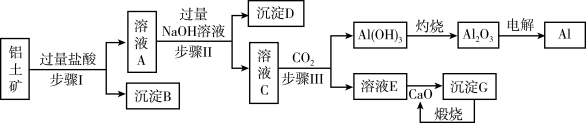
(1)写出步骤Ⅱ生成溶液C 的离子方程式___________ ,步骤I、Ⅱ、Ⅲ都要用到的分离方法是___________ 。
(2)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:___________ 。
(3)CO2中心原子的杂化方式为___________ ,VSEPR 模型为___________ 。
 等)中冶炼Al的工业生产流程如下图:
等)中冶炼Al的工业生产流程如下图:
(1)写出步骤Ⅱ生成溶液C 的离子方程式
(2)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:
(3)CO2中心原子的杂化方式为
您最近一年使用:0次
名校
解题方法
9 . 如图所示:①~⑩分别代表有关反应中的一种物质,它们均为常见物质。已知①~⑤和⑥~⑩中分别含有同一种元素。试回答下列问题:
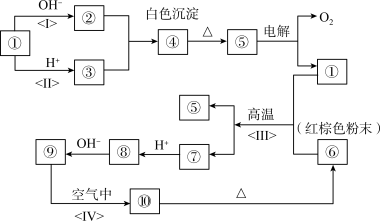
(1)写出指定物质的化学式:④_______ ;⑥_______ ;
(2)写出反应(Ⅲ)的化学方程式_______ ;指出该反应的重要用途之一:_______ ;
(3)写出反应(Ⅰ)的离子方程式_______ ;
(4)反应(Ⅳ)的主要实验现象是_______ ;该反应的化学方程式为:_______ 。

(1)写出指定物质的化学式:④
(2)写出反应(Ⅲ)的化学方程式
(3)写出反应(Ⅰ)的离子方程式
(4)反应(Ⅳ)的主要实验现象是
您最近一年使用:0次
名校
解题方法
10 . 下列“类推”合理的是
| 已知 | 类推 | |
| A | 工业制 : :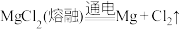 | 工业制 : : |
| B | 将 加入 加入 溶液中: 溶液中: | 将 加入 加入 溶液中: 溶液中: |
| C | 将 加入盐酸中: 加入盐酸中: | 将 加入 加入 溶液中: 溶液中: |
| D |  和 和 发生铝热反应: 发生铝热反应: |  和 和 发生铝热反应: 发生铝热反应: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次