解题方法
1 . 富马酸亚铁(结构简式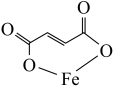 ,刚对分子质量170)是治疗贫血药物的一种。实验制备富马酸亚铁并测其产品中富马酸亚铁的质量分数。
,刚对分子质量170)是治疗贫血药物的一种。实验制备富马酸亚铁并测其产品中富马酸亚铁的质量分数。
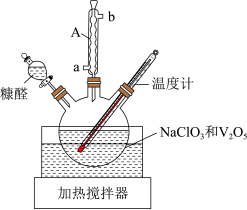
Ⅰ.富马酸( )的制备。制取装置如图所示(夹持仪器已略去),按如图装置打开分液漏斗活塞,滴加糠醛(
)的制备。制取装置如图所示(夹持仪器已略去),按如图装置打开分液漏斗活塞,滴加糠醛(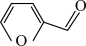 ),在90~100℃条件下层续加热2~3h。
),在90~100℃条件下层续加热2~3h。
Ⅱ.富马酸亚铁的制备
步骤1:将4.64 g富马酸置于100 mL烧杯中,加水20 mL,在热沸搅拌下加入
 溶液10 mL,使其pH为6.5~6.7;
溶液10 mL,使其pH为6.5~6.7;步骤2:将上述溶液转移至如图所示的装置中,缓慢加入40 mL 2 mol⋅L

 溶液,维持温度100℃,充分搅拌1.5 h;
溶液,维持温度100℃,充分搅拌1.5 h;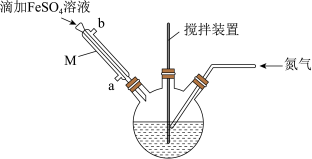
(2)在回流过程中一直通入氮气的目的是
(3)步骤1控制溶液pH为6.5~6.7;若反应后溶液的pH太小;则引起的后果是
Ⅲ.产品纯度测定
步骤①:准确称取粗产品0.1600 g,加煮沸过的3 mol⋅L

 溶液15 mL,待样品完全溶解后,加煮沸过的冷水50 mL和4滴邻二氮菲-亚铁指示剂,立即用0.0500 mol⋅L
溶液15 mL,待样品完全溶解后,加煮沸过的冷水50 mL和4滴邻二氮菲-亚铁指示剂,立即用0.0500 mol⋅L
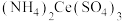 (硫酸高铈铵)标准溶液进行滴定。用去标准液的体积为16.82 mL(反应式为
(硫酸高铈铵)标准溶液进行滴定。用去标准液的体积为16.82 mL(反应式为 ),
),步骤②:不加产品,重复步骤①操作,滴定终点用去标准液0.02 mL。
(4)
(5)产品中富马酸亚铁的质量分数为
您最近半年使用:0次
解题方法
2 . 下列装置或试剂合理且能达到实验目的的是
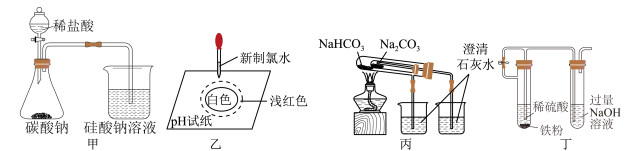
A.用装置甲可以证明非金属性强弱: |
B.乙实验说明新制氯水中含有 和 和 |
C.装置丙可以用于比较 和 和 的热稳定性 的热稳定性 |
| D.装置丁能较长时间观察到有白色沉淀生成 |
您最近半年使用:0次
3 . 东莨菪内酯( )具有镇痛、抗炎、祛痰、平喘的作用。东莨菪内酯为淡黄色固体,熔点
)具有镇痛、抗炎、祛痰、平喘的作用。东莨菪内酯为淡黄色固体,熔点 ,微溶于水和冷乙醇、溶于热乙醇或热冰醋酸、几乎不溶于苯,其主要从丁公藤、杭白芷等植物中提取。一种利用丁公藤提取东莨菪内酯的实验步骤如下:
,微溶于水和冷乙醇、溶于热乙醇或热冰醋酸、几乎不溶于苯,其主要从丁公藤、杭白芷等植物中提取。一种利用丁公藤提取东莨菪内酯的实验步骤如下:
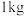 ,粉碎,加入70%乙醇,常温超声波提取30min,过滤得提取液;
,粉碎,加入70%乙醇,常温超声波提取30min,过滤得提取液;ⅱ.减压蒸馏:将提取液减压蒸馏回收乙醇,浓缩得到浸膏;蒸馏装置如图所示;
 碳酸钠溶液分散,用苯萃取体系中的有机物杂质,保留水相;
碳酸钠溶液分散,用苯萃取体系中的有机物杂质,保留水相;ⅳ.酸还原沉淀:将上述水相加盐酸酸化至
 为6,析出沉淀,过滤,沉淀物用少量苯洗涤,得到固体;
为6,析出沉淀,过滤,沉淀物用少量苯洗涤,得到固体;ⅴ.提纯:将上述固体加乙醇加热溶解,趁热过滤、静置、冷却结晶,过滤、冷乙醇洗涤,干燥得到产品。回答下列问题:
(1)超声波辅助能使溶剂很快进入原料内部,步骤ⅰ超声波提取的优点为
(2)步骤ⅱ减压蒸馏宜选用
(3)步骤ⅲ浸膏用稍过量的10%碳酸钠溶液分散,发生反应的化学方程式为
 溶液代替
溶液代替 碳酸钠溶液,回答并说明原因:
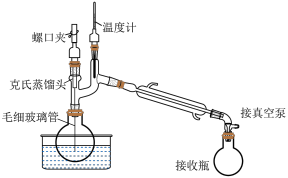
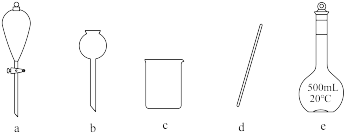
碳酸钠溶液,回答并说明原因:(4)实验室完成步骤ⅲ实验,下列玻璃仪器中必须用到的是
 东莨菪内酯,则该丁公藤样品中东莨菪内酯含量最低为
东莨菪内酯,则该丁公藤样品中东莨菪内酯含量最低为
您最近半年使用:0次
解题方法
4 . 某同学为了获取在 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
Ⅰ.向三颈瓶中加入饱和 溶液,按图示连接装置(夹持装置已略去,气密性已检查);
溶液,按图示连接装置(夹持装置已略去,气密性已检查);
Ⅱ.打开磁力搅拌器,立即加入 溶液;
溶液;
Ⅲ.采集三颈瓶内空气中 体积分数和溶液中
体积分数和溶液中 浓度的数据。
浓度的数据。
实验现象:
三颈瓶中生成白色絮状沉淀,沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:
(1)搅拌的目的是___________ 。
(2)生成白色絮状沉淀的离子方程式为___________ 。
(3)沉淀由白色变为红褐色发生反应的化学方程式为___________ 。
(4)通过上述实验,可得到“在 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是___________ 。
(5)结合上述实验,提出制备 过程中应注意的事项
过程中应注意的事项___________ (回答一项即可)。
 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。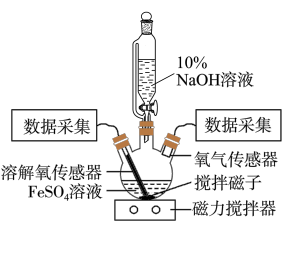
Ⅰ.向三颈瓶中加入饱和
 溶液,按图示连接装置(夹持装置已略去,气密性已检查);
溶液,按图示连接装置(夹持装置已略去,气密性已检查);Ⅱ.打开磁力搅拌器,立即加入
 溶液;
溶液;Ⅲ.采集三颈瓶内空气中
 体积分数和溶液中
体积分数和溶液中 浓度的数据。
浓度的数据。实验现象:
三颈瓶中生成白色絮状沉淀,沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:
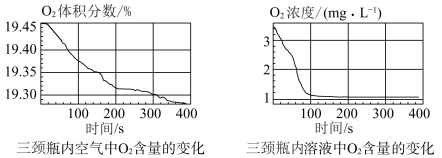
(1)搅拌的目的是
(2)生成白色絮状沉淀的离子方程式为
(3)沉淀由白色变为红褐色发生反应的化学方程式为
(4)通过上述实验,可得到“在
 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是(5)结合上述实验,提出制备
 过程中应注意的事项
过程中应注意的事项
您最近半年使用:0次
解题方法
5 . 某同学设计了如图所示的装置,进行还原铁粉与水蒸气反应的实验。下列说法错误的是
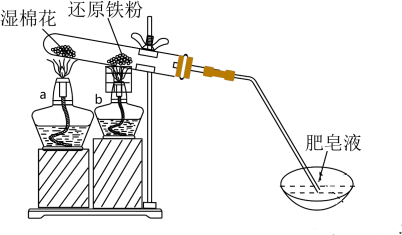
| A.试管中发生的是置换反应 |
| B.湿棉花的作用是提供水蒸气 |
C.点燃酒精灯的顺序是先 后 后 |
| D.加热时试管内生成红色物质,点燃肥皂泡可听到爆鸣声 |
您最近半年使用:0次
名校
6 . 下列为达到实验目的所用实验操作或原理解释存在错误的是
| 实验目的 | 实验操作 | 原理解释 | |
| A | 探究 有氧化性 有氧化性 | 钠在燃烧匙中点燃,迅速伸入盛满 的集气瓶中 的集气瓶中 |  被还原成碳单质 被还原成碳单质 |
| B | 探究硫的酒精溶液属于胶体 | 用激光笔照射硫的酒精溶液 | 硫的酒精溶液中分散质粒子的直径在 之间 之间 |
| C | 除去 酸性溶液中的 酸性溶液中的 | 在加热搅拌的条件下向溶液中加入足量的 固体,过滤后,再向滤液中加入适量的稀盐酸 固体,过滤后,再向滤液中加入适量的稀盐酸 | 溶解度: |
| D | 探究温度对 水解程度的影响 水解程度的影响 | 用 计测 计测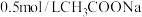 溶液的 溶液的 随温度变化 随温度变化 | 随温度升高,溶液中 水解程度增大 水解程度增大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7 . 用下列实验装置进行相应实验,能 达到实验目的的是

| A.用装置甲除去实验室制取乙烯中混有的少量 SO2 |
| B.用装置乙分离乙酸乙酯与饱和碳酸钠溶液 |
| C.用装置丙将海带灼烧成灰 |
| D.用装置丁可以制备和收集 CO2或 NO |
您最近半年使用:0次
8 . 硫代硫酸钠( )又名次亚硫酸钠、大苏打、海波,主要用于照相业作定影剂,某学习小组用如图装置制备硫代硫酸钠。
)又名次亚硫酸钠、大苏打、海波,主要用于照相业作定影剂,某学习小组用如图装置制备硫代硫酸钠。
①“绿矾”是指 ,高温受热可完全分解得红棕色固体和气体混合物;
,高温受热可完全分解得红棕色固体和气体混合物;
② 熔点-75.5℃,沸点-10℃;
熔点-75.5℃,沸点-10℃; 熔点16.8℃,沸点44.8℃
熔点16.8℃,沸点44.8℃
③硫代硫酸钠( )具有还原性,受热、遇酸易分解。
)具有还原性,受热、遇酸易分解。
请回答下列问题:
Ⅰ.制取硫代硫酸钠( )
)
(1)A装置中发生反应的化学方程式为___________________ 。
(2)检查装置气密性,加入药品。 和
和 混合溶液用煮沸过的蒸馏水配制,煮沸的目的是
混合溶液用煮沸过的蒸馏水配制,煮沸的目的是_______________ ;B装置的作用是_________________ 。
(3)从锥形瓶中得到 晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是
晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是_______________ 。
(4)将一定量的绿矾在500℃时隔绝空气加热一段时间后检验其固体产物,请设计实验证明:此固体产物不含二价铁:__________________ 。
Ⅱ.探究 的性质
的性质
为探究 的性质,小组将装置C换成钡盐溶液,并先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入
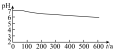
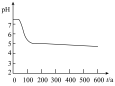
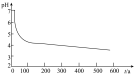
的性质,小组将装置C换成钡盐溶液,并先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入 流速一致。四次实验分别得到如表pH—t图:
流速一致。四次实验分别得到如表pH—t图:
(5)分析pH—t图,写出②中发生反应的离子方程式___________________________ ,上述四次实验中有白色沉淀生成的是__________ (填编号)。
 )又名次亚硫酸钠、大苏打、海波,主要用于照相业作定影剂,某学习小组用如图装置制备硫代硫酸钠。
)又名次亚硫酸钠、大苏打、海波,主要用于照相业作定影剂,某学习小组用如图装置制备硫代硫酸钠。
①“绿矾”是指
 ,高温受热可完全分解得红棕色固体和气体混合物;
,高温受热可完全分解得红棕色固体和气体混合物;②
 熔点-75.5℃,沸点-10℃;
熔点-75.5℃,沸点-10℃; 熔点16.8℃,沸点44.8℃
熔点16.8℃,沸点44.8℃③硫代硫酸钠(
 )具有还原性,受热、遇酸易分解。
)具有还原性,受热、遇酸易分解。请回答下列问题:
Ⅰ.制取硫代硫酸钠(
 )
)(1)A装置中发生反应的化学方程式为
(2)检查装置气密性,加入药品。
 和
和 混合溶液用煮沸过的蒸馏水配制,煮沸的目的是
混合溶液用煮沸过的蒸馏水配制,煮沸的目的是(3)从锥形瓶中得到
 晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是
晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是(4)将一定量的绿矾在500℃时隔绝空气加热一段时间后检验其固体产物,请设计实验证明:此固体产物不含二价铁:
Ⅱ.探究
 的性质
的性质为探究
 的性质,小组将装置C换成钡盐溶液,并先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入
的性质,小组将装置C换成钡盐溶液,并先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入 流速一致。四次实验分别得到如表pH—t图:
流速一致。四次实验分别得到如表pH—t图: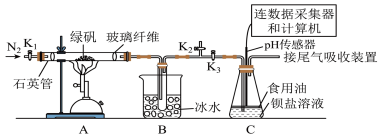
①已煮沸的 (aq) (aq) | ②未煮沸的 (aq) (aq) | ③已煮沸的 (aq) (aq) | ④未煮沸的 (aq) (aq) |
|
|
|
|
(5)分析pH—t图,写出②中发生反应的离子方程式
您最近半年使用:0次
名校
9 . 碘是生物必需的一种微量元素,海带、海藻等食物含碘量最为丰富。某小组通过实验提取并测定干海带中碘的含量。回答下列问题:
Ⅰ.从海带中提取碘。该小组同学按如图实验流程进行实验:___________ (填仪器名称)。___________ (用离子方程式表示)。
Ⅱ.滴定法测海带中碘的含量。
用 滴定
滴定 的水溶液,淀粉溶液作指示剂。原理为:
的水溶液,淀粉溶液作指示剂。原理为: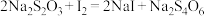 ,
,
(3)用___________ 滴定管(填入酸式或者碱式)量取I2的水溶液。
(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点。
猜想1:碘离子被___________ 氧化;
猜想2:碘离子被步骤iii中过量的 氧化;
氧化;
②验证猜想
③查阅资料 小组同学认为可能是反应速率不同造成的, 氧化I-速率
氧化I-速率___________ (填“快于”或“慢于”) 还原I2的速率,导致待测液反复变为蓝色。
还原I2的速率,导致待测液反复变为蓝色。
④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案___________ 。
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL
 溶液,则干海带中碘的含量为
溶液,则干海带中碘的含量为___________ mg/g(保留2位有效数字)。
Ⅰ.从海带中提取碘。该小组同学按如图实验流程进行实验:

Ⅱ.滴定法测海带中碘的含量。
用
 滴定
滴定 的水溶液,淀粉溶液作指示剂。原理为:
的水溶液,淀粉溶液作指示剂。原理为: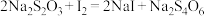 ,
,(3)用
(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点。

猜想1:碘离子被
猜想2:碘离子被步骤iii中过量的
 氧化;
氧化;②验证猜想
| 序号 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量原海带浸出液,加入硫酸酸化,再滴加几滴淀粉溶液,鼓入空气 | 待测液始终保持无色 | 猜想1不成立 |
| 2 | 将2mL0.1mol/L KI溶液、2滴0.1mol/L 溶液、2滴淀粉溶液和1滴0.2mol/L 溶液、2滴淀粉溶液和1滴0.2mol/L 溶液混合配制待测液,用 溶液混合配制待测液,用 溶液滴定 溶液滴定 | 猜想2不成立 |
 氧化I-速率
氧化I-速率 还原I2的速率,导致待测液反复变为蓝色。
还原I2的速率,导致待测液反复变为蓝色。④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL

 溶液,则干海带中碘的含量为
溶液,则干海带中碘的含量为
您最近半年使用:0次
名校
10 . 某化学兴趣小组研究浓硝酸与KSCN溶液的反应。
资料:Ⅰ.SCN‒中S、C、N元素的化合价依次为:-2价、+4价、-3价。
Ⅱ.SCN‒的性质类似卤素离子,能被氧化为(SCN)2,(SCN)2可聚合为红色的(SCN)x。
Ⅲ.NO2可溶于浓硝酸。
(1)实验一:___________ (填化学式)。
(2)实验二:研究SCN‒的转化产物。
a.将实验一ⅲ中的气体通入Ba(OH)2和NaOH的混合溶液中,有白色沉淀生成。
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。
c.另取少量实验一ⅲ中试管内的溶液加入BaCl2溶液,产生大量白色沉淀。
①甲同学根据实验一iii的现象推断SCN‒的氧化产物中一定有NO2,乙同学认为证据不足,理由是___________ 。
②通过b证实了红棕色气体中不含SO2,证据是___________ 。
③由上述实验现象可知:SCN‒转化的最终产物中一定有___________ 。
(3)实验三:研究实验一ⅲ中“静置一段时间后,突然剧烈反应,红色迅速褪去”的原因。丙同学设计了实验三,与实验一进行对比,证实了一定浓度的NO2能加快浓硝酸氧化(SCN)x的化学反应速率。
实验三:___________ 。
②操作2是___________ 。
资料:Ⅰ.SCN‒中S、C、N元素的化合价依次为:-2价、+4价、-3价。
Ⅱ.SCN‒的性质类似卤素离子,能被氧化为(SCN)2,(SCN)2可聚合为红色的(SCN)x。
Ⅲ.NO2可溶于浓硝酸。
(1)实验一:
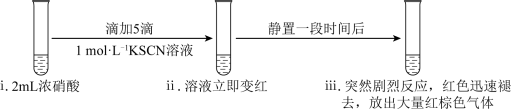
(2)实验二:研究SCN‒的转化产物。
a.将实验一ⅲ中的气体通入Ba(OH)2和NaOH的混合溶液中,有白色沉淀生成。
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。
c.另取少量实验一ⅲ中试管内的溶液加入BaCl2溶液,产生大量白色沉淀。
①甲同学根据实验一iii的现象推断SCN‒的氧化产物中一定有NO2,乙同学认为证据不足,理由是
②通过b证实了红棕色气体中不含SO2,证据是
③由上述实验现象可知:SCN‒转化的最终产物中一定有
(3)实验三:研究实验一ⅲ中“静置一段时间后,突然剧烈反应,红色迅速褪去”的原因。丙同学设计了实验三,与实验一进行对比,证实了一定浓度的NO2能加快浓硝酸氧化(SCN)x的化学反应速率。
实验三:
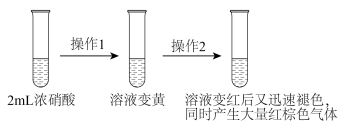
②操作2是
您最近半年使用:0次