碳是形成化合物种类最多的元素,其单质及其部分化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程:
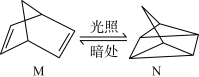 ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是__________ 。
(2)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是________ 。
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
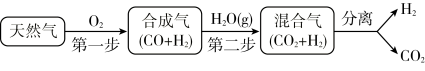
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式___________________________________________________________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程:
 ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是(2)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
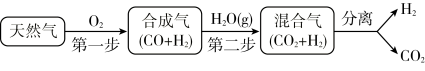
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式
19-20高二上·甘肃甘南·阶段练习 查看更多[5]
湖南省常德外国语学校2020-2021学年高二上学期期中考试化学试题(已下线)1.2+燃烧热++能源-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)第一章 化学反应与能量(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)1.2 燃烧热 能源(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)甘肃省甘南藏族自治州合作第一中学2019-2020学年高二上学期9月月考化学试题
更新时间:2020-04-15 09:09:22
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
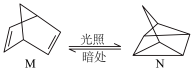
(1)有机物M经过太阳光照可转化成N,转化过程如下,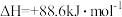 。则M、N相比,较稳定的是
。则M、N相比,较稳定的是_______
(2)已知 (l)的燃烧热为238.6kJ/mol,
(l)的燃烧热为238.6kJ/mol,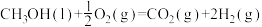
 ,则a
,则a_______ 238.6(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(3)使 和
和 (g)通过灼热的炭层,生成HCl(g)和
(g)通过灼热的炭层,生成HCl(g)和 ,当有1mol
,当有1mol 参与反应时释放出145kJ热量,写出该反应的热化学方程式
参与反应时释放出145kJ热量,写出该反应的热化学方程式_______ 。
(4)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为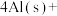
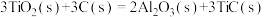
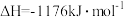 。反应过程中每转移1mol
。反应过程中每转移1mol 放出的热量为
放出的热量为_______ kJ。
(5)已知1mol燃料完全燃烧的数据分别为:
使用上述燃料最能体现“低碳经济”理念的是_______ 。
(6)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM—5催化下合成ETBE,反应的热化学方程式为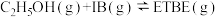
 。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
_______ a ;反应历程的最优途径是
;反应历程的最优途径是
_______ (填“ ”、“
”、“ ”或“
”或“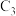 ”)。
”)。
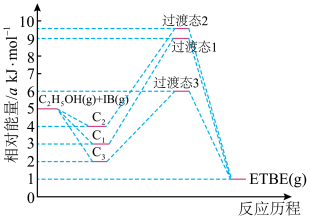
 表示先吸附乙醇,
表示先吸附乙醇, 表示先吸附异丁烯,
表示先吸附异丁烯,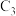 表示乙醇和异丁烯同时吸附
表示乙醇和异丁烯同时吸附
(1)有机物M经过太阳光照可转化成N,转化过程如下,
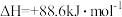 。则M、N相比,较稳定的是
。则M、N相比,较稳定的是
(2)已知
 (l)的燃烧热为238.6kJ/mol,
(l)的燃烧热为238.6kJ/mol,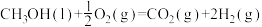
 ,则a
,则a ”、“
”、“ ”或“
”或“ ”)。
”)。(3)使
 和
和 (g)通过灼热的炭层,生成HCl(g)和
(g)通过灼热的炭层,生成HCl(g)和 ,当有1mol
,当有1mol 参与反应时释放出145kJ热量,写出该反应的热化学方程式
参与反应时释放出145kJ热量,写出该反应的热化学方程式(4)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为
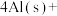
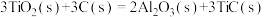
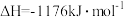 。反应过程中每转移1mol
。反应过程中每转移1mol 放出的热量为
放出的热量为(5)已知1mol燃料完全燃烧的数据分别为:
| 燃料 | 一氧化碳 | 甲烷 | 异辛烷(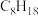 ) ) | 乙醇 |
 | 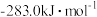 | 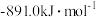 | 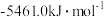 | 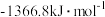 |
(6)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM—5催化下合成ETBE,反应的热化学方程式为
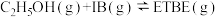
 。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
 ;反应历程的最优途径是
;反应历程的最优途径是
 ”、“
”、“ ”或“
”或“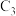 ”)。
”)。
 表示先吸附乙醇,
表示先吸附乙醇, 表示先吸附异丁烯,
表示先吸附异丁烯,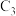 表示乙醇和异丁烯同时吸附
表示乙醇和异丁烯同时吸附
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现代社会的一切活动都离不开能量,所以要更好的关注化学反应中的物质和能量变化。
Ⅰ.已知:P(s,白磷)=P(s,黑磷),每1molP(s,白磷)发生反应,放出39.3kJ的热量,P(s,白磷)=P(s,红磷),每1molP(s,白磷)发生反应,放出17.6kJ的热量。
(1)由此推知,其中最稳定的是_______ (填“黑磷”、“红磷”或“白磷”)。
Ⅱ.在恒容密闭容器中,气体X与气体Y反应可生成气体Z,反应过程中,X、Y、Z的浓度(c)随时间(t)的变化关系如图。
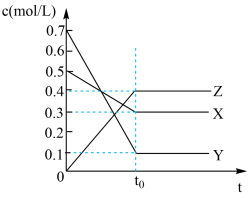
(2)该反应的化学方程式为_______ 。
(3)若t0=10s,用X表示的该反应速率为_______ 。
III.一种新型催化剂用于NO和CO的反应: 。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
(4)a=_______ ,b=_______ 。
(5)能验证温度对化学反应速率规律的是实验_______ (填实验序号)。
Ⅲ.某化学兴趣小组利用原电池原理(如下图所示)探究 的氧化性强于
的氧化性强于 。
。
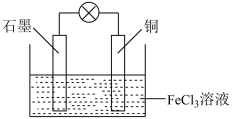
(6)写出该装置的电极反应式。负极:_______ ;正极:_______ 。
Ⅰ.已知:P(s,白磷)=P(s,黑磷),每1molP(s,白磷)发生反应,放出39.3kJ的热量,P(s,白磷)=P(s,红磷),每1molP(s,白磷)发生反应,放出17.6kJ的热量。
(1)由此推知,其中最稳定的是
Ⅱ.在恒容密闭容器中,气体X与气体Y反应可生成气体Z,反应过程中,X、Y、Z的浓度(c)随时间(t)的变化关系如图。
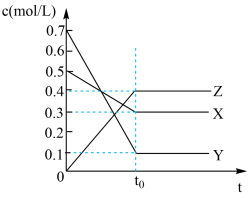
(2)该反应的化学方程式为
(3)若t0=10s,用X表示的该反应速率为
III.一种新型催化剂用于NO和CO的反应:
 。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。| 实验编号 | t(℃) | 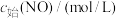 |  | 催化剂的比表面积(m2/g) |
| A | 280 | 1.2×10-3 | 5.80×10-3 | 82 |
| B | 280 | 1.2×10-3 | b | 124 |
| C | 350 | a | 5.80×10-3 | 82 |
(5)能验证温度对化学反应速率规律的是实验
Ⅲ.某化学兴趣小组利用原电池原理(如下图所示)探究
 的氧化性强于
的氧化性强于 。
。
(6)写出该装置的电极反应式。负极:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1) 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下: ,则S(单斜,s)、S(斜方,s)相比,较稳定的是
,则S(单斜,s)、S(斜方,s)相比,较稳定的是___________ [填“S(单斜,s)”或“S(斜方、s)”]。
(2)下表中的数据表示破坏 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 )。
)。
热化学方程式: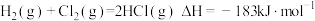 ,则
,则 键的键能为
键的键能为___________  。
。
(3)标准状况下,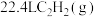 在
在 中完全燃烧生成
中完全燃烧生成 和
和 ,放出
,放出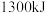 热量,请写出该反应的热化学方程式:
热量,请写出该反应的热化学方程式:___________ 。
(4)已知: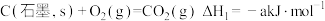
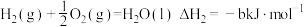
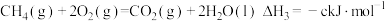
计算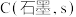 与
与 反应生成
反应生成 的
的 为
为___________ (用含a、b、c的式子表示) 。
。
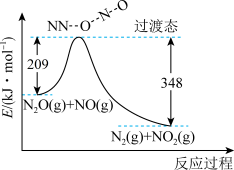
(5) 和
和 反应生成
反应生成 和
和 的能量变化如图所示。则反应过程中,每生成
的能量变化如图所示。则反应过程中,每生成 理论上放出的热量为
理论上放出的热量为___________
(1)
 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下: ,则S(单斜,s)、S(斜方,s)相比,较稳定的是
,则S(单斜,s)、S(斜方,s)相比,较稳定的是(2)下表中的数据表示破坏
 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 )。
)。| 化学键 |  |  |
| 键能 | 436 | 431 |
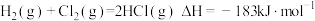 ,则
,则 键的键能为
键的键能为 。
。(3)标准状况下,
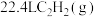 在
在 中完全燃烧生成
中完全燃烧生成 和
和 ,放出
,放出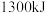 热量,请写出该反应的热化学方程式:
热量,请写出该反应的热化学方程式:(4)已知:
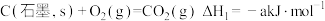
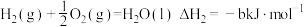
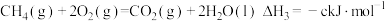
计算
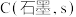 与
与 反应生成
反应生成 的
的 为
为 。
。(5)
 和
和 反应生成
反应生成 和
和 的能量变化如图所示。则反应过程中,每生成
的能量变化如图所示。则反应过程中,每生成 理论上放出的热量为
理论上放出的热量为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】水合肼 ( )常用作航天器燃料以及医药生产和工业生产。实验室制取水合肼的实验流程如下:
)常用作航天器燃料以及医药生产和工业生产。实验室制取水合肼的实验流程如下:
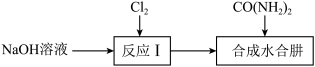
(1)反应Ⅰ中温度升高时易产生副产物 。为提高
。为提高 产率,实验中可采取的措施有
产率,实验中可采取的措施有_______ 。
A.反应容器浸入热水中
B.适当减慢通入 的速率
的速率
C.不断搅拌溶液
(2) 与
与 反应合成水合肼的离子方程式为
反应合成水合肼的离子方程式为_______ 。
(3)检验分离出水合肼后的溶液中 的实验操作是
的实验操作是_______ 。
(4)工业上可用肼(N2H4)与新生 反应制备纳米级
反应制备纳米级 ,同时放出
,同时放出 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(5)发射火箭时,肼为燃料,双氧水为氧化剂,两者反应生成氮气与水蒸气。已知1.6g液态肼在上述反应中放出64.22kJ的热量,该反应的热化学方程式为_______ 。
 )常用作航天器燃料以及医药生产和工业生产。实验室制取水合肼的实验流程如下:
)常用作航天器燃料以及医药生产和工业生产。实验室制取水合肼的实验流程如下:
(1)反应Ⅰ中温度升高时易产生副产物
 。为提高
。为提高 产率,实验中可采取的措施有
产率,实验中可采取的措施有A.反应容器浸入热水中
B.适当减慢通入
 的速率
的速率C.不断搅拌溶液
(2)
 与
与 反应合成水合肼的离子方程式为
反应合成水合肼的离子方程式为(3)检验分离出水合肼后的溶液中
 的实验操作是
的实验操作是(4)工业上可用肼(N2H4)与新生
 反应制备纳米级
反应制备纳米级 ,同时放出
,同时放出 ,该反应的化学方程式为
,该反应的化学方程式为(5)发射火箭时,肼为燃料,双氧水为氧化剂,两者反应生成氮气与水蒸气。已知1.6g液态肼在上述反应中放出64.22kJ的热量,该反应的热化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答下列问题:
(1)在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量,请回答下列问题:
①该反应的反应物总能量___________ (填“大于”“小于”或“等于”)生成物总能量。
②该反应的热化学方程式为___________ 。
(2)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是___________ (用字母表示,下同)。
②同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是___________ 。
③等pH等体积三种酸,中和NaOH的能力由大到小的顺序是___________ 。
(1)在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量,请回答下列问题:
①该反应的反应物总能量
②该反应的热化学方程式为
(2)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
②同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是
③等pH等体积三种酸,中和NaOH的能力由大到小的顺序是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列小题
(1)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意如图:
。两步反应的能量变化示意如图:
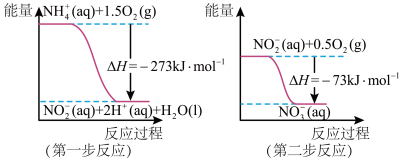
①第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
②1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___________ 。
(2)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463kJ·mol-1,O=O键能为498kJ·mol-1,计算H—H键能为___________ kJ·mol-1.
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=___________ kJ·mol-1.
(1)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意如图:
。两步反应的能量变化示意如图:
①第一步反应是
②1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(2)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463kJ·mol-1,O=O键能为498kJ·mol-1,计算H—H键能为
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是________ 。
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(2)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
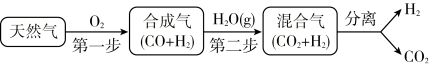
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21 kJ热量,写出该反应的热化学方程式____________________ 。
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(2)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:

CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21 kJ热量,写出该反应的热化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】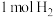 完全燃烧时放热约
完全燃烧时放热约 ,而
,而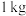 汽油完全燃烧时放热约
汽油完全燃烧时放热约 。请回答:
。请回答:
(1)等质量的氢气和汽油相比,_______ 完全燃烧放出的热多,请通过计算加以说明:_______
(2)氢气被公认是21世纪替代矿石燃料的理想能源,试简述氢气作为能源的三个优点:
①_______ ;
②_______ ;
③_______ 。
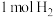 完全燃烧时放热约
完全燃烧时放热约 ,而
,而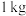 汽油完全燃烧时放热约
汽油完全燃烧时放热约 。请回答:
。请回答:(1)等质量的氢气和汽油相比,
(2)氢气被公认是21世纪替代矿石燃料的理想能源,试简述氢气作为能源的三个优点:
①
②
③
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】2023年7月28日,第31届世界大学生运动会在四川省成都市盛大开幕。已知:
回答下列问题:
(1)火炬“蓉火"采用了生物质丙烷为燃料。
①写出表示丙烷气体燃烧热的热化学方程式:_______ 。
②生物质丙烷由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和石油提炼的丙烷相比,其优点是_______ 。
(2)火炬“蓉火”通过优化燃料喷注和空气掺混等方式,减少了燃料的使用量,其原因是_______ 。
(3)我国科学家将甲烷无氧偶联制备乙烷和氢气,根据以上数据,计算该反应2CH4(g)=C2H6(g)+H2(g)的△H=_______ 。
| 物质 | 甲烷CH4 | 乙烷C2H6 | 丙烷C3H8 | H2 |
| 燃烧热△H/(kJ/mol) | -890.3 | -1559.8 | -2219.9 | -285.8 |
(1)火炬“蓉火"采用了生物质丙烷为燃料。
①写出表示丙烷气体燃烧热的热化学方程式:
②生物质丙烷由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和石油提炼的丙烷相比,其优点是
(2)火炬“蓉火”通过优化燃料喷注和空气掺混等方式,减少了燃料的使用量,其原因是
(3)我国科学家将甲烷无氧偶联制备乙烷和氢气,根据以上数据,计算该反应2CH4(g)=C2H6(g)+H2(g)的△H=
您最近半年使用:0次



