2023年7月28日,第31届世界大学生运动会在四川省成都市盛大开幕。已知:
回答下列问题:
(1)火炬“蓉火"采用了生物质丙烷为燃料。
①写出表示丙烷气体燃烧热的热化学方程式:_______ 。
②生物质丙烷由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和石油提炼的丙烷相比,其优点是_______ 。
(2)火炬“蓉火”通过优化燃料喷注和空气掺混等方式,减少了燃料的使用量,其原因是_______ 。
(3)我国科学家将甲烷无氧偶联制备乙烷和氢气,根据以上数据,计算该反应2CH4(g)=C2H6(g)+H2(g)的△H=_______ 。
| 物质 | 甲烷CH4 | 乙烷C2H6 | 丙烷C3H8 | H2 |
| 燃烧热△H/(kJ/mol) | -890.3 | -1559.8 | -2219.9 | -285.8 |
(1)火炬“蓉火"采用了生物质丙烷为燃料。
①写出表示丙烷气体燃烧热的热化学方程式:
②生物质丙烷由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和石油提炼的丙烷相比,其优点是
(2)火炬“蓉火”通过优化燃料喷注和空气掺混等方式,减少了燃料的使用量,其原因是
(3)我国科学家将甲烷无氧偶联制备乙烷和氢气,根据以上数据,计算该反应2CH4(g)=C2H6(g)+H2(g)的△H=
更新时间:2023-11-25 14:41:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)据了解,我国的三峡工程将提供相当于3000万千瓦火力发电站的水力发电功率。因此,三峡工程建设将有助于控制___________
(2)已知1g炭粉在氧气中完全燃烧放出热量32.8kJ(与1g原煤相当),若以火力发电,要达3000万千瓦的功率,每年至少需耗原煤多少万吨?(每年按365天计, )
)___________
(1)据了解,我国的三峡工程将提供相当于3000万千瓦火力发电站的水力发电功率。因此,三峡工程建设将有助于控制___________
| A.温室效应 | B.白色污染 |
| C.城市污水的任意排放 | D.长江中、下游的洪涝灾害 |
 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】碳是形成化合物种类最多的元素,其单质及其部分化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程:
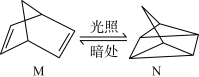 ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是__________ 。
(2)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是________ 。
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
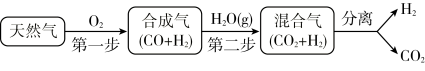
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式___________________________________________________________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程:
 ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是(2)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
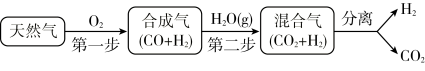
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是________ 。
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(2)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
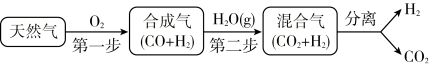
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21 kJ热量,写出该反应的热化学方程式____________________ 。
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(2)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:

CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21 kJ热量,写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】丙烯( )是仅次于乙烯(
)是仅次于乙烯( )的重要基本有机原料,工业上常利用丙烷(
)的重要基本有机原料,工业上常利用丙烷( )催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:
)催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:
①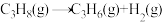 ;
;
②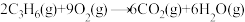 ;
;
③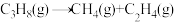 。
。
已知各物质的燃烧热如表,请计算反应①的反应热
_______ 。
 )是仅次于乙烯(
)是仅次于乙烯( )的重要基本有机原料,工业上常利用丙烷(
)的重要基本有机原料,工业上常利用丙烷( )催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:
)催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:①
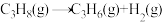 ;
;②
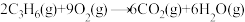 ;
;③
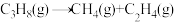 。
。已知各物质的燃烧热如表,请计算反应①的反应热

| 物质 |  |  |  |  |  |
燃烧热/( ) ) | 285.8 | 891.0 | 1411.0 | 2013.4 | 2217.8 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
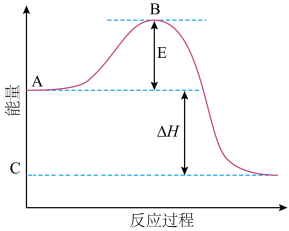
(1)图中A、C分别表示____ ,___ ,E的大小对该反应的反应热__ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点___ (填“升高”或“降低”),ΔH___ (填“变大”“变小”或“不变”)。
(2)图中ΔH=____ kJ·mol-1。
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量H2(g)反应,生成NH3(g),放出92.2kJ热量:_____ 。
②1molCu(s)与适量O2(g)反应,生成CuO(s),放出157kJ热量:_____ 。
③在25℃、101kPa时,8 g CH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式是_____ 。

(1)图中A、C分别表示
(2)图中ΔH=
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量H2(g)反应,生成NH3(g),放出92.2kJ热量:
②1molCu(s)与适量O2(g)反应,生成CuO(s),放出157kJ热量:
③在25℃、101kPa时,8 g CH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求书写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式_____________________________________________________________________ 。
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式____________________________________________________________________ 。
(3)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g) =CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+1/2O2(g) =H2O(l) ΔH3=-285.8 kJ/mol
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式______________________________________________________________________ 。
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式
(3)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g) =CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+1/2O2(g) =H2O(l) ΔH3=-285.8 kJ/mol
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】 是一种重要的化工产品,被公认为“万能中间体”。
是一种重要的化工产品,被公认为“万能中间体”。
Ⅰ.甲醇脱氢法制 是工业上的一种重要方法,具有工艺流程短、原料单一、反应条件温和等优点。其工艺过程涉及如下反应:
是工业上的一种重要方法,具有工艺流程短、原料单一、反应条件温和等优点。其工艺过程涉及如下反应:
反应a: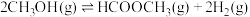

反应b: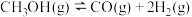
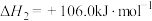
反应c: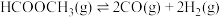
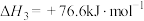
(1)
_____  。
。
(2)一定条件下,在容积为10L的恒容密闭容器中通入
 气体发生上述反应,在不同温度下连续反应4h.测得甲醇的总转化率
气体发生上述反应,在不同温度下连续反应4h.测得甲醇的总转化率 和
和 的选择性
的选择性 随温度变化如图所示。(已知:
随温度变化如图所示。(已知: 的选择性
的选择性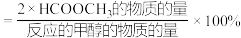 )
)
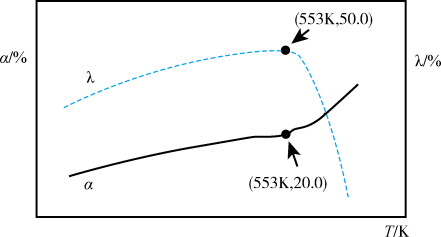
①553K时,体系中 的物质的量为
的物质的量为_____  ,4h内反应速率
,4h内反应速率
_____  。
。
②当温度高于553K时, 的选择性迅速下降的原因不可能是
的选择性迅速下降的原因不可能是_____ (填字母)。
A.升高温度使催化剂活性降低
B.升高温度使反应a逆向移动
C.反应a平衡常数减小
D.温度升高反应b速率加快
E.温度升高反应c速率加快
Ⅱ.在一定条件下可利用甲醇羰基化法制甲酸甲酯,其反应原理可表示为: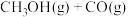
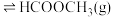
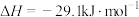 。
。
(3)向体积为2L的密闭容器中充入
 和
和
 ,测得容器内的压强p随时间t的变化关系如下图中ⅰ、ⅱ、ⅲ曲线所示:
,测得容器内的压强p随时间t的变化关系如下图中ⅰ、ⅱ、ⅲ曲线所示:
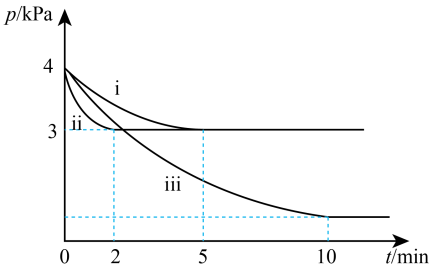
①ⅱ和ⅰ相比,改变的反应条件是_____ 。
②反应ⅱ在2min时达到平衡,平衡常数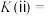
_____  。在体积和温度不变的条件下,在上述反应达到平衡ⅱ时,再往容器中加入
。在体积和温度不变的条件下,在上述反应达到平衡ⅱ时,再往容器中加入
 和
和
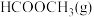 后,
后,
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③反应ⅰ的温度
_____ (填“>”、“<”或“=”)反应ⅲ的温度 。
。
 是一种重要的化工产品,被公认为“万能中间体”。
是一种重要的化工产品,被公认为“万能中间体”。Ⅰ.甲醇脱氢法制
 是工业上的一种重要方法,具有工艺流程短、原料单一、反应条件温和等优点。其工艺过程涉及如下反应:
是工业上的一种重要方法,具有工艺流程短、原料单一、反应条件温和等优点。其工艺过程涉及如下反应:反应a:
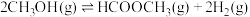

反应b:
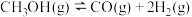
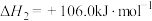
反应c:
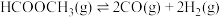
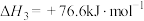
(1)

 。
。(2)一定条件下,在容积为10L的恒容密闭容器中通入

 气体发生上述反应,在不同温度下连续反应4h.测得甲醇的总转化率
气体发生上述反应,在不同温度下连续反应4h.测得甲醇的总转化率 和
和 的选择性
的选择性 随温度变化如图所示。(已知:
随温度变化如图所示。(已知: 的选择性
的选择性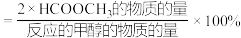 )
)
①553K时,体系中
 的物质的量为
的物质的量为 ,4h内反应速率
,4h内反应速率
 。
。②当温度高于553K时,
 的选择性迅速下降的原因不可能是
的选择性迅速下降的原因不可能是A.升高温度使催化剂活性降低
B.升高温度使反应a逆向移动
C.反应a平衡常数减小
D.温度升高反应b速率加快
E.温度升高反应c速率加快
Ⅱ.在一定条件下可利用甲醇羰基化法制甲酸甲酯,其反应原理可表示为:
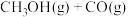
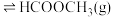
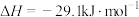 。
。(3)向体积为2L的密闭容器中充入

 和
和
 ,测得容器内的压强p随时间t的变化关系如下图中ⅰ、ⅱ、ⅲ曲线所示:
,测得容器内的压强p随时间t的变化关系如下图中ⅰ、ⅱ、ⅲ曲线所示:
①ⅱ和ⅰ相比,改变的反应条件是
②反应ⅱ在2min时达到平衡,平衡常数
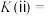
 。在体积和温度不变的条件下,在上述反应达到平衡ⅱ时,再往容器中加入
。在体积和温度不变的条件下,在上述反应达到平衡ⅱ时,再往容器中加入
 和
和
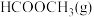 后,
后,
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③反应ⅰ的温度

 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)用O2将HCl转化为Cl2,可提高效益,减少污染。传统上该转化通过如下图所示的催化循环实现。
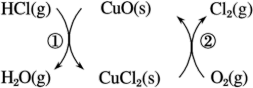
其中,反应①为2HCl(g)+CuO(s) = H2O(g)+CuCl2(s) ΔH1,反应②生成1 mol Cl2的反应热为ΔH2,则总反应的热化学方程式为______________ (反应热用ΔH1和ΔH2表示)。
(2)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。
已知25 ℃,101 kPa时:
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1648 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393 kJ·mol-1
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480 kJ·mol-1
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是____________ 。
(3)已知:温度为T时:CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH=+165 kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ·mol-1
贮氢合金ThNi5可催化由CO、H2合成CH4的反应,温度为T时,该反应的热化学方程式为______ 。
(4)已知:Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1344.1 kJ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1169.2 kJ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为___________ 。
(5)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) = CH3OH(g) ΔH1
②CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g) = CO(g)+H2O(g) ΔH3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
由此计算ΔH1=________ kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=________ kJ·mol-1。
(6)已知:① H2(g)+Cl2(g)=2HCl(g) △H=-183 kJ/mol
② 断开1mol H2分子中的化学键需要吸收436kJ的能量
③ 断开1mol Cl2分子中的化学键需要吸收243kJ的能量
则:断开1mol HCl分子中的化学键需要吸收______ kJ的能量。
(1)用O2将HCl转化为Cl2,可提高效益,减少污染。传统上该转化通过如下图所示的催化循环实现。
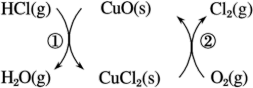
其中,反应①为2HCl(g)+CuO(s) = H2O(g)+CuCl2(s) ΔH1,反应②生成1 mol Cl2的反应热为ΔH2,则总反应的热化学方程式为
(2)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。
已知25 ℃,101 kPa时:
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1648 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393 kJ·mol-1
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480 kJ·mol-1
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是
(3)已知:温度为T时:CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH=+165 kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ·mol-1
贮氢合金ThNi5可催化由CO、H2合成CH4的反应,温度为T时,该反应的热化学方程式为
(4)已知:Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1344.1 kJ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1169.2 kJ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为
(5)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) = CH3OH(g) ΔH1
②CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g) = CO(g)+H2O(g) ΔH3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
(6)已知:① H2(g)+Cl2(g)=2HCl(g) △H=-183 kJ/mol
② 断开1mol H2分子中的化学键需要吸收436kJ的能量
③ 断开1mol Cl2分子中的化学键需要吸收243kJ的能量
则:断开1mol HCl分子中的化学键需要吸收
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】将CO2转化为高附加值碳基燃料,可有效减少碳排放。将CO2和H2在催化剂作用下,可实现二氧化碳甲烷化。可能发生反应:
i.CO2(g)+4H2 (g) CH4 (g)+2 H2O(g) ΔH1
CH4 (g)+2 H2O(g) ΔH1
ii.CO2(g)+H2 (g) CO (g)+ H2O(g) ΔH2=+41.2 kJ·mol-1
CO (g)+ H2O(g) ΔH2=+41.2 kJ·mol-1
iii.CO(g)+3H2 (g) CH4 (g)+ H2O(g) ΔH3=-206.1kJ·mol-1
CH4 (g)+ H2O(g) ΔH3=-206.1kJ·mol-1
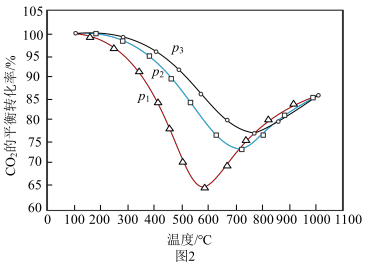
(1)不同条件下,投料,发生上述反应,CO2的平衡转化率与温度的关系如图2,升高温度,反应i的化学平衡常数___________ (填“增大”或“减小”);p1、p2、p3由大到小的顺序是___________ 。压强为p1的条件下,温度高于600℃之后,随着温度升高转化率增大的原因是___________ 。
(2)在某温度下,向恒容容器中充入7 mol CO2和12 mol H2,初始压强为19kPa,反应经10min达到平衡,此时气体的总物质的量为17mol,p(CO)=3kPa,则v(CH4)=___________ kPa/min,该温度下反应ii的化学平衡常数K=___________ 。
(3)若保持温度不变压缩容器的体积,CH4的物质的量___________ (填“增加”“减小”或“不变”),反应i的平衡将___________ (填“正向”“逆向”或“不”)移动。
i.CO2(g)+4H2 (g)
 CH4 (g)+2 H2O(g) ΔH1
CH4 (g)+2 H2O(g) ΔH1ii.CO2(g)+H2 (g)
 CO (g)+ H2O(g) ΔH2=+41.2 kJ·mol-1
CO (g)+ H2O(g) ΔH2=+41.2 kJ·mol-1iii.CO(g)+3H2 (g)
 CH4 (g)+ H2O(g) ΔH3=-206.1kJ·mol-1
CH4 (g)+ H2O(g) ΔH3=-206.1kJ·mol-1
(1)不同条件下,投料,发生上述反应,CO2的平衡转化率与温度的关系如图2,升高温度,反应i的化学平衡常数
(2)在某温度下,向恒容容器中充入7 mol CO2和12 mol H2,初始压强为19kPa,反应经10min达到平衡,此时气体的总物质的量为17mol,p(CO)=3kPa,则v(CH4)=
(3)若保持温度不变压缩容器的体积,CH4的物质的量
您最近一年使用:0次



