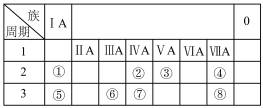
下表是元素周期表的一部分,按要求填空(填元素符号 或化学式 ):
(1)写出下列元素的元素符号 :①___ ,②___ ;
(2)在这些元素中,最活泼的金属元素 是___ ,最不活泼的元素 是___ 。
(3)在这些元素的最高价氧化物对应水化物 中,酸性最强的是___ ,碱性最强的是___ ,呈两性的氢氧化物 是___ 。
(4)写出③和⑧的单质反应产物的电子式___ 。
(5)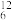 C在周期表中的位置:第
C在周期表中的位置:第___ 周期___ 族,它与氧气完全燃烧的产物的电子式___ 。
(6)在③与④的单质 中,化学性质较活泼的是___ ,判断的实验依据是___ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)在这些元素中,最活泼的
(3)在这些元素的最高价氧化物对应
(4)写出③和⑧的单质反应产物的电子式
(5)
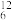 C在周期表中的位置:第
C在周期表中的位置:第(6)在③与④的
更新时间:2020-04-28 18:42:21
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E为原子序数依次增大的同一短周期主族元素,已知A、C、D三种原子最外层共有10个电子,且这3种元素的最高价氧化物对应的水化物两两皆能发生反应生成盐和水。则:
(1)5种元素简单离子的离子半径由大到小的顺序是(用实际离子符号表示):_______ 。
(2)比较A、B、C的最高价氧化物的水化物的碱性(用化学式表示):_______ 。
(3)比较D、E的最高价氧化物的水化物的酸性(用化学式表示):_______ 。
(4)写出A、B两元素的最高价氧化物的水化物之间反应的离子方程式:_______ 。
(1)5种元素简单离子的离子半径由大到小的顺序是(用实际离子符号表示):
(2)比较A、B、C的最高价氧化物的水化物的碱性(用化学式表示):
(3)比较D、E的最高价氧化物的水化物的酸性(用化学式表示):
(4)写出A、B两元素的最高价氧化物的水化物之间反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】已知A、B、C、D是短周期元素的气态单质,其中A是黄绿色的气体单质,C在空气中含量最高,D是最轻的气体;E是一种最常用的金属;Y是一种常见的液态物质,Z是唯一显碱性的气体; M是一种红棕色的有毒气体;I为红褐色难溶于水的固体。有关的转化关系如下图所示(反应条件均已略去)。
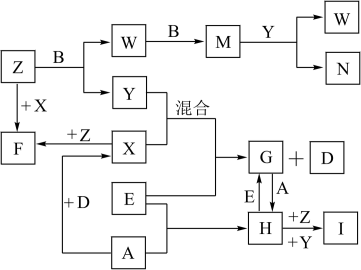
回答下列问题:
(1)A的组成元素在元素周期表的位置为____ ;
(2)F中化学键的类型是___ 、____ ;
(3)Z和W在催化剂作用下反应生成C和Y,这是很有实际意义的反应,可以消除W对环境的污染,该反应的化学方程式为_ ;
(4)将过量的E加到N的稀溶液中,若过程中转移电子的数目为3.01×1023,则参加反应的E的质量为____ g。

回答下列问题:
(1)A的组成元素在元素周期表的位置为
(2)F中化学键的类型是
(3)Z和W在催化剂作用下反应生成C和Y,这是很有实际意义的反应,可以消除W对环境的污染,该反应的化学方程式为
(4)将过量的E加到N的稀溶液中,若过程中转移电子的数目为3.01×1023,则参加反应的E的质量为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知:Y为地壳中含量最多的元素,M原子的最外层电子数与次外层电数之比为3:4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,请回答下列问题:
(1)M在元素周期表中的位置__ ;Z+离子的结构示意图为__ 。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式__ 。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__ 。
(4)实验室制备R的单质,该反应的离子方程式为__ 。
(5)R非金属性强于M,下列选项中能证明这一事实的是__ (填字母序号)。
A.常温下的R单质熔沸点比M单质的高
B.R的氢化物比M的氢化物更稳定
C.一定条件下R和M的单质都能与NaOH溶液反应
D.最高价氧化物对应水化物的酸性强弱:R>M
(6)由X、Y、Z、M四种元素组成的一种弱酸酸式盐A。向A溶液中通入氯气,得到无色溶液,写出该反应的离子方程式__ 。
(1)M在元素周期表中的位置
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式
(4)实验室制备R的单质,该反应的离子方程式为
(5)R非金属性强于M,下列选项中能证明这一事实的是
A.常温下的R单质熔沸点比M单质的高
B.R的氢化物比M的氢化物更稳定
C.一定条件下R和M的单质都能与NaOH溶液反应
D.最高价氧化物对应水化物的酸性强弱:R>M
(6)由X、Y、Z、M四种元素组成的一种弱酸酸式盐A。向A溶液中通入氯气,得到无色溶液,写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下列是部分短周期中第二、第三周期元素的原子半径及主要化合价。
回答下列问题:
(1)⑦在元素周期表中的位置是(周期、族)_______ 。
(2)七种元素的最高价氧化物的水化物中,酸性最强的是_______ (填化学式)。
(3)①元素和⑤元素形成化合物的电子式是_______ 。
(4)写出③最高价氧化物对应水化物与⑤的氢化物水溶液反应的离子方程式:_______ 。
(5)下列叙述正确的是_______ (填字母)。
A.③、④处于同周期
B.②的阳离子与⑦的阴离子的核外电子数相等
C.⑤在同主族元素中非金属性最强
D.④元素与⑥元素两者核电荷数之差是 8
E.①与⑦形成的化合物具有两性
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(nm) | 0.186 | 0.160 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +3 | +5、−3 | +7、−1 | +5、−3 | −2 |
(1)⑦在元素周期表中的位置是(周期、族)
(2)七种元素的最高价氧化物的水化物中,酸性最强的是
(3)①元素和⑤元素形成化合物的电子式是
(4)写出③最高价氧化物对应水化物与⑤的氢化物水溶液反应的离子方程式:
(5)下列叙述正确的是
A.③、④处于同周期
B.②的阳离子与⑦的阴离子的核外电子数相等
C.⑤在同主族元素中非金属性最强
D.④元素与⑥元素两者核电荷数之差是 8
E.①与⑦形成的化合物具有两性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是______ (填元素符号,下同),形成化合物种类最多的元素是________________________ 。
(2)第三周期元素除⑩外原子半径最小的是______ (填元素符号),
(3)这些元素的最高价氧化物对应水化物中碱性最强的是__________ (填化学式,下同),具有两性的是____________ 。
(4)⑤、⑧两种元素的最高价氧化物对应的水化物相互反应的离子方程式为____________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)第三周期元素除⑩外原子半径最小的是
(3)这些元素的最高价氧化物对应水化物中碱性最强的是
(4)⑤、⑧两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有重要的作用。下表列出①〜⑩十种元素在周期表中的位置。
(1)①〜⑩中金属性最强的元素为______ (写名称)。
(2)⑦、⑨两种元素的最高价氧化物对应水化物的酸性较强的是______ (填化学式)。
(3)①、⑥、⑧、⑨四种元素形成的简单离子半径由大到小的顺序依次是_______ 。(用微粒符号来表示)
(4)⑤元素的氢化物实验室制法的化学方程式是_____ 。⑤、⑨的气态氢化物在空气中相遇有白烟生成,写出白烟对应物质的电子式_______ 。
(5)下列说法正确的是_____ (填字母)。
a.⑥的非金属性强于⑦
b.氢化物稳定性:⑦<⑩
c.③单质与水反应比单质①剧烈
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ⑤ | ⑧ | ||||||
| 3 | ① | ③ | ④ | ⑥ | ⑨ | |||
| 4 | ② | ⑦ | ⑩ |
(1)①〜⑩中金属性最强的元素为
(2)⑦、⑨两种元素的最高价氧化物对应水化物的酸性较强的是
(3)①、⑥、⑧、⑨四种元素形成的简单离子半径由大到小的顺序依次是
(4)⑤元素的氢化物实验室制法的化学方程式是
(5)下列说法正确的是
a.⑥的非金属性强于⑦
b.氢化物稳定性:⑦<⑩
c.③单质与水反应比单质①剧烈
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,⑦的元素符号____ ,原子半径最大的是____ ,S2-结构示意图为____ 。
(2)元素的最高价氧化物对应的水化物中酸性最强的___ ,碱性最强的是____ ,呈两性的氢氧化物是____ 。
(3)按要求写出下列两种物质的电子式:①的氢化物_____ ;③的最高价氧化物对应的水化物____ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)元素的最高价氧化物对应的水化物中酸性最强的
(3)按要求写出下列两种物质的电子式:①的氢化物
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】元素是构成我们生活的世界中一切物质的“原材料”。短周期元素A、B、D、E、G、J在周期表中的位置如下:

根据上表回答问题:
(1)D在周期表中的位置是_______ ;
(2)A、B、E、G的原子半径由大到小的顺序是_______ (填元素符号);
(3)用电子式表示E的最高价氧化物的形成过程_______ ;
(4)B、D的气态氢化物的稳定性大小关系为_______ (填化学式);
(5)E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i 、ii
、ii_______ 、iii_______ ;
(6)J单质通入E的最高价氧化物对应水化物的溶液中,可以得到漂白液,相应反应的化学方程式为_______ 。

根据上表回答问题:
(1)D在周期表中的位置是
(2)A、B、E、G的原子半径由大到小的顺序是
(3)用电子式表示E的最高价氧化物的形成过程
(4)B、D的气态氢化物的稳定性大小关系为
(5)E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i
 、ii
、ii(6)J单质通入E的最高价氧化物对应水化物的溶液中,可以得到漂白液,相应反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表为元素周期表的一部分。请参照元素①~⑧在表中的位置,用化学用语回答问题:
(1)画出元素③的原子结构示意图:___________ ,它的气态氢化物的化学式为___________ 。
(2)①~⑧中,最活泼的金属元素是____________ (写元素符号,下同);最活泼的非金属元素是___________ 。
(3)⑦⑧的最高价氧化物对应水化物的酸性由强到弱的顺序是____________ 。
(4)④、⑤、⑥三种元素的简单离子半径由大到小的顺序是___________ 。
(5)⑥的最高价氧化物与⑤的最高价氧化物对应水化物反应的离子方程式是______________________ 。

(1)画出元素③的原子结构示意图:
(2)①~⑧中,最活泼的金属元素是
(3)⑦⑧的最高价氧化物对应水化物的酸性由强到弱的顺序是
(4)④、⑤、⑥三种元素的简单离子半径由大到小的顺序是
(5)⑥的最高价氧化物与⑤的最高价氧化物对应水化物反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下列是部分短周期中第二、第三周期元素的原子半径及主要化合价。
回答下列问题:
(1)⑦在元素周期表中的位置是(周期、族)_______ 。
(2)七种元素的最高价氧化物的水化物中,酸性最强的是_______ (填化学式)。
(3)①元素和⑤元素形成化合物的电子式是_______ 。
(4)写出③最高价氧化物对应水化物与⑤的氢化物水溶液反应的离子方程式:_______ 。
(5)下列叙述正确的是_______ (填字母)。
A.③、④处于同周期
B.②的阳离子与⑦的阴离子的核外电子数相等
C.⑤在同主族元素中非金属性最强
D.④元素与⑥元素两者核电荷数之差是 8
E.①与⑦形成的化合物具有两性
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(nm) | 0.186 | 0.160 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +3 | +5、−3 | +7、−1 | +5、−3 | −2 |
(1)⑦在元素周期表中的位置是(周期、族)
(2)七种元素的最高价氧化物的水化物中,酸性最强的是
(3)①元素和⑤元素形成化合物的电子式是
(4)写出③最高价氧化物对应水化物与⑤的氢化物水溶液反应的离子方程式:
(5)下列叙述正确的是
A.③、④处于同周期
B.②的阳离子与⑦的阴离子的核外电子数相等
C.⑤在同主族元素中非金属性最强
D.④元素与⑥元素两者核电荷数之差是 8
E.①与⑦形成的化合物具有两性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】X、Y、Z、V、W为五种前四周期元素,其中X是短周期(除稀有气体外)原子半径最大的元素;Y与X同周期,其最高价氧化物的水化物呈两性;Z原子基态时2p原子轨道上有3个未成对的电子;V原子的核外电子排布式为ls22s22p63s2;W的原子序数为29,W的离子能与乙二胺(H2N—CH2—CH2—NH2)形成配离子(如图):回答下列问题:

(1)W原子的核外电子排布式为___________ ,配位原子的杂化类型为___________ ,该配离子中不含有的化学键类型有___________ 。(填字母)
a.配位键 b.极性键 c.离子键 d.非极性键
(2)元素X、Y、V第一电离能由大到小的顺序是___________ (用元素符号表示)。
(3)Z元素在周期表中的位置为___________ ,Z元素简单氢化物的空间构型是___________ ;
(4)确定V元素的科学方法是______
(5)Y元素的最高价氧化物的水化物具有两性,写出该两性物质与X元素的最高价氧化物的水化物反应的离子方程式:___________ 。

(1)W原子的核外电子排布式为
a.配位键 b.极性键 c.离子键 d.非极性键
(2)元素X、Y、V第一电离能由大到小的顺序是
(3)Z元素在周期表中的位置为
(4)确定V元素的科学方法是______
| A.红外光谱 | B.质谱 | C.原子光谱 | D.核磁共振谱 |
您最近一年使用:0次