解题方法
1 . 元素周期表是学习物质结构和性质的重要工具。下表是元素周期表的一部分,表中所列序号代表对应的元素。请回答下列问题:_______ (填元素符号),元素⑧在周期表中的位置是_______ 。
(2)由上述元素形成的最高价氧化物对应的水化物中,酸性最强的是_______ (填物质名称)。
(3)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是_______ (填离子符号)。
(4)①与⑤可形成 微粒,写出该微粒的电子式:
微粒,写出该微粒的电子式:_______ 。
(5)欲比较⑤与⑥的非金属性强弱,下列说法可作为判断依据的是_______ (填标号)。
a.比较⑤、⑥两种元素单质的沸点高低
b.比较⑤、⑥两种元素单质与 化合的难易程度
化合的难易程度
c.比较⑤、⑥两种元素气态氢化物的稳定性
d.比较⑤、⑥两种元素的氧化物对应水化物的酸性强弱
(6)元素③和④的金属性:③_______ ④(填“>”或“<”),元素④的单质可与元素③的最高价氧化物的水化物反应,写出该反应的化学方程式:_______ 。

(2)由上述元素形成的最高价氧化物对应的水化物中,酸性最强的是
(3)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是
(4)①与⑤可形成
 微粒,写出该微粒的电子式:
微粒,写出该微粒的电子式:(5)欲比较⑤与⑥的非金属性强弱,下列说法可作为判断依据的是
a.比较⑤、⑥两种元素单质的沸点高低
b.比较⑤、⑥两种元素单质与
 化合的难易程度
化合的难易程度c.比较⑤、⑥两种元素气态氢化物的稳定性
d.比较⑤、⑥两种元素的氧化物对应水化物的酸性强弱
(6)元素③和④的金属性:③
您最近半年使用:0次
解题方法
2 . 下表为元素周期表中的一部分.
用化学式或元素符号回答下列问题:
(1)①③⑤中,最高价氧化物对应水化物中碱性最强的是____________ .
(2)②③④中形成的简单离子半径由大到小的顺序是____________ .
(3)⑨的最高价氧化物对应水化物的化学式为____________ .①和⑨两元素形成化合物的化学式为____________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为____________ .
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是____________ ,三者非金属性的强弱顺序为____________ .
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(1)①③⑤中,最高价氧化物对应水化物中碱性最强的是
(2)②③④中形成的简单离子半径由大到小的顺序是
(3)⑨的最高价氧化物对应水化物的化学式为
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近半年使用:0次
3 . 下表列出了①~⑨九种元素在周期表中的位置:
(1)元素④在周期表中所处位置_______ 。
(2)按气态氢化物的稳定性由强到弱的顺序排列,④⑦⑧的氢化物稳定性:_______ (写氢化物的化学式)。
(3)元素⑤、⑥最高价氧化物对应水化物的碱性强弱为_______ (填化学式)。
(4)元素⑧的原子结构示意图是_______ 。
(5)写出元素⑤形成的单质在氧气中燃烧的化学方程式_______ 。
(6)用电子式表示⑤与⑧反应得到的化合物的形成过程_______ 。
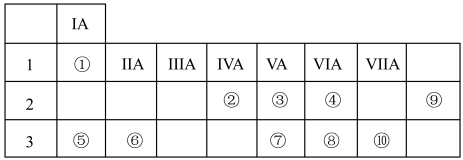
(1)元素④在周期表中所处位置
(2)按气态氢化物的稳定性由强到弱的顺序排列,④⑦⑧的氢化物稳定性:
(3)元素⑤、⑥最高价氧化物对应水化物的碱性强弱为
(4)元素⑧的原子结构示意图是
(5)写出元素⑤形成的单质在氧气中燃烧的化学方程式
(6)用电子式表示⑤与⑧反应得到的化合物的形成过程
您最近半年使用:0次
解题方法
4 . 下表是元素周期表的一部分。请按要求回答下列问题:___________ ,⑦的最高价氧化物对应水化物的化学式___________ 。
(2)上述所列元素最高价氧化物对应水化物碱性最强的是___________ (填化学式)。
(3)写出由上述所列元素形成的18电子的双原子分子的化学式___________ 。
(4)下列说法不正确的是___________。
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式___________ 。
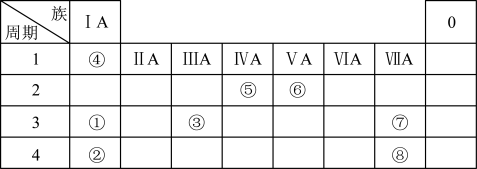
(2)上述所列元素最高价氧化物对应水化物碱性最强的是
(3)写出由上述所列元素形成的18电子的双原子分子的化学式
(4)下列说法不正确的是___________。
| A.⑥形成的最简单氢化物比⑤形成的最简单氢化物的稳定性高 |
| B.元素最高正价与最低负价绝对值相等的元素一定处于第ⅣA族 |
| C.第5周期第ⅦA族元素的原子序数为53 |
| D.周期表中当某元素的周期序数大于其主族序数时,该元素可能属于金属或非金属 |
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式
您最近半年使用:0次
名校
5 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
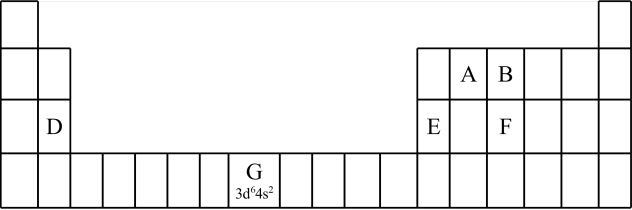
(1)认识元素周期表的结构:___________ 区。
②2017年5月9日我国发布了113号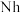 、115号
、115号 、117号
、117号 、118号
、118号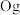 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期 族
族
b.117号元素 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:
(2)认识原子结构与元素周期表的关系:见表中元素 的信息,其中 “
的信息,其中 “ ”称为该元素原子的
”称为该元素原子的___________ ,该元素 能层上具有
能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D_______ E(填“>” “<”或“=”)。
②气态氢化物的沸点:B_____ F (填“>”“<”或“=”),理由是___________ 。B的另一种氢化物可以作为火箭推进剂的燃料之一,其电子式为___________ 。
(1)认识元素周期表的结构:
②2017年5月9日我国发布了113号
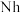 、115号
、115号 、117号
、117号 、118号
、118号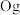 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是a.113号元素在周期表中的位置是第七周期
 族
族b.117号元素
 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:

(2)认识原子结构与元素周期表的关系:见表中元素
 的信息,其中 “
的信息,其中 “ ”称为该元素原子的
”称为该元素原子的 能层上具有
能层上具有(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近半年使用:0次
名校
解题方法
6 . 碱金属中的锂被称为“21世纪的能源金属”,锂电池在航空工业中有着重要作用。离子化合物氢化锂(LiH)是一种制氢剂,其中H-离子半径大于Li+离子半径,用物质结构理论分析,其原因是___________ 。
您最近半年使用:0次
名校
解题方法
7 . 铝及其合金是金属材料界后起之秀。铝的冶炼历史较短,这是由于炼铝原料Al2O3的熔点较高的缘故,直到人们找到助熔剂冰晶石(Na3AlF6) 才实现了Al2O3在较低温度下的熔融电离。据此判断:Al2O3属于
才实现了Al2O3在较低温度下的熔融电离。据此判断:Al2O3属于___________ (选填“离子”或“共价”)化合物。列举一个事实证明并判断:组成冰晶石的两种金属元素,它们金属性的相对强弱___________ 。
 才实现了Al2O3在较低温度下的熔融电离。据此判断:Al2O3属于
才实现了Al2O3在较低温度下的熔融电离。据此判断:Al2O3属于
您最近半年使用:0次
名校
解题方法
8 . 某品牌去屑洗发水的有效成分为二硫化硒(SeS2),利用元素周期律知识分析, 中Se元素化合价呈正价的原因。
中Se元素化合价呈正价的原因。___________ 。
 中Se元素化合价呈正价的原因。
中Se元素化合价呈正价的原因。
您最近半年使用:0次
名校
解题方法
9 . 硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
A.酸性: | B.热稳定性: |
| C.二氧化硒(SeO2)只具有还原性 | D.硒元素的最低负化合价为-2价 |
您最近半年使用:0次
10 . 下列关于F、Cl、Br、I的比较中,正确的是
| A.随核电荷数的增加,单质的密度逐渐减小 |
| B.随核电荷数的增加,氢化物的稳定性逐渐增强 |
| C.随核电荷数的增加,单质的颜色逐渐加深 |
| D.单质与水反应均可表示为X2+H2O=HX+HXO |
您最近半年使用:0次



