名校
解题方法
1 . 根据下表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| 主要化合价 |  |  |  |  、 、 |  |
A.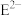 与 与 的核外电子数不可能相等 的核外电子数不可能相等 | B.单质与稀盐酸反应的速率 |
C.最高价氧化物对应水化物的碱性 | D.氢化物的稳定性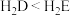 |
您最近半年使用:0次
名校
解题方法
2 . 科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是
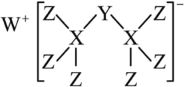
| A.WZ的水溶液呈碱性 |
B.元素非金属性的顺序为 |
| C.Y的最高价氧化物的水化物的晶体是分子晶体 |
| D.该新化合物中Y不满足8电子稳定结构 |
您最近半年使用:0次
名校
3 . X、Y、Z、M四种短周期元素,原子半径M>Z>X>Y,其中X、Y处在同一周期,X、Z处在同一主族。Z原子核内质子数等于X、Y原子核内质子数之和,原子核外最外层上的电子数是M原子核外最外层电子数的4倍。请回答:
(1)这两种元素名称分别是X_______ ,M_______ 。
(2)Y的简单离子结构示意图是_______ ;Z在周期表中的位置是_______ 。
(3)X、Y、Z这三种元素的气态氢化物的稳定性由大而小的顺序是_______ 。
(4)X与Y形成的三原子分子甲的结构式是_______ ,Y与M形成的原子个数比为1∶1的化合物乙的电子式是_______ ,甲与乙反应的化学方程式是_______ 。
(1)这两种元素名称分别是X
(2)Y的简单离子结构示意图是
(3)X、Y、Z这三种元素的气态氢化物的稳定性由大而小的顺序是
(4)X与Y形成的三原子分子甲的结构式是
您最近半年使用:0次
4 . 下表为八种短周期主族元素的部分性质(已知铍的原子半径为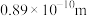 ):
):
(1)元素Z在元素周期表中的位置为___________ ,元素Y为___________ (填元素符号)。
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:___________ 。
(3)R与T相比,非金属性较强的是___________ (填元素符号),下列事实能证明这一结论的是___________ (填标号)。
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性: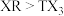
c.最高价氧化物对应水化物的酸性:
(4)J与Q相比,金属性较强的是___________ (填元素符号),能证明这一结论的依据是___________ 。
(5)根据表中数据推测,M的原子半径的最小范围是___________ 。
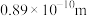 ):
):| 元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径 | 0.74 | 0.75 | r | 0.99 | 1.86 | 1.43 | 1.10 | |
| 主要化合价 |  |  、 、 |  、 、 |  、 、 |  |  |  、 、 | |
| 其他 | 原子核内无中子 | 重要的半导体材料 | 有两种氧化物 |
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:
(3)R与T相比,非金属性较强的是
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性:
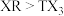
c.最高价氧化物对应水化物的酸性:

(4)J与Q相比,金属性较强的是
(5)根据表中数据推测,M的原子半径的最小范围是
您最近半年使用:0次
名校
5 . 由X、Y、Z、M四种原子序数依次增大的短周期主族元素组成的化合物甲可用作杀虫剂和纺织工业中的树脂整理催化剂。其中元素X的一种原子中没有中子;元素Y的最外层电子数比电子层数多1;Z与X形成的化合物的水溶液呈碱性,M与X形成的化合物的水溶液不能用玻璃瓶保存。下列说法正确的是
| A.非金属性:Y>Z>M |
| B.Z元素对应的简单离子半径大于M元素对应的简单离子半径 |
| C.最高价氧化物对应水化物的酸性:Y>Z |
| D.X的单质与M的单质不发生反应 |
您最近半年使用:0次
解题方法
6 . 有以下6种元素,其中R、W、X、Y、M是原子序数依次增大的五种短周期元素,R最常见同位素的原子核中不含中子。W与X可形成两种稳定的化合物:WX和WX2.工业革命以来,人类使用的化石燃料在燃烧过程中将大量WX2排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相邻。Q是第4周期第Ⅷ族元素,它的一种复杂的化合物是具有磁性的黑色晶体。
(1)若R的一种原子中质子数和中子数相等,则R的原子组成符号为___________ ;R2Y、R2X都属于___________ (填“离子”或“共价”)化合物。W在元素周期表中的位置___________ 。
(2)M是生活中常见的一种元素,它能与很多元素形成化合物。
①用电子式表示RM的形成过程___________ 。
②如图所示,将M单质水溶液滴入试管中。试管中的实验现象为___________ 。___________ 。
③MX2是一种高效消毒剂,工业上用其处理中性废水中的锰,使 转化为MnO2沉淀除去,M被还原至最低价,该反应的离子方程式为
转化为MnO2沉淀除去,M被还原至最低价,该反应的离子方程式为___________ 。
(3)元素硒(Se)的原子结构示意图为
根据元素周期律,下列推断正确的是___________ (填字母序号)
a.Se位于第4周期、与Y同主族 b.Se的最低负化合价为-2价
c.SeO2具有还原性 d.H2Se的还原性比H2Y强
e.H2SeO3的酸性强于H2SO4 f.SeO2在一定条件下可与NaOH溶液反应
(4)下列事实能判断元素金属性强弱的是___________ (填字母)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(1)若R的一种原子中质子数和中子数相等,则R的原子组成符号为
(2)M是生活中常见的一种元素,它能与很多元素形成化合物。
①用电子式表示RM的形成过程
②如图所示,将M单质水溶液滴入试管中。试管中的实验现象为

③MX2是一种高效消毒剂,工业上用其处理中性废水中的锰,使
 转化为MnO2沉淀除去,M被还原至最低价,该反应的离子方程式为
转化为MnO2沉淀除去,M被还原至最低价,该反应的离子方程式为(3)元素硒(Se)的原子结构示意图为

根据元素周期律,下列推断正确的是
a.Se位于第4周期、与Y同主族 b.Se的最低负化合价为-2价
c.SeO2具有还原性 d.H2Se的还原性比H2Y强
e.H2SeO3的酸性强于H2SO4 f.SeO2在一定条件下可与NaOH溶液反应
(4)下列事实能判断元素金属性强弱的是
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
您最近半年使用:0次
7 . 根据元素周期律判断,不正确的是
| A.Mg原子失电子能力比Ca弱 | B.K与水反应比Mg与水反应剧烈 |
| C.HCl的稳定性强于HBr | D. 酸性强于 酸性强于 |
您最近半年使用:0次
名校
解题方法
8 . X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子K层和L层电子数之比为1∶2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,R的一种氧化物能使品红溶液褪色,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)X的最高价氧化物的电子式为______ ;
(2)X、Y、Z、W的原子半径由大到小的顺序:____________ (用元素符号表示)。
(3)元素W在周期表的位置______ ,其最高价氧化物对应水化物与R的最高价氧化物对应水化物(酸性或碱性)强弱是______ (用化学式表示)。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做其吸收剂,写出吸收剂与足量该氧化物反应的离子方程式____________ 。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1∶3,则该反应的化学方程式为____________ 。
(1)X的最高价氧化物的电子式为
(2)X、Y、Z、W的原子半径由大到小的顺序:
(3)元素W在周期表的位置
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做其吸收剂,写出吸收剂与足量该氧化物反应的离子方程式
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1∶3,则该反应的化学方程式为
您最近半年使用:0次
解题方法
9 . 下表列出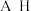 八种元素在周期表中的位置:
八种元素在周期表中的位置:
回答下列问题:
(1) 、
、 、
、 三种元素中,原子半径最大的是
三种元素中,原子半径最大的是___________ (填元素符号,下同)。
(2)写出 与
与 两元素最高价氧化物对应水化物反应的离子方程式:
两元素最高价氧化物对应水化物反应的离子方程式:___________ 。
(3)这八种元素中非金属性最强的元素是___________ 。
(4)写出 、
、 两元素形成的原子个数比为
两元素形成的原子个数比为 的物质的电子式:
的物质的电子式:___________ 。
(5) 的氢化物属于
的氢化物属于___________ (填“离子化合物”或“共价化合物”)。
该氢化物与水反应的化学方程式为___________ 。
(6) 和
和 两种元素形成的简单氢化物的稳定性
两种元素形成的简单氢化物的稳定性
___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
 八种元素在周期表中的位置:
八种元素在周期表中的位置:| 周期 | 主族 | ||||||
Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | |
| 2 |  |  |  | ||||
| 3 |  |  |  |  | |||
| 4 |  | ||||||
(1)
 、
、 、
、 三种元素中,原子半径最大的是
三种元素中,原子半径最大的是(2)写出
 与
与 两元素最高价氧化物对应水化物反应的离子方程式:
两元素最高价氧化物对应水化物反应的离子方程式:(3)这八种元素中非金属性最强的元素是
(4)写出
 、
、 两元素形成的原子个数比为
两元素形成的原子个数比为 的物质的电子式:
的物质的电子式:(5)
 的氢化物属于
的氢化物属于该氢化物与水反应的化学方程式为
(6)
 和
和 两种元素形成的简单氢化物的稳定性
两种元素形成的简单氢化物的稳定性
 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近半年使用:0次
10 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近半年使用:0次



