解题方法
1 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:_____________ (填具体元素符号,下同),原子结构示意图为_____________ 。元素⑩名称为_____________ ,在周期表中的位置_________________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_________________ ,碱性最强的化合物的电子式是:_________________________ 。
(3)用电子式表示元素②的常见单质_____________ 其结构式为_________________ 。
(4)表示①与⑦的化合物的电子式为_________________ ,该化合物是由_____________ (填“极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是_________ 。
(6)元素③的简单氢化物的结构式为_____________________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为 _____________________ 。
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素②的常见单质
(4)表示①与⑦的化合物的电子式为
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式为
您最近半年使用:0次
名校
解题方法
2 . X、Y、Z、W四种元素的原子序数依次增大,X单质有多种同素异形体,有的能导电、有的不导电,Y元素原子M层电子数比K层少1,Z原子有四个电子层、位于周期表第8列,人体缺少W元素易患甲状腺肿大。下列说法不正确 的是
| A.某种X元素单质能使氯水褪色,是利用它的还原性 |
| B.Y是金属元素,能使火焰颜色变为黄色 |
| C.Z元素在周期表所处的族是Ⅷ,属于过渡金属 |
| D.W元素的单质常温下紫黑色固体,受热易升华 |
您最近半年使用:0次
名校
解题方法
3 . 已知 A、B、C、D、E 是原子序数依次增大前四周期元素,其元素性质或原子结构如表:
(1)A的最高价氧化物是___________ 分子。(填“极性”或“非极性”)该分子的杂化类型是___________
(2)B与其同周期相邻元素第一电离能由大到小的顺序为___________ (填元素符号)。B2O分子的空间构型是___________
(3)C气态氢化物稳定性是同族元素氢化物中最高的,其原因是___________ 。
(4)D 属于___________ 区的元素,该元素原子核外电子占据的最高能层符号是___________ 其基态原子的价层电子轨道表示式为___________ 。
(5)E 的基态原子的电子排布式为___________ 。E-e-=E+的过程中,失去的电子是基态E 中___________ 轨道上的电子。
| A | 原子核外电子分占 3 个不同能级, 且每个能级上排布的电子数相同 |
| B | 原子最高能级的不同轨道都有电子, 且自旋方向相同 |
| C | 在周期表所有元素中电负性最大 |
| D | 位于周期表中第 4 纵列 |
| E | 基态原子 M 层全充满, N 层只有一个电子 |
(2)B与其同周期相邻元素第一电离能由大到小的顺序为
(3)C气态氢化物稳定性是同族元素氢化物中最高的,其原因是
(4)D 属于
(5)E 的基态原子的电子排布式为
您最近半年使用:0次
2024-04-27更新
|
58次组卷
|
2卷引用:福建省福州第二中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
4 . 如表列出了①-⑧八种元素在周期表中的位置:
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是_____ (填写化学式)。
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为______ (用元素符号表示)。
(3)元素①的气态氢化物的电子式是______ ,实验室常用稀硫酸吸收过量的该气体,防止污染环境。写出反应的化学方程式为_______ 。
(4)元素⑤的最高价氧化物的结构式为_______ 。
(5)元素④的最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式为_____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑦ | |||
| 4 | ⑥ | ⑧ |
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为
(3)元素①的气态氢化物的电子式是
(4)元素⑤的最高价氧化物的结构式为
(5)元素④的最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式为
您最近半年使用:0次
5 . X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,X最外层电子数是内层电子数的2倍,Y的单质与氢气在暗处能剧烈化合并发生爆炸,Z短周期元素中原子半径最大,W其氧化物是两性氧化物,Q同周期元素中,最高价氧化物对应水化物的酸性最强。
(1)元素Y在元素周期表中的位置是___________ 。
(2)Z在氧气中完全燃烧的产物的化学式为___________ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。___________ 、___________ ;M为___________ (填化学式),其作用是___________ 。
②能说明X元素的非金属性比硅元素强的实验现象是___________ 。
(5)元素Z与W相比,金属性较弱的是___________ (填元素名称),请写出能证明这一结论的实验事实___________ 。(列举一条)
(1)元素Y在元素周期表中的位置是
(2)Z在氧气中完全燃烧的产物的化学式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较弱的是
您最近半年使用:0次
名校
解题方法
6 . X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期位置相邻,Y、Z同主族,Z、W位置相邻。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是
A.原子半径: |
B.最高价氧化物对应水化物的酸性: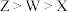 |
| C.4种元素的单质中,Z单质的熔、沸点最高 |
| D.W单质是一种具有漂白性的物质 |
您最近半年使用:0次
名校
7 . 已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法正确的是
| A.原子半径:Z>W>R>X |
| B.对应气态氢化物的热稳定性:W>R>Y |
| C.W与Y、Z与R形成的化合物微粒组成比相同 |
| D.W与R的氧化物对应的水化物是强酸 |
您最近半年使用:0次
解题方法
8 . 短周期主族元素M、E、X、Y、Z原子序数依次增大,其中M、E、Z位于同一主族,X原子最外层电子数比次外层的多1,Y元素的第一电离能比周期表中位置相邻元素的大。下列说法正确的是
| A.原子半径:X>Y>Z>M |
| B.电负性:M>X>Y>Z |
| C.X、Y、Z分别与M形成简单化合物,熔点最高的为Z |
| D.E、Z的最高价氧化物对应水化物的碱性:E>Z |
您最近半年使用:0次
解题方法
9 . 已知Te为第五周期第ⅥA族元素。下列结论错误的是
A.粒子半径: |
B.氧化性: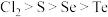 |
C.酸性: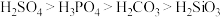 |
D.金属性: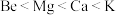 |
您最近半年使用:0次
2024-03-09更新
|
231次组卷
|
4卷引用:福建省漳州市第五中学2023-2024学年高一下学期第一次月考化学试卷
名校
解题方法
10 . 根据元素周期律,由下列事实进行归纳推测,推测不合理的是
| 事实 | 推测 | |
| A |  可以和NaBr溶液反应生成 可以和NaBr溶液反应生成 |  可以和NaCl溶液反应生成 可以和NaCl溶液反应生成 |
| B | Si与 高温时反应,S与 高温时反应,S与 加热能反应 加热能反应 | P与 在高温时能反应 在高温时能反应 |
| C |  与水反应缓慢, 与水反应缓慢,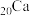 与水反应较快 与水反应较快 | 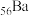 (ⅡA族)与水反应会更快 (ⅡA族)与水反应会更快 |
| D | HCl在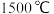 时分解,HI在 时分解,HI在 时分解 时分解 | HBr的分解温度介于二者之间 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-03-03更新
|
133次组卷
|
3卷引用:福建省厦门英才学校2023-2024学年高一下学期3月月考化学试卷



