如表列出了①-⑧八种元素在周期表中的位置:
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是_____ (填写化学式)。
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为______ (用元素符号表示)。
(3)元素①的气态氢化物的电子式是______ ,实验室常用稀硫酸吸收过量的该气体,防止污染环境。写出反应的化学方程式为_______ 。
(4)元素⑤的最高价氧化物的结构式为_______ 。
(5)元素④的最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式为_____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑦ | |||
| 4 | ⑥ | ⑧ |
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为
(3)元素①的气态氢化物的电子式是
(4)元素⑤的最高价氧化物的结构式为
(5)元素④的最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式为
更新时间:2024-04-16 18:40:59
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】胃酸过多是常见的胃病。下面是甲、乙两种常见胃药的说明摘要。
甲:(1)白色结晶状粉末,可缓缓分解;(2)能溶于水,水溶液呈弱碱性;(3)遇酸及酸性药物则产生二氧化碳;(4)胃酸过多患者服用多见胃胀气,甚至有引起胃穿孔的危险。
乙:(1)与胃酸的中和作用缓慢而持久,可维持3~4小时;(2)凝胶本身覆盖于溃疡面上,具有保护作用;(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是______ (填化学式);乙中含有的主要化学成分是__________ (填化学式)。
(2)试写出甲中含有的主要化学成分引起胃胀气反应的离子方程式:_________ 。
(3)试写出乙中含有的主要化学成分分别与稀盐酸和氢氧化钠溶液反应的离子方程式:___ 。
甲:(1)白色结晶状粉末,可缓缓分解;(2)能溶于水,水溶液呈弱碱性;(3)遇酸及酸性药物则产生二氧化碳;(4)胃酸过多患者服用多见胃胀气,甚至有引起胃穿孔的危险。
乙:(1)与胃酸的中和作用缓慢而持久,可维持3~4小时;(2)凝胶本身覆盖于溃疡面上,具有保护作用;(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是
(2)试写出甲中含有的主要化学成分引起胃胀气反应的离子方程式:
(3)试写出乙中含有的主要化学成分分别与稀盐酸和氢氧化钠溶液反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图是元素周期表的一部分,其中所列的字母分别代表某一化学元素。
(1)硒是人体的微量元素之一,可保护细胞组织,请在周期表中标出元素符号_______ 。
(2)比较元素c、d、e、f的离子半径,由大到小的顺序是_______ (填离子符号)。
(3)根据核外电子的排布分区,字母g属于_______ 区元素,该区的价层电子通式为_______ 。
(4)位于金属元素与非金属元素分界线上的元素常被称为半金属或类金属,其单质及化合物有一定特殊性,如ef3为_______ (填“离子化合物”或“共价化合物”),元素e的最高价氧化物对应的水化物与强碱反应的离子方程式是_______ 。
(5)第VIIA的元素组成的单质,从上到下熔沸点逐渐升高,其原因是_______ 。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | ||||||||||||||
(2)比较元素c、d、e、f的离子半径,由大到小的顺序是
(3)根据核外电子的排布分区,字母g属于
(4)位于金属元素与非金属元素分界线上的元素常被称为半金属或类金属,其单质及化合物有一定特殊性,如ef3为
(5)第VIIA的元素组成的单质,从上到下熔沸点逐渐升高,其原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某无色稀溶液X中,可能含有下表所列离子中的某几种。
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。

(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是________________ ,ab段发生反应的离子是________ ,bc段发生反应的离子方程式为__________ 。
(2)若Y是NaOH溶液,则X中一定含有的阳离子是_____________ ,其物质的量之比为_________ ,ab段反应的离子方程式为____________ 。
| 阴离子 | CO 、SiO 、SiO 、AlO 、AlO 、Cl- 、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH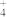 、Na+ 、Na+ |

(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是
(2)若Y是NaOH溶液,则X中一定含有的阳离子是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大且总和为24。则W、X、Y、Z分别为___________ 。


您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】黑火药爆炸时发生化学反应:S+2KNO 3+3C →K2S+3CO2↑+N2↑,完成下列填空:
(1)上述反应中,还原剂是____________ ,属于第三周期的元素是_____________ 。
(2)上述反应的生成物中,属于共价化合物的是_____________________ ,属于离子化合物的是___________________ ,N2的电子式是____________________ 。
(3)写出K、N最高价氧化物对应的水化物之间发生反应的化学方程式。_________________ 。
(1)上述反应中,还原剂是
(2)上述反应的生成物中,属于共价化合物的是
(3)写出K、N最高价氧化物对应的水化物之间发生反应的化学方程式。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】大多数金属硫化物难溶于水,可溶于硝酸。例如:
①FeS +HNO3(稀)→Fe(NO3)3 +NO↑+S↓+H2O(未配平)
②CuS +HNO3(浓)→CuSO4 +NO2↑+H2O(未配平)
(1)配平反应②的方程式:
__ CuS +__ HNO3(浓)→__ CuSO4 +__ NO2↑+__ H2O
(2)反应①中若生成3.2g硫,则电子转移___ 个。
(3)由反应①和②是否能够判断稀硝酸与浓硝酸的氧化性强弱?并说明判断依据。____ 。
(4)反应①和②所涉及的4种非金属元素中,原子半径由大到小的顺序是____ ;未成对电子最多的原子核外电子排布式为___ 。
下列描述,不能用来比较硫、氮两种元素的非金属性强弱的是___ 。
a.单质与氧气化合的难易程度 b.气态氢化物的稳定性
c.含氧酸的酸性强弱 d.S4N4中共用电子对的偏向
(5)写出①NO ②S ③H2O ④NO2四种物质的沸点由高到低的顺序(用编号回答)____ 。若要判断NO2分子的极性,你所需要的信息是___ 。
①FeS +HNO3(稀)→Fe(NO3)3 +NO↑+S↓+H2O(未配平)
②CuS +HNO3(浓)→CuSO4 +NO2↑+H2O(未配平)
(1)配平反应②的方程式:
(2)反应①中若生成3.2g硫,则电子转移
(3)由反应①和②是否能够判断稀硝酸与浓硝酸的氧化性强弱?并说明判断依据。
(4)反应①和②所涉及的4种非金属元素中,原子半径由大到小的顺序是
下列描述,不能用来比较硫、氮两种元素的非金属性强弱的是
a.单质与氧气化合的难易程度 b.气态氢化物的稳定性
c.含氧酸的酸性强弱 d.S4N4中共用电子对的偏向
(5)写出①NO ②S ③H2O ④NO2四种物质的沸点由高到低的顺序(用编号回答)
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已知A、D位于同一主族,D是短周期中原子半径最大的。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是___________ (用元素符号填写)。
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写)。
(3)下列事实能说明G元素的非金属性比F元素的非金属性强的是(填序号)______
A.G单质与Na2S溶液反应溶液变浑浊
B.F的氢化物的酸性比G的氢化物酸性弱
C.G和F两元素的简单氢化物受热分解,前者的分解温度高
(4)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是___________ 。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是
(3)下列事实能说明G元素的非金属性比F元素的非金属性强的是(填序号)
A.G单质与Na2S溶液反应溶液变浑浊
B.F的氢化物的酸性比G的氢化物酸性弱
C.G和F两元素的简单氢化物受热分解,前者的分解温度高
(4)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑩九种元素在周期表中的位置。
请回答:
(1)在表里所列元素中,最高价氧化物对应的水化物中,酸性最强的是________ (填化学式 )。
(2)在②③④三种元素的最高价氧化物对应的水化物中,碱性最强 的是_______ (填化学式 )。电子式:________ 。
(3)⑦⑧⑨形成的气态氢化物中,最稳定的是________ (填化学式 )。
(4)元素⑥的氢化物的化学式是________ ,电子式:________
(5)⑧元素与②元素形成的化合物的电子式:________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ⑩ | ||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑤ | ⑨ |
请回答:
(1)在表里所列元素中,最高价氧化物对应的水化物中,酸性最强的是
(2)在②③④三种元素的最高价氧化物对应的水化物中,
(3)⑦⑧⑨形成的气态氢化物中,最稳定的是
(4)元素⑥的氢化物的化学式是
(5)⑧元素与②元素形成的化合物的电子式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A,C同周期,B,C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1)写出五种元素的元素符号:A:________ 、B:________ 、C:________ 、D:________ 、E:________ 。
(2)用电子式表示离子化合物A2B的形成过程:______________________ 。
(3)写出下列物质的电子式:
①D元素形成的单质:_______________________________________________ 。
②E与B形成的化合物:_____________________________________________ 。
③A,B,E形成的化合物:___________________________________________ 。
④D与E形成的化合物:______________________________________________ 。
⑤C,D,E形成的离子化合物:________________________________________ 。
(1)写出五种元素的元素符号:A:
(2)用电子式表示离子化合物A2B的形成过程:
(3)写出下列物质的电子式:
①D元素形成的单质:
②E与B形成的化合物:
③A,B,E形成的化合物:
④D与E形成的化合物:
⑤C,D,E形成的离子化合物:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H除外):____ ,所含元素的原子半径由小到大的顺序:_____ ,Mg在元素周期表中的位置:_______ ,Mg(OH)2的电子式:_____
(2)在NaCl、NaOH、N2、H2S中,只含有离子键的是____ ,仅含有共价键的化合物是_______
(3)用电子式表示MgCl2的形成过程___________
(4)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净,干燥后称重,总质量为47g,则产生氢气的体积___ mL(标准状况)
(2)在NaCl、NaOH、N2、H2S中,只含有离子键的是
(3)用电子式表示MgCl2的形成过程
(4)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净,干燥后称重,总质量为47g,则产生氢气的体积
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】人体含氧65%、碳18%、氢10%、氮3%、钙1.5%、磷1%、钾0.35%、硫0.25%、钠0.15%、氯0.15%、镁0.05%(均以质量计),它们被称为人体常量元素。
(1)上述常量元素中,从周期表来看,元素种类最多族为_______ 族。
(2)以上属于第三周期的非金属元素的原子半径由大到小的顺序_______ (填元素符号)。
(3)人体还有许多微量元素,如:锶(Sr),锶位于元素周期表的第五周期ⅡA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。
①在上述反应体系中出现的几种短周期元素中非金属性最强的是_______ (填元素符号)。
②反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式_______ 。
③已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号_______ 。
④下列关于锶及其化合物的叙述中,错误的是_______ 。
a.锶的金属性比镁强 b.氢氢化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(1)上述常量元素中,从周期表来看,元素种类最多族为
(2)以上属于第三周期的非金属元素的原子半径由大到小的顺序
(3)人体还有许多微量元素,如:锶(Sr),锶位于元素周期表的第五周期ⅡA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。
①在上述反应体系中出现的几种短周期元素中非金属性最强的是
②反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式
③已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号
④下列关于锶及其化合物的叙述中,错误的是
a.锶的金属性比镁强 b.氢氢化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
您最近半年使用:0次



