名校
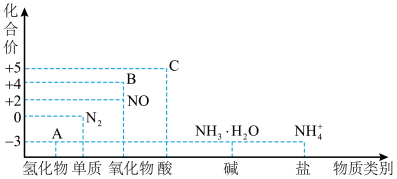
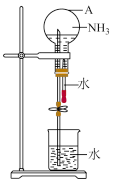
1 . 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价——物质类别关系如图。回答下列问题:___________ (填化学式),常用作制冷剂的物质是___________ (填名称)
(2)实验室以 固体为主要原料制备
固体为主要原料制备 气体,其化学方程式为
气体,其化学方程式为___________
(3)欲吸收尾气中的A,下列装置中不可选用___________ (填字母)。(已知 难溶于
难溶于 )
)___________ (填字母)。 和水 b.
和水 b. 和饱和
和饱和 溶液
溶液
c. 和浓
和浓 溶液 d.
溶液 d. 和水
和水
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究的成果用于汽车尾气处理中,在催化剂存在下可将 和
和 反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
反应转化为两种无色无毒气体,用化学反应方程式表示这个过程___________ 。
(6)在标准状况下进行如下反应,将一定量的铜粉投入一定量浓 中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由
中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由 、
、 、
、 等组成的含氮混合气体,这些混合气体与
等组成的含氮混合气体,这些混合气体与 氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为
氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为___________  。
。
(2)实验室以
 固体为主要原料制备
固体为主要原料制备 气体,其化学方程式为
气体,其化学方程式为(3)欲吸收尾气中的A,下列装置中不可选用
 难溶于
难溶于 )
)a. b.
b.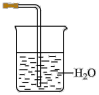 c.
c.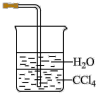 d.
d.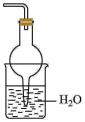
 和水 b.
和水 b. 和饱和
和饱和 溶液
溶液c.
 和浓
和浓 溶液 d.
溶液 d. 和水
和水(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究的成果用于汽车尾气处理中,在催化剂存在下可将
 和
和 反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
反应转化为两种无色无毒气体,用化学反应方程式表示这个过程(6)在标准状况下进行如下反应,将一定量的铜粉投入一定量浓
 中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由
中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由 、
、 、
、 等组成的含氮混合气体,这些混合气体与
等组成的含氮混合气体,这些混合气体与 氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为
氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为 。
。
您最近半年使用:0次
名校
2 . 无机物 均为短周期元素组成的物质,且均含有同种元素,其中
均为短周期元素组成的物质,且均含有同种元素,其中 是最简单氢化物、
是最简单氢化物、 是单质:上述物质在一定条件下可以发生如下转化。
是单质:上述物质在一定条件下可以发生如下转化。 为强碱,则
为强碱,则 的电子式为
的电子式为___________ 。
(2)若 为二元弱酸,则
为二元弱酸,则 的化学式为
的化学式为___________ 。
(3)若 为强酸,
为强酸, 在标准状况下是白色固体,则:
在标准状况下是白色固体,则:
① 的浓溶液与炭反应的化学方程式
的浓溶液与炭反应的化学方程式___________ 。
② 溶于水显酸性的原因(化学原理)是
溶于水显酸性的原因(化学原理)是___________ 。
(4)若 为强酸,且
为强酸,且 和
和 可以发生反应生成一种盐
可以发生反应生成一种盐 ,则:
,则:
① 的催化氧化是工业上制备硝酸的基础,其化学方程式
的催化氧化是工业上制备硝酸的基础,其化学方程式___________ 。
②实验室检验 中阳离子的离子方程式为
中阳离子的离子方程式为___________ 。
 均为短周期元素组成的物质,且均含有同种元素,其中
均为短周期元素组成的物质,且均含有同种元素,其中 是最简单氢化物、
是最简单氢化物、 是单质:上述物质在一定条件下可以发生如下转化。
是单质:上述物质在一定条件下可以发生如下转化。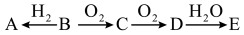
 为强碱,则
为强碱,则 的电子式为
的电子式为(2)若
 为二元弱酸,则
为二元弱酸,则 的化学式为
的化学式为(3)若
 为强酸,
为强酸, 在标准状况下是白色固体,则:
在标准状况下是白色固体,则:①
 的浓溶液与炭反应的化学方程式
的浓溶液与炭反应的化学方程式②
 溶于水显酸性的原因(化学原理)是
溶于水显酸性的原因(化学原理)是(4)若
 为强酸,且
为强酸,且 和
和 可以发生反应生成一种盐
可以发生反应生成一种盐 ,则:
,则:①
 的催化氧化是工业上制备硝酸的基础,其化学方程式
的催化氧化是工业上制备硝酸的基础,其化学方程式②实验室检验
 中阳离子的离子方程式为
中阳离子的离子方程式为
您最近半年使用:0次
名校
3 . 下列实验操作、现象和结论都正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向某溶液中加入 溶液并加热,产生能使湿润蓝色石蕊试纸变红的气体 溶液并加热,产生能使湿润蓝色石蕊试纸变红的气体 | 该溶液中一定含有 |
| B | 室温下,向 溶液中滴加少量 溶液中滴加少量 溶液,再滴加几滴淀粉溶液,溶液变蓝色 溶液,再滴加几滴淀粉溶液,溶液变蓝色 |  的氧化性比 的氧化性比 的强 的强 |
| C | 向溶液中加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失 | 一定有 |
| D | 向某溶液中加入少量新制氯水后再加几滴 溶液,溶液变为红色 溶液,溶液变为红色 | 该溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列实验装置或方案能达到实验目的的是
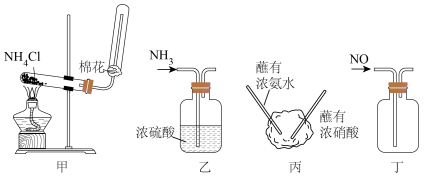
| A.用装置甲制取氨气 | B.用装置乙除去氨气中的水蒸气 |
C.丙的原理为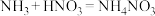 | D.收集 气体 气体 |
您最近半年使用:0次
5 . 下列表示对应化学反应的离子方程式正确的是
A.足量铁粉加入稀硝酸中: |
B.将 通入到 通入到 溶液中: 溶液中: |
C. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
D.向 溶液中通入 溶液中通入 气体使溶液棕黄色变浅: 气体使溶液棕黄色变浅: |
您最近半年使用:0次
6 . 下列关于 和
和 的说法正确的是
的说法正确的是
 和
和 的说法正确的是
的说法正确的是A. 是红棕色气体,易溶于水反应生成酸,属于酸性氧化物 是红棕色气体,易溶于水反应生成酸,属于酸性氧化物 |
B. 与水的反应中, 与水的反应中, 是还原剂 是还原剂 |
C. 和 和 以一定比例混合可以被水完全吸收转化成 以一定比例混合可以被水完全吸收转化成 |
D.从元素化合价角度看, 只有还原性 只有还原性 |
您最近半年使用:0次
名校
7 . 氮是各种生物体生命活动不可缺少的重要元素,下列过程属于氮的固定的是
| A.在一定条件下由氨气和二氧化碳合成尿素 |
| B.雷雨闪电时,大气中产生了一氧化氮 |
| C.氯化铵受热分解生成氨气和氯化氢 |
| D.工业上用氨气和硝酸合成硝酸铵 |
您最近半年使用:0次
名校
8 . 乙研究小组为了利用稀硫酸制备 ,进行了如图所示的实验设计。
,进行了如图所示的实验设计。 能加快生成
能加快生成 的反应速率,发挥作用的原理可表述为:
的反应速率,发挥作用的原理可表述为:
①
②……
(1)反应②的离子方程式 为______________ 。
(2)某小组通过向铜和稀硫酸的混合物中加入过氧化氢的方法制备硫酸铜,但是在实际操作时,发现所消耗的 的量往往会大于理论值,原因是
的量往往会大于理论值,原因是__________ 。
取 晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。
晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。 时,固体的成分为
时,固体的成分为________ (写出计算步骤 )。
(4)当剩余固体为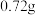 时,加热的温度不能低于
时,加热的温度不能低于_____ ℃,如果此时产生的气体中含有 ,请写出
,请写出 受热分解的化学方程式
受热分解的化学方程式________ 。
 ,进行了如图所示的实验设计。
,进行了如图所示的实验设计。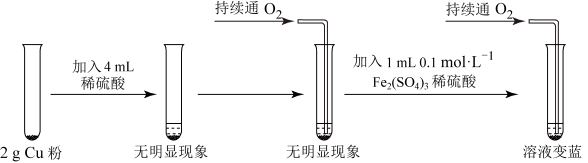
 能加快生成
能加快生成 的反应速率,发挥作用的原理可表述为:
的反应速率,发挥作用的原理可表述为:①

②……
(1)反应②的
(2)某小组通过向铜和稀硫酸的混合物中加入过氧化氢的方法制备硫酸铜,但是在实际操作时,发现所消耗的
 的量往往会大于理论值,原因是
的量往往会大于理论值,原因是取
 晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。
晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。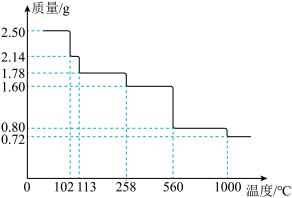
 时,固体的成分为
时,固体的成分为(4)当剩余固体为
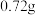 时,加热的温度不能低于
时,加热的温度不能低于 ,请写出
,请写出 受热分解的化学方程式
受热分解的化学方程式
您最近半年使用:0次
名校
解题方法
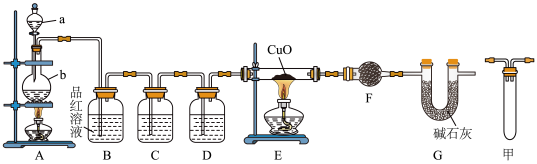
9 . 甲研究小组按如图装置进行实验,验证锌与浓硫酸反应生成物中的气体成分,取足量的Zn置于b中,向a中加入适量浓硫酸,经过一段时间的反应,Zn仍有剩余。______ ,仪器b的名称是_______ 。
(2)在反应初始阶段 ,装置A中发生的化学方程式为__________ 。
(3)装置C中若为酸性高锰酸钾溶液,则对应的离子方程式 为____________ 。
(4)装置F的名称为球形干燥管,其中加入的试剂是_______ ,作用为________ 。
(5)有同学认为A、B间应增加图中的甲装置,该装置的作用为________ 。
(2)在
(3)装置C中若为酸性高锰酸钾溶液,则对应的
(4)装置F的名称为球形干燥管,其中加入的试剂是
(5)有同学认为A、B间应增加图中的甲装置,该装置的作用为
您最近半年使用:0次
名校
解题方法
10 . 室温下,下列实验探究方案不能 达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向盛有FeSO4溶液的试管中滴加几滴KSCN溶液,振荡,再滴加几滴新制氯水,观察溶液颜色变化 | Fe2+具有还原性 |
| B | 向盛有SO2水溶液的试管中滴加几滴品红溶液并振荡,加热试管,观察溶液颜色变化 | SO2具有漂白性 |
| C | 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 | Br2的氧化性比I2的强 |
| D | 用pH计测量碳酸和亚硫酸的pH,比较溶液pH大小 | 酸性:碳酸弱于亚硫酸 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



