名校
解题方法
1 . 利用压强传感器测定氨气的喷泉实验中的压强变化。___________ 。
(2)可以用___________ 试纸置于三颈瓶口c处验满。
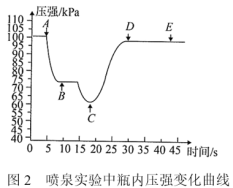
(3)关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,___________ 点时喷泉最剧烈(选填A、B、C、D、E)。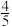 且混合均匀,实验开始前烧瓶中气体的平均分子量为
且混合均匀,实验开始前烧瓶中气体的平均分子量为___________ ,实验结束后烧瓶中溶液的物质的量浓度为___________ mol/L。
(2)可以用
(3)关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,
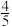 且混合均匀,实验开始前烧瓶中气体的平均分子量为
且混合均匀,实验开始前烧瓶中气体的平均分子量为
您最近半年使用:0次
名校
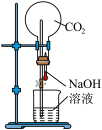
2 . 下列关于喷泉实验的说法错误的是

| A.甲、乙和丙三个装置必须要用极易溶于水的气体才能完成喷泉实验 |
| B.甲装置烧瓶中装满纯净干燥的氨气,挤压胶头滴管,打开止水夹,可引发喷泉 |
| C.乙装置中的液体为NaOH溶液时,气体可以是CO2、SO2、Cl2、NO2等 |
| D.丙装置的原理是锥形瓶中产生不溶于水的气体,气压增大,液体迅速流入烧瓶,形成喷泉 |
您最近半年使用:0次
名校
解题方法
3 . 标准状况下,通过喷泉实验可以验证气体是否极易溶于水。装置中烧杯内的水均为足量,下列有关喷泉实验描述中正确的是
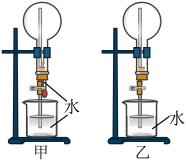
A.若甲装置中收集满NO2与O2的混合气体,且V(NO2):V(O2)=4:1,则进行喷泉实验后所得溶液的浓度为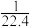 mol/L mol/L |
B.若甲装置中收集满NO2,则进行喷泉实验后所得溶液充满烧瓶且浓度为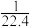 mol/L mol/L |
| C.若乙装置烧瓶内充满Cl2,将烧杯内的水换成饱和食盐水,也能完成喷泉实验 |
| D.若乙装置中装满NH3,则引发喷泉的操作为打开止水夹并用热毛巾敷圆底烧瓶 |
您最近半年使用:0次
名校
4 . 喷泉实验的改进实验装置如图所示。常温常压下,在X、Y处分别通入等体积的气体后,关闭X、Y处止水夹,打开止水夹c,能出现喷泉现象的是
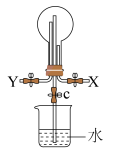
| 选项 | X | Y |
| A |  |  |
| B |  |  |
| C |  |  |
| D |  | NO |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 某兴趣小组利用下列装置进行实验,其中能达到实验目的的是
|
|
|
|
| A.喷泉实验 | B.验证压强对平衡的影响 | C.制备 | D.制取无水 固体 固体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
6 . 含氮化合物在工农业有着重要的用途。
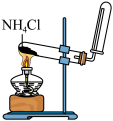
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为____________ 。
(2)预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:a→______ (按气流方向,用小写字母表示)。
(3)请写出氨气的检验方法:____________ 。
(4)甲、乙两同学分别设计了下图装备进行喷泉实验,____________ 。
②乙同学想用乙装备在两个烧瓶同时产生喷泉,引发双喷泉的操作是:______ —______ 。
Ⅱ. 经一系列反应可以得到
经一系列反应可以得到 。
。
(5)①中, 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是____________ 。
(6)NO的检验方法是:____________ 。
Ⅲ.研究 、
、 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。
(7)选择性催化还原技术(SCR)可使 与
与 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:____________ 。
(8)大气污染物中的氮氧化物地可用NaOH吸收,先后发生如下反应:
 ;
; 。
。
若33.6 mL(标况下)氮氧化物(只含NO和 )与V mL0.1 mol/L NaOH溶液恰好完全反应,则
)与V mL0.1 mol/L NaOH溶液恰好完全反应,则
______ 。
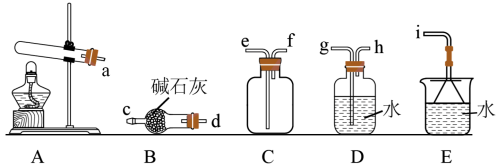
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为
(2)预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:a→
(3)请写出氨气的检验方法:
(4)甲、乙两同学分别设计了下图装备进行喷泉实验,
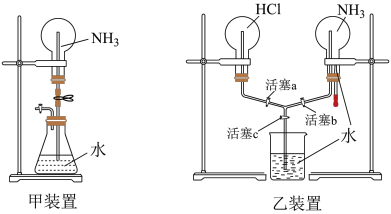
②乙同学想用乙装备在两个烧瓶同时产生喷泉,引发双喷泉的操作是:
Ⅱ.
 经一系列反应可以得到
经一系列反应可以得到 。
。
(5)①中,
 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是(6)NO的检验方法是:
Ⅲ.研究
 、
、 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。(7)选择性催化还原技术(SCR)可使
 与
与 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:(8)大气污染物中的氮氧化物地可用NaOH吸收,先后发生如下反应:
 ;
; 。
。若33.6 mL(标况下)氮氧化物(只含NO和
 )与V mL0.1 mol/L NaOH溶液恰好完全反应,则
)与V mL0.1 mol/L NaOH溶液恰好完全反应,则
您最近半年使用:0次
名校
7 . 用充有NH3的烧瓶进行“喷泉实验”,装置及现象如下图。下列关于该实验的分析正确的是
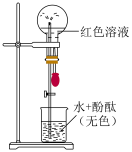
| A.产生“喷泉”证明NH3与H2O发生了反应 |
| B.无色溶液变红证明NH3极易溶于水 |
| C.烧瓶中剩余少量气体,证明NH3溶解已达饱和 |
| D.加热红色溶液可观察到红色变浅或褪去 |
您最近半年使用:0次
名校
8 . 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价——物质类别关系如图。回答下列问题:___________ (填化学式),常用作制冷剂的物质是___________ (填名称)
(2)实验室以 固体为主要原料制备
固体为主要原料制备 气体,其化学方程式为
气体,其化学方程式为___________
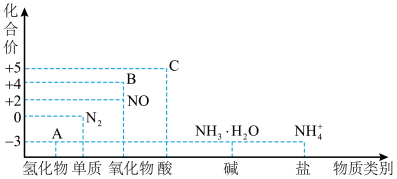
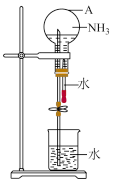
(3)欲吸收尾气中的A,下列装置中不可选用___________ (填字母)。(已知 难溶于
难溶于 )
)___________ (填字母)。 和水 b.
和水 b. 和饱和
和饱和 溶液
溶液
c. 和浓
和浓 溶液 d.
溶液 d. 和水
和水
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究的成果用于汽车尾气处理中,在催化剂存在下可将 和
和 反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
反应转化为两种无色无毒气体,用化学反应方程式表示这个过程___________ 。
(6)在标准状况下进行如下反应,将一定量的铜粉投入一定量浓 中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由
中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由 、
、 、
、 等组成的含氮混合气体,这些混合气体与
等组成的含氮混合气体,这些混合气体与 氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为
氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为___________  。
。
(2)实验室以
 固体为主要原料制备
固体为主要原料制备 气体,其化学方程式为
气体,其化学方程式为(3)欲吸收尾气中的A,下列装置中不可选用
 难溶于
难溶于 )
)a. b.
b.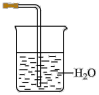 c.
c.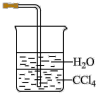 d.
d.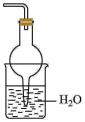
 和水 b.
和水 b. 和饱和
和饱和 溶液
溶液c.
 和浓
和浓 溶液 d.
溶液 d. 和水
和水(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究的成果用于汽车尾气处理中,在催化剂存在下可将
 和
和 反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
反应转化为两种无色无毒气体,用化学反应方程式表示这个过程(6)在标准状况下进行如下反应,将一定量的铜粉投入一定量浓
 中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由
中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由 、
、 、
、 等组成的含氮混合气体,这些混合气体与
等组成的含氮混合气体,这些混合气体与 氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为
氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为 。
。
您最近半年使用:0次
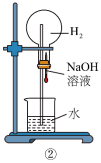
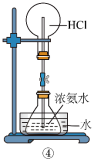
9 . 下图是课外活动小组的同学设计的4个喷泉实验方案,下列有关操作不可能引发喷泉的是
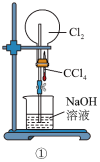
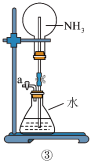
A.先打开止水夹再挤压装置①的胶头滴管使 全部进入烧瓶 全部进入烧瓶 |
B.先打开止水夹再挤压装置②的胶头滴管使 溶液全部进入烧瓶 溶液全部进入烧瓶 |
| C.先打开止水夹然后用鼓气装置从装置③的a处不断鼓入空气 |
| D.先打开止水夹然后在装置④的水槽中慢慢加入足量浓硫酸 |
您最近半年使用:0次
名校
10 . 利用氨的催化氧化原理制备硝酸并进行喷泉实验,装置如图所示(省略夹持装置),下列说法正确的是

A.可以利用 制备氨气 制备氨气 |
| B.一段时间后,可以在圆底烧瓶观察到无色喷泉 |
C.若要液体充满圆底烧瓶,理论上通入的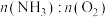 小于1∶2 小于1∶2 |
D.1mol  完全转化为硝酸,转移电子的数目为8 完全转化为硝酸,转移电子的数目为8 |
您最近半年使用:0次