名校
1 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.32g  中所含共价键数目为 中所含共价键数目为 |
B.0.1  溶液中所含 溶液中所含 数目少于0.1 数目少于0.1 |
C.标准状况下,22.4L  溶于足量NaOH溶液中,转移电子数目为2 溶于足量NaOH溶液中,转移电子数目为2 |
D.将10g铁粉加入稀硝酸中,最终有4.4g铁未溶解,该过程中转移电子数目为0.3 |
您最近半年使用:0次
名校
解题方法
2 . 某处工厂排出的烟道气中含氮氧化物(主要为NO、 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式______________ ;若反应后尾气无残留,则参加反应的 、NO物质的量比值为
、NO物质的量比值为_____ (填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(4)有氧条件下,NO在催化剂作用下可被 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是___________ 。
(5)羟基自由基( )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程:______________ 。 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加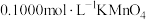 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗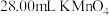 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数__________ 。(写出计算过程)
 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: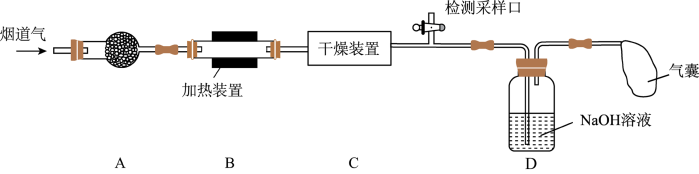
 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式 、NO物质的量比值为
、NO物质的量比值为a.≥1 b.≤1 c.任意值
(2)可使用适量酸性
 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性
 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是(4)有氧条件下,NO在催化剂作用下可被
 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: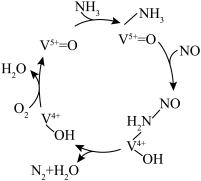
 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是(5)羟基自由基(
 )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程: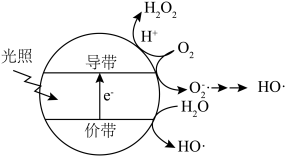
 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加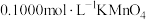 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗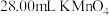 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数
您最近半年使用:0次
名校
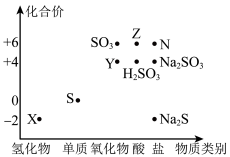
3 . 请根据硫元素的价类二维图,回答下列问题:___________ 。
(2)宋代著名法医学家宋慈的 洗冤集录
洗冤集录 中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法
中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法错误 的是___________(填字母)。
(3)Y转化为Z可以选择下列试剂___________ 。写出你所选试剂将Y转化为Z的离子方程式___________ 。
A.酸性KMnO4溶液 B.FeCl2溶液 C.NaOH溶液 D.X的水溶液
(4)若N是CuSO4,某同学设计了甲和乙两种方法制备:
甲: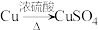 乙:
乙:
①写出甲方法反应的化学方程式:___________ 。
②甲和乙方法更合理的是___________ (填“甲”或“乙”),理由是(答两点) ___________ 。
(5)电化学法处理 是目前研究的热点。利用过氧化氢吸收
是目前研究的热点。利用过氧化氢吸收 可消除
可消除 污染,设计装置如图所示。
污染,设计装置如图所示。___________ 。
②石墨2电极处发生的电极反应式为___________ 。
(6)已知空气中SO2的最大允许排放浓度不得超过0.02 mg•L-1,可通过下列装置定量分析空气中SO2的含量。___________ mg•L-1(结果精确到0.001)。
(2)宋代著名法医学家宋慈的
 洗冤集录
洗冤集录 中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法
中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法| A.当银针变黑时,说明所检验的物质中可能有毒 |
| B.银针验毒时,Ag被氧化 |
| C.X在上述验毒反应中作还原剂 |
| D.上述验毒反应中氧化剂和还原剂的物质的量之比为4∶1 |
(3)Y转化为Z可以选择下列试剂
A.酸性KMnO4溶液 B.FeCl2溶液 C.NaOH溶液 D.X的水溶液
(4)若N是CuSO4,某同学设计了甲和乙两种方法制备:
甲:
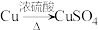 乙:
乙:
①写出甲方法反应的化学方程式:
②甲和乙方法更合理的是
(5)电化学法处理
 是目前研究的热点。利用过氧化氢吸收
是目前研究的热点。利用过氧化氢吸收 可消除
可消除 污染,设计装置如图所示。
污染,设计装置如图所示。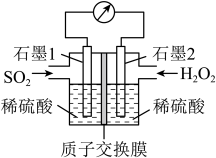
②石墨2电极处发生的电极反应式为
(6)已知空气中SO2的最大允许排放浓度不得超过0.02 mg•L-1,可通过下列装置定量分析空气中SO2的含量。
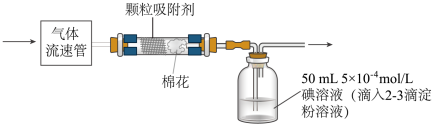
您最近半年使用:0次
名校
解题方法
4 . 将25.6g铜与一定量的浓硝酸反应,铜消耗完时,共产生 混合气体11.2L(标准状况),则整个反应过程中消耗
混合气体11.2L(标准状况),则整个反应过程中消耗 总的物质的量为
总的物质的量为
 混合气体11.2L(标准状况),则整个反应过程中消耗
混合气体11.2L(标准状况),则整个反应过程中消耗 总的物质的量为
总的物质的量为| A.1mol | B. | C.1.6mol | D.1.3mol |
您最近半年使用:0次
5 . 水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示。下列说法错误的是
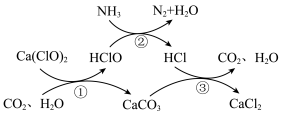
A.标准状况下, 所含的共用电子对数目为 所含的共用电子对数目为 |
B.标准状况下, 所含的原子总数为 所含的原子总数为 |
C.标准状况下, 气体溶于 气体溶于 水中形成的溶液浓度为 水中形成的溶液浓度为 |
D.反应②每生成 消耗 消耗 分子数目为 分子数目为 |
您最近半年使用:0次
解题方法
6 . 向 含
含 和
和 混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
 含
含 和
和 混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是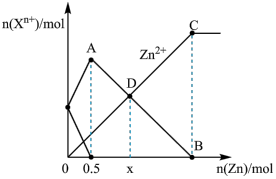
A.起始时, 溶液和 溶液和 溶液的物质的量浓度均为 溶液的物质的量浓度均为 |
B.D点的横坐标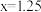 |
C.线段 表示溶液中 表示溶液中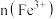 的变化趋势 的变化趋势 |
D.反应至 点时,溶液总质量增加 点时,溶液总质量增加 |
您最近半年使用:0次
名校
解题方法
7 . 正钒酸(H3VO4)溶于水,其氧化性大于氯气,酸性条件下与乙二酸(H2C2O4)发生离子反应: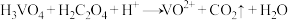 (未配平)。下列说法错误的是
(未配平)。下列说法错误的是
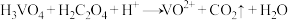 (未配平)。下列说法错误的是
(未配平)。下列说法错误的是A.该反应中,还原剂与氧化剂的物质的量之比为 |
B.每生成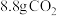 ,转移 ,转移 电子 电子 |
C.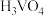 为强酸 为强酸 |
D.向正钒酸溶液中通入一定量的 ,溶液变浑浊 ,溶液变浑浊 |
您最近半年使用:0次
解题方法
8 . 在酸性条件下,黄铁矿 催化氧化反应的离子方程式为
催化氧化反应的离子方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
 催化氧化反应的离子方程式为
催化氧化反应的离子方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是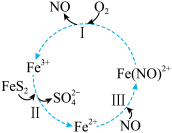
| A.黄铁矿催化氧化中NO作催化剂 |
B.反应Ⅰ的离子方程式为 |
| C.反应Ⅲ是非氧化还原反应 |
D.反应Ⅱ中若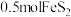 被还原,转移电子的物质的量为 被还原,转移电子的物质的量为 |
您最近半年使用:0次
名校
解题方法
9 . 二氧化硫是最常见、最简单、有刺激性的硫氧化物,大气主要污染物之一,火山爆发时会喷出该气体,在许多工业过程中也会产生二氧化硫。SO2在生活、生产中有重要用途,使用不当会造成环境污染。
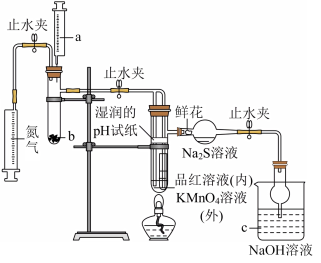
(1)某同学利用如图所示装置研究二氧化硫的性质。___________ ,加入药品前需要___________ 。
②实验开始前先通入一段时间N2,此操作的目的是___________ 。
③装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有___________ 性。
④装置c中的溶液___________ (填能或不能)用澄清石灰水替换,理由是___________ 。
(2)某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。___________ 。该空气中二氧化硫的体积分数为___________ 。
(1)某同学利用如图所示装置研究二氧化硫的性质。
②实验开始前先通入一段时间N2,此操作的目的是
③装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有
④装置c中的溶液
(2)某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。

您最近半年使用:0次
10 .  是一种高效多功能水处理剂,应用前景十分看好。一种制备
是一种高效多功能水处理剂,应用前景十分看好。一种制备 的方法可用化学方程式表示为:
的方法可用化学方程式表示为: ,对此反应下列说法中不正确的是
,对此反应下列说法中不正确的是
 是一种高效多功能水处理剂,应用前景十分看好。一种制备
是一种高效多功能水处理剂,应用前景十分看好。一种制备 的方法可用化学方程式表示为:
的方法可用化学方程式表示为: ,对此反应下列说法中不正确的是
,对此反应下列说法中不正确的是A. 既作氧化剂又作还原剂 既作氧化剂又作还原剂 |
B.2  发生反应时,反应中共有8 发生反应时,反应中共有8 电子转移 电子转移 |
C.每生成 氧气就有 氧气就有  被氧化 被氧化 |
D. 既是还原产物又是氧化产物 既是还原产物又是氧化产物 |
您最近半年使用:0次



