名校
1 . 以硅藻土为载体的五氧化二钒(V2O3)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O3既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
以下是一种废钒催化剂回收工艺路线:
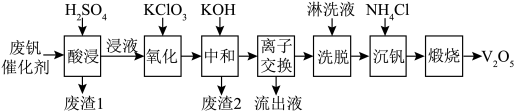
回答下列问题:
(1)“酸浸”时V2O5转化为 , 反应的离子方程式为
, 反应的离子方程式为___________ ,同时V2O4转化为 。“废渣1”的主要成分是
。“废渣1”的主要成分是______ 。
(2)“氧化”中使 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为______ 。
(3)“中和”后的溶液中,钒主要以 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
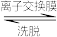
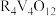 +
+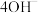 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈_____ 性(填“敢”或“碱”)。
(4)检验“流出液”中含量最多的阳离子,其实验操作称为___ 。
(5)“煅烧”中发生反应的化学方程式 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式_________ 。
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.20~2.90 | 2.8~3.32 | 22~28 | 60~65 | 1~2 | <1 |

回答下列问题:
(1)“酸浸”时V2O5转化为
 , 反应的离子方程式为
, 反应的离子方程式为 。“废渣1”的主要成分是
。“废渣1”的主要成分是(2)“氧化”中使
 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为(3)“中和”后的溶液中,钒主要以
 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
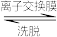
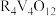 +
+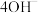 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈(4)检验“流出液”中含量最多的阳离子,其实验操作称为
(5)“煅烧”中发生反应的化学方程式
 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式
您最近半年使用:0次
名校
解题方法
2 . 实验室中利用固体 进行如图所示实验,下列说法错误的是
进行如图所示实验,下列说法错误的是
 进行如图所示实验,下列说法错误的是
进行如图所示实验,下列说法错误的是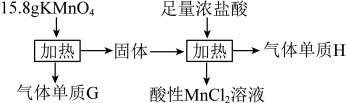
| A.气体G与气体H均为氧化产物 | B.实验中 既是氧化剂,又是还原剂 既是氧化剂,又是还原剂 |
| C.Mn元素至少参与了3个氧化还原反应 | D.G与H在标准状况下的总体积可能为5.6 L |
您最近半年使用:0次
解题方法
3 . CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0gCH4完全燃烧生成液体水放出444.8kJ热量。
CH4(g)+202(g)=CO2(g)+2H2O(1) ∆H=___________ kJ·mol-1。
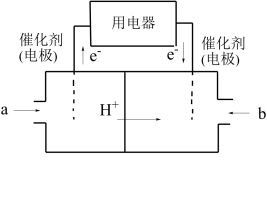
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为___________ ,通入b气体的电极反应式为___________ 。(质子交换膜只允许H'通过)___________ ℃左右。
②该反应催化剂的有效成分为CuAlO2,其用氧化物的形式表示为mCu2O·nAl2O3.m:n=___________ 。
(4)CH4还原法是处理NOx气体的一种方法。一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为___________ 。
(1)已知8.0gCH4完全燃烧生成液体水放出444.8kJ热量。
CH4(g)+202(g)=CO2(g)+2H2O(1) ∆H=
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为
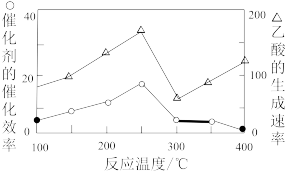
②该反应催化剂的有效成分为CuAlO2,其用氧化物的形式表示为mCu2O·nAl2O3.m:n=
(4)CH4还原法是处理NOx气体的一种方法。一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为
您最近半年使用:0次
解题方法
4 . 按要求,回答下列问题:
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是___________ 。
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:___________ 。
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是___________ 。
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
(5)某同学在探究漂白粉溶液性质时,在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈___________ 性,并具有___________ 性。
(6)实验室也可用 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: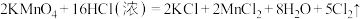 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为___________ 。
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
| A.食醋 | B.食盐 | C.烧碱 | D.纯碱 |
(6)实验室也可用
 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: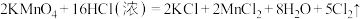 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
您最近半年使用:0次
解题方法
5 . 汽车剧烈碰撞时,安全气囊中发生反应 。有关该反应,下列叙述正确的是
。有关该反应,下列叙述正确的是
 。有关该反应,下列叙述正确的是
。有关该反应,下列叙述正确的是A.上述反应中 是还原剂 是还原剂 |
B.每生成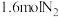 ,转移的电子为2mol ,转移的电子为2mol |
C. 中N的化合价为-3价 中N的化合价为-3价 |
| D.若被氧化的N原子的物质的量为3mol,则氧化产物比还原产物多1.4mol |
您最近半年使用:0次
解题方法
6 . 下列有关 说法正确的是
说法正确的是
 说法正确的是
说法正确的是A. 中阴阳离子的个数比为1:1 中阴阳离子的个数比为1:1 |
B. 体现强氧化性,可以用作呼吸面具的供氧剂 体现强氧化性,可以用作呼吸面具的供氧剂 |
C. 由钠在常温下与氧气反应得到 由钠在常温下与氧气反应得到 |
D. 与 与 反应,产生标准状况下 反应,产生标准状况下 ,转移 ,转移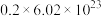 个电子 个电子 |
您最近半年使用:0次
解题方法
7 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备 和
和 的部分实验步骤如下:
的部分实验步骤如下: ”步骤中,为加快溶解速率,可采取的措施是
”步骤中,为加快溶解速率,可采取的措施是___________ 。(任写一种方法)。
(2)从“滤液 ”中提取
”中提取 的实验步骤依次为
的实验步骤依次为___________ 、过滤、冰水洗涤、低温干燥,其中冰水洗涤晶体的目的是___________ 。
(3)在“溶解 ”步骤中,发生反应的化学方程式为
”步骤中,发生反应的化学方程式为___________ 。
(4)为测定产品中 的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
 溶液至刚好完全反应,消耗
溶液至刚好完全反应,消耗 溶液25.00mL。
溶液25.00mL。
已知: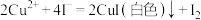 ,
, 。请依据实验数据计算样品中
。请依据实验数据计算样品中 的质量分数
的质量分数___________ (写出计算过程,结果保留2位小数)。
 和
和 的部分实验步骤如下:
的部分实验步骤如下: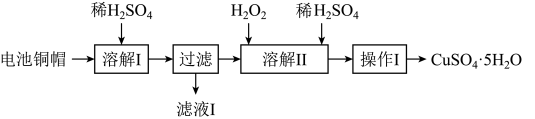
 ”步骤中,为加快溶解速率,可采取的措施是
”步骤中,为加快溶解速率,可采取的措施是(2)从“滤液
 ”中提取
”中提取 的实验步骤依次为
的实验步骤依次为(3)在“溶解
 ”步骤中,发生反应的化学方程式为
”步骤中,发生反应的化学方程式为(4)为测定产品中
 的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
 溶液至刚好完全反应,消耗
溶液至刚好完全反应,消耗 溶液25.00mL。
溶液25.00mL。已知:
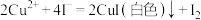 ,
, 。请依据实验数据计算样品中
。请依据实验数据计算样品中 的质量分数
的质量分数
您最近半年使用:0次
8 . 研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是
| A.正极反应式:Ag+Cl--e-=AgCl |
| B.每生成1mol Na2Mn5O10转移2 mol电子 |
| C.Na+不断向“水”电池的负极移动 |
| D.AgCl是还原产物 |
您最近半年使用:0次
9 . 根据金属钠与水(滴有酚酞)反应的现象,下列有关说法错误的是
| A.钠熔化成闪亮的小球,说明钠的熔点低且反应放热 |
| B.反应后溶液的颜色逐渐变红,说明反应生成了碱 |
| C.该反应中每1mol的Na得到1mol的电子 |
| D.当火灾现场存放有大量金属钠时不能用水来灭火 |
您最近半年使用:0次
10 . 在微生物作用下电解有机废水 含
含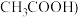 ,可获得清洁能源
,可获得清洁能源 ,其原理如图所示,下列有关说法不正确的是
,其原理如图所示,下列有关说法不正确的是
 含
含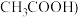 ,可获得清洁能源
,可获得清洁能源 ,其原理如图所示,下列有关说法不正确的是
,其原理如图所示,下列有关说法不正确的是
A.电极 极为负极 极为负极 |
B.与电源 极相连的惰性电极上发生的反应为: 极相连的惰性电极上发生的反应为: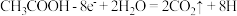  |
C.通电后,  通过质子交换膜向右移动。若导线中转移 通过质子交换膜向右移动。若导线中转移  电子,左侧溶液质量减轻 电子,左侧溶液质量减轻 |
D.通电后,若有   生成,则转移 生成,则转移  电子 电子 |
您最近半年使用:0次



