解题方法
1 . 食品包装中的铁系脱氧剂由还原铁粉、氯化钠和炭粉等组成,利用铁的吸氧腐蚀除去氧气,主要反应有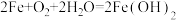 ,
,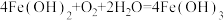 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:
(1)还原铁粉的物质的量是_______ mol。
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是_______ mol。
(3)在25 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理_______ mL包装盒中的空气。
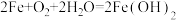 ,
,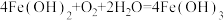 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:(1)还原铁粉的物质的量是
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是
(3)在25
 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
您最近一年使用:0次
名校
解题方法
2 . 铁盐与亚铁盐在工业生产和生活中具有重要应用。硫酸亚铁溶液可用于脱除烟气中的二氧化硫等有害气体。  溶液催化脱除烟气中 SO2的反应原理如图所示。下列说法正确的是
溶液催化脱除烟气中 SO2的反应原理如图所示。下列说法正确的是
 溶液催化脱除烟气中 SO2的反应原理如图所示。下列说法正确的是
溶液催化脱除烟气中 SO2的反应原理如图所示。下列说法正确的是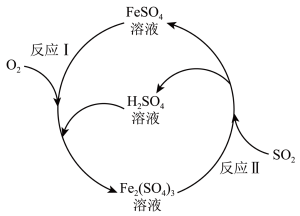
| A.“反应Ⅰ”中氧化剂和还原剂的物质的量之比为4∶1 |
B.“反应Ⅱ”的离子方程式为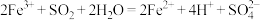 |
C.反应一段时间后,溶液中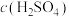 保持不变 保持不变 |
D.反应每脱除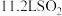 转移电子的物质的量为 转移电子的物质的量为 |
您最近一年使用:0次
2024-04-12更新
|
259次组卷
|
9卷引用:浙江省杭州市八县区2022-2023学年高一上学期期末检测化学试题
浙江省杭州市八县区2022-2023学年高一上学期期末检测化学试题浙江省杭州市临平区2022-2023学年高一上学期期末学业水平测试化学试题(已下线)【2023】【高一上】【杭七】【期末考】【高中化学】【廖汨平收集】13-2023新东方高二上期中考化学13河北师范大学附属中学2023-2024学年高一上学期12月月考化学试题河南省名校联盟2023-2024学年高一下学期3月月考化学试题河南省信阳高级中学2023-2024学年高一下学期3月月考化学试题云南省红河哈尼族彝族自治州蒙自市第一高级中学2023-2024学年高一下学期4月月考化学试题湖南省邵阳市第二中学2023-2024学年高一下学期第一次月考化学试题
3 . Na2FeO4是一种高效多功能水处理剂,具备强氧化性,自身被还原为Fe(OH)3,其制备方法为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。下列有关该反应的说法中不正确的是
| A.该反应中还原剂与氧化剂的物质的量之比为1:3 |
| B.Na2FeO4作为水处理剂,是因为其不仅具有杀菌的功能,还原产物还能吸附悬浮固体形成沉淀,从而使水净化 |
| C.氧化产物是Na2FeO4和O2 |
| D.当有3.9gNa2O2作氧化剂参与反应时,产生224mLO2(标准状况) |
您最近一年使用:0次
解题方法
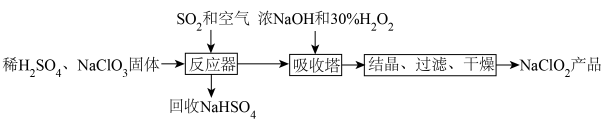
4 . ClO2是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成NaClO2晶体以便储运。亚氯酸钠(NaClO2)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成Cl-。亚氯酸钠晶体的一种生产工艺如图:
②H2O受热易分解。
(1)向“反应器”中鼓入空气的作用是______ 。
(2)“吸收塔”的作用是将产生的ClO2转化为NaClO2,在此过程中加入的H2O2的作用是_____ (填“氧化剂”或“还原剂”),当有1molH2O2参与该反应时,反应转移的电子数为______ 。
(3)“吸收塔”中需要控制温度不超过20℃,其原因是______ 。
(4)写出“反应器”步骤中生成ClO2的离子方程式______ 。
②H2O受热易分解。
(1)向“反应器”中鼓入空气的作用是
(2)“吸收塔”的作用是将产生的ClO2转化为NaClO2,在此过程中加入的H2O2的作用是
(3)“吸收塔”中需要控制温度不超过20℃,其原因是
(4)写出“反应器”步骤中生成ClO2的离子方程式
您最近一年使用:0次
解题方法
5 . 高铁酸钠是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理为:NaClO+Fe(NO3)3+NaOH→Na2FeO4↓+NaCl+NaNO3+H2O(未配平)。若反应消耗了150.00mL 1.00 mol/L NaClO溶液(不考虑其他物质与Fe3+反应),则产物中高铁酸钠理论产量(单位:g)为
| A.8.3 | B.33.2 | C.16.6 | D.24.9 |
您最近一年使用:0次
解题方法
6 . 实验室制Cl2的反应为4HCl(浓)十MnO2 MnCl2+C12↑+2H2O,下列说法错误的是
MnCl2+C12↑+2H2O,下列说法错误的是
 MnCl2+C12↑+2H2O,下列说法错误的是
MnCl2+C12↑+2H2O,下列说法错误的是| A.还原剂是HCl,氧化剂是MnO2 |
| B.每生成1.12LCl2,转移电子的物质的量为0.1 mol |
| C.每消耗8.7 gMnO2,被氧化的HCl的物质的量为0.2mol |
| D.生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质 |
您最近一年使用:0次
名校
解题方法
7 . 有一块铁的“氧化物”样品,用140mL5.0mol•L-1盐酸恰好将之完全溶解,所得溶液还能吸收0.56LCl2(标况下),恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为
| A.Fe4O5 | B.Fe3O4 | C.Fe5O7 | D.Fe2O3 |
您最近一年使用:0次
2024-02-14更新
|
54次组卷
|
3卷引用:浙江省绍兴市诸暨中学暨阳分校2023-2024学年高一上学期期中考试化学试题
8 . Ⅰ.无水 与
与 作用会生成
作用会生成 。现有
。现有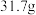 无水
无水 ,吸收
,吸收 后变成
后变成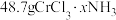 ,试回答下列问题:
,试回答下列问题:
(1) 中
中
______ 。
(2) 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到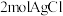 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为______ 。
Ⅱ.将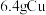 溶于
溶于 过量的硝酸溶液中,假设硝酸的还原产物只有
过量的硝酸溶液中,假设硝酸的还原产物只有 和
和 。反应结束后,将所得的溶液加水稀释至
。反应结束后,将所得的溶液加水稀释至 ,测得
,测得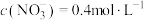 。(假设生成气体完全逸出)。请计算:
。(假设生成气体完全逸出)。请计算:
(3)稀释后溶液中 的物质的量浓度
的物质的量浓度______ 
(4)生成的气体中 物质的量
物质的量______  (用含有
(用含有 的表达式表示)
的表达式表示)
 与
与 作用会生成
作用会生成 。现有
。现有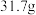 无水
无水 ,吸收
,吸收 后变成
后变成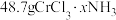 ,试回答下列问题:
,试回答下列问题:(1)
 中
中
(2)
 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到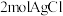 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为Ⅱ.将
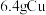 溶于
溶于 过量的硝酸溶液中,假设硝酸的还原产物只有
过量的硝酸溶液中,假设硝酸的还原产物只有 和
和 。反应结束后,将所得的溶液加水稀释至
。反应结束后,将所得的溶液加水稀释至 ,测得
,测得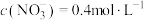 。(假设生成气体完全逸出)。请计算:
。(假设生成气体完全逸出)。请计算:(3)稀释后溶液中
 的物质的量浓度
的物质的量浓度
(4)生成的气体中
 物质的量
物质的量 (用含有
(用含有 的表达式表示)
的表达式表示)
您最近一年使用:0次
解题方法
9 . 下图是氯的“价类二维图”,请根据所学回答下列问题:

(1)已知A、H均为一元酸,写出A、H的化学式:___________ 、___________ 。
(2)写出B物质的一种用途:___________ 。
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:___________ 。
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的___________ 倍(已知两种消毒剂均被还原为 )。
)。

(1)已知A、H均为一元酸,写出A、H的化学式:
(2)写出B物质的一种用途:
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的
 )。
)。
您最近一年使用:0次
解题方法
10 . 在分析实验室常用 将溶液中的银离子(
将溶液中的银离子( )还原为银单质(Ag),而自身变为
)还原为银单质(Ag),而自身变为 ,则在该反应中氧化剂与还原剂的物质的量之比为
,则在该反应中氧化剂与还原剂的物质的量之比为
 将溶液中的银离子(
将溶液中的银离子( )还原为银单质(Ag),而自身变为
)还原为银单质(Ag),而自身变为 ,则在该反应中氧化剂与还原剂的物质的量之比为
,则在该反应中氧化剂与还原剂的物质的量之比为| A.1:1 | B.2:1 | C.3:1 | D.4:1 |
您最近一年使用:0次



