下图是氯的“价类二维图”,请根据所学回答下列问题:

(1)已知A、H均为一元酸,写出A、H的化学式:___________ 、___________ 。
(2)写出B物质的一种用途:___________ 。
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:___________ 。
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的___________ 倍(已知两种消毒剂均被还原为 )。
)。

(1)已知A、H均为一元酸,写出A、H的化学式:
(2)写出B物质的一种用途:
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的
 )。
)。
更新时间:2024-01-28 22:31:36
|
相似题推荐
【推荐1】某反应中反应物与生成物有:KMnO4、H2O2、H2SO4、O2、K2SO4、H2O和一种未知物质X。
(1)已知KMnO4在反应中得到电子,则该反应的还原剂是_______________ 。
(2)已知0.2mol KMnO4在反应中得到1mol电子生成X,则X的化学式为______________ 。
(3)根据上述反应可推知(在该条件下)__________ 。
a.氧化性:KMnO4>O2 b.氧化性: O2> KMnO4
c.还原性:H2O2>X d.还原性:X>H2O2
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:______

(1)已知KMnO4在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KMnO4在反应中得到1mol电子生成X,则X的化学式为
(3)根据上述反应可推知(在该条件下)
a.氧化性:KMnO4>O2 b.氧化性: O2> KMnO4
c.还原性:H2O2>X d.还原性:X>H2O2
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:

您最近一年使用:0次
【推荐2】I. 用电弧法合成碳纳米管,常伴有大量杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯, 其反应方程式为:
其反应方程式为:
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
(1)用双线桥法表示出该反应电子转移的方向和数目_____________ 。
(2)此反应的氧化产物和还原产物的物质的量之比为_______________ 。
(3)标准状况下,若产生6.72 LCO2气体,该反应中转移电子的物质的量为_________ 。
II.有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3组成一个氧化还原反应,请回答下列问题:
(1)将这6种物质分别填入下面对应的横线上,组成化学方程式并配平:
______ +_________ +_______ →________ I2+________ +_______ +____ H2O
(2)反应物中发生氧化反应的物质是______ (填化学式),被还原的元素是______ (填元素符号)。
 其反应方程式为:
其反应方程式为:2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
(1)用双线桥法表示出该反应电子转移的方向和数目
(2)此反应的氧化产物和还原产物的物质的量之比为
(3)标准状况下,若产生6.72 LCO2气体,该反应中转移电子的物质的量为
II.有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3组成一个氧化还原反应,请回答下列问题:
(1)将这6种物质分别填入下面对应的横线上,组成化学方程式并配平:
(2)反应物中发生氧化反应的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,保护水资源人人有责。
Ⅰ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是:在强碱性条件下,NaClO溶液和FeCl3溶液反应生成高铁酸钠和氯化钠。
(1)高铁酸钠中铁元素的化合价为_______ 。
(2)反应中高铁酸钠是_______ 产物(填“氧化”或“还原”)。
(3)写出制备高铁酸钠的离子方程式_______ 。
(4)使用氯气对自来水消毒时,氯气与水中的有机物反应生成对人体有害的物质,人们开始使用新的自来水消毒剂,如氯元素的某种氧化物,写出这种新消毒剂的名称_______ 。
Ⅱ.工业酸性废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O 转化为Cr3+。
转化为Cr3+。
(5)绿矾是结晶水合物,风化是指在室温和干燥的空气里,结晶水合物失去结晶水的现象,则风化属于_______ 变化(填“物理”或“化学”)。
(6)在溶液中Cr2O 存在反应:Cr2O
存在反应:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+,该反应
+2H+,该反应_______ 氧化还原反应(填“属于”或“不属于”)。
(7)写出处理工业酸性废水时发生反应的离子方程式_______ 。
Ⅰ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是:在强碱性条件下,NaClO溶液和FeCl3溶液反应生成高铁酸钠和氯化钠。
(1)高铁酸钠中铁元素的化合价为
(2)反应中高铁酸钠是
(3)写出制备高铁酸钠的离子方程式
(4)使用氯气对自来水消毒时,氯气与水中的有机物反应生成对人体有害的物质,人们开始使用新的自来水消毒剂,如氯元素的某种氧化物,写出这种新消毒剂的名称
Ⅱ.工业酸性废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O 转化为Cr3+。
转化为Cr3+。(5)绿矾是结晶水合物,风化是指在室温和干燥的空气里,结晶水合物失去结晶水的现象,则风化属于
(6)在溶液中Cr2O
 存在反应:Cr2O
存在反应:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+,该反应
+2H+,该反应(7)写出处理工业酸性废水时发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电石(主要成分为 )是重要的基本化工原料,主要用于生产乙炔。回答下列问题:
)是重要的基本化工原料,主要用于生产乙炔。回答下列问题:
(1)碳元素在元素周期表中的位置为_______ ; 的电子式为
的电子式为_______ 。
(2)①目前工业上合成电石主要采用氧热法。
已知: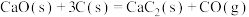
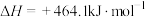 ;
;

 。
。
若不考虑热量耗散,物料转化率均为 ,最终炉中出来的气体只有
,最终炉中出来的气体只有 。则为了维持热平衡,每生产
。则为了维持热平衡,每生产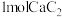 ,投料的量为
,投料的量为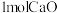 、
、_______ 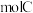 及
及_______ 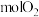 。
。
②制乙炔后的固体废渣主要成分为 ,可用于制取漂白粉,制取漂白粉的化学方程式为
,可用于制取漂白粉,制取漂白粉的化学方程式为_______ 。
(3)乙炔是二种重要的有机化工原料,乙炔在不同的反应条件下可以转化成下列化合物:
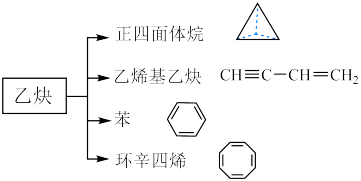
下列说法正确的是_______(填标号)。
(4)以乙炔为原料可制备维尼纶(PVAC),其合成路线如下:
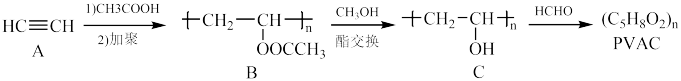
① 中官能团名称为
中官能团名称为_______ 。
② 经过两步反应,第二步为加聚反应,第一步反应类型为
经过两步反应,第二步为加聚反应,第一步反应类型为_______ 。
③ 的反应过程中另一种生成物的结构简式为
的反应过程中另一种生成物的结构简式为_______ 。
 )是重要的基本化工原料,主要用于生产乙炔。回答下列问题:
)是重要的基本化工原料,主要用于生产乙炔。回答下列问题:(1)碳元素在元素周期表中的位置为
 的电子式为
的电子式为(2)①目前工业上合成电石主要采用氧热法。
已知:
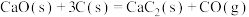
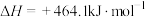 ;
;
 。
。若不考虑热量耗散,物料转化率均为
 ,最终炉中出来的气体只有
,最终炉中出来的气体只有 。则为了维持热平衡,每生产
。则为了维持热平衡,每生产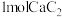 ,投料的量为
,投料的量为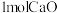 、
、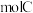 及
及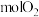 。
。②制乙炔后的固体废渣主要成分为
 ,可用于制取漂白粉,制取漂白粉的化学方程式为
,可用于制取漂白粉,制取漂白粉的化学方程式为(3)乙炔是二种重要的有机化工原料,乙炔在不同的反应条件下可以转化成下列化合物:

下列说法正确的是_______(填标号)。
| A.乙烯基乙炔分子中所有原子可以处于同一直线上 |
B.常温下, 苯中含碳碳双键数目约为 苯中含碳碳双键数目约为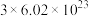 |
| C.环辛四烯与苯均能使酸性高锰酸钾溶液褪色 |
| D.正四面体烷与环辛四烯的一取代物均只有一种 |
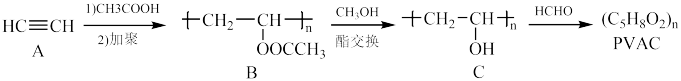
①
 中官能团名称为
中官能团名称为②
 经过两步反应,第二步为加聚反应,第一步反应类型为
经过两步反应,第二步为加聚反应,第一步反应类型为③
 的反应过程中另一种生成物的结构简式为
的反应过程中另一种生成物的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯是一种生产生活中常见的元素,下图是几种含氯产品。

(1)Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图装置进行尾气处理,用化学方程式表示该原理___________ 。气体应该由___________ (填a或b)管通入。若要吸收标准状况下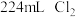 ,至少需要1mol/L的上述溶液
,至少需要1mol/L的上述溶液___________ mL。
(2)工业上制取漂白粉的化学方程式是___________ 。
(3)抗击新冠肺炎的战役中使用了大量的84消毒液。同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。将5mL市售84消毒液稀释100倍,测得稀释后溶液的 ,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
已知溶液中 、HClO和
、HClO和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
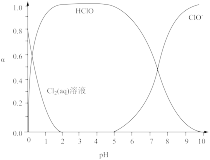
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色___________ (填“越快”或“越慢”)。
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是___________ 。

(1)Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图装置进行尾气处理,用化学方程式表示该原理
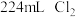 ,至少需要1mol/L的上述溶液
,至少需要1mol/L的上述溶液(2)工业上制取漂白粉的化学方程式是
(3)抗击新冠肺炎的战役中使用了大量的84消毒液。同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。将5mL市售84消毒液稀释100倍,测得稀释后溶液的
 ,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:| 烧杯 | 溶液pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色比b烧杯中10min后的浅;4h后红纸褪色 |
 、HClO和
、HClO和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】实验室用二氧化锰和浓盐酸反应制取氯气并探究其性质,实验装置如图所示
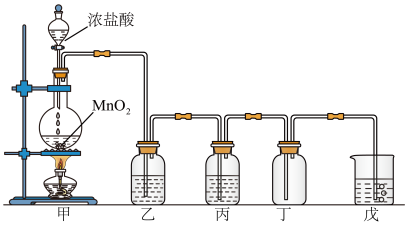
(1)装置甲中发生的离子方程式为_______ ;
(2)装置乙中盛放的试剂为_______ ;装置丙的作用为_______ ;
(3)将生成的气体通入紫色石蕊试液中,现象为_______ ;
(4)戊中反应化学方程式为_______ ;
(5)如果将甲中产生的气体和SO2一起通入品红溶液中反应的方程式为_______ ;当两气体同时按照物质的量比1:1通入时,品红溶液中的现象为_______ 。

(1)装置甲中发生的离子方程式为
(2)装置乙中盛放的试剂为
(3)将生成的气体通入紫色石蕊试液中,现象为
(4)戊中反应化学方程式为
(5)如果将甲中产生的气体和SO2一起通入品红溶液中反应的方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。实验室制取干燥
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为___________ 。

 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。实验室制取干燥
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】借助现代科技手段研究化学反应原理能加深对知识本质的理解。
(1)下图是电解质导电性测试实验装置, 的电离方程式为
的电离方程式为___________ ,接通电源后,灯泡不亮,本质原因是___________ ,要使灯泡发光,可采取的操作是___________ ;将少量 溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是___________ 。

(2)下图是一套验证气体性质的实验装置,回答下列问题:
①实验室可用二氧化锰与浓盐酸制备氯气,反应的离子方程式为___________ ,如图所示,在A处通入干燥的氯气。一段时间后,观察到C处红布条褪色,则B处的开关应该处于___________ (填“关闭”或“打开”)状态。
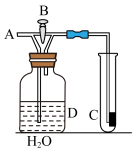
②实验后,利用数字传感器对D中的有色溶液进行光照实验分析,溶液光照实验前后比较,数目增加的离子有___________ (填化学式),对光照后溶液的叙述错误的是___________ (填标号)。
a.颜色变浅 b.漂白性增强 c.酸性增强 d.氧化性减弱
(1)下图是电解质导电性测试实验装置,
 的电离方程式为
的电离方程式为 溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
(2)下图是一套验证气体性质的实验装置,回答下列问题:
①实验室可用二氧化锰与浓盐酸制备氯气,反应的离子方程式为

②实验后,利用数字传感器对D中的有色溶液进行光照实验分析,溶液光照实验前后比较,数目增加的离子有
a.颜色变浅 b.漂白性增强 c.酸性增强 d.氧化性减弱
您最近一年使用:0次




