名校
解题方法
1 . 下列反应的离子方程式书写不正确的是
A.用 溶液检验 溶液检验 气体: 气体: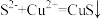 |
B.向亚硫酸溶液中加入双氧水: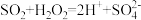 |
C. 溶于水: 溶于水: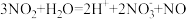 |
D. 溶液中加入 溶液中加入 溶液并微热: 溶液并微热: |
您最近半年使用:0次
解题方法
2 . 宏观辨识与微观探析是化学学科核心素养之一,下列方程式不能正确解释相应事实的是
A.SO2气体通入足量NaClO溶液中:SO2+H2O+3ClO-=Cl-+ +2HClO +2HClO |
B.亚硫酸氢钠水解方程式: +H2O +H2O H2SO3+OH- H2SO3+OH- |
C.向加碘食盐(含碘酸钾)中加入碘化钾溶液和稀硫酸: +5I-+6H+=3I2+3H2O +5I-+6H+=3I2+3H2O |
| D.常用稀H2SO4和Fe2+为原料处理废旧铅酸蓄电池中的PbO2:2Fe2++PbO2+4H+=2Fe3++Pb2++2H2O |
您最近半年使用:0次
解题方法
3 . 铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为_______ ,发生反应的离子方程式为_______ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是_______ 。
(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为_______ 。
(4)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:_______ 。
② 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为_______ 。
③滤液II中溶质的用途之一是_______ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为
(4)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:
②
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为③滤液II中溶质的用途之一是
您最近半年使用:0次
解题方法
4 . 现有下列10种物质:①液态HCl;② 固体;③NaCl溶液;④
固体;③NaCl溶液;④ ;⑤蔗糖溶液;⑥
;⑤蔗糖溶液;⑥ 粉末;⑦稀硫酸;⑧氨水;⑨
粉末;⑦稀硫酸;⑧氨水;⑨ ;⑩Zn。
;⑩Zn。
(1)物质中属于电解质的有_______ (填序号,下同),能导电的有_______ 。
(2)写出⑨与⑩在水溶液中反应的离子方程式:_______ 。
(3)写出过氧化钠与④反应的化学方程式并用双线桥表示其得失电子情况:_______ 。
(4)同温、同压下等质量的 和CO,它们所占的体积比为
和CO,它们所占的体积比为_______ 。
(5)将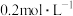 的
的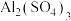 和
和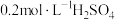 溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
_______  。
。
(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为____ 。
 固体;③NaCl溶液;④
固体;③NaCl溶液;④ ;⑤蔗糖溶液;⑥
;⑤蔗糖溶液;⑥ 粉末;⑦稀硫酸;⑧氨水;⑨
粉末;⑦稀硫酸;⑧氨水;⑨ ;⑩Zn。
;⑩Zn。(1)物质中属于电解质的有
(2)写出⑨与⑩在水溶液中反应的离子方程式:
(3)写出过氧化钠与④反应的化学方程式并用双线桥表示其得失电子情况:
(4)同温、同压下等质量的
 和CO,它们所占的体积比为
和CO,它们所占的体积比为(5)将
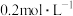 的
的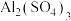 和
和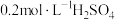 溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
 。
。(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为
您最近半年使用:0次
解题方法
5 . 写出下列反应的离子方程式:
(1)硫酸与Ba(OH)2溶液反应___________ 。
(2)碳酸钙与盐酸反应___________ 。
(1)硫酸与Ba(OH)2溶液反应
(2)碳酸钙与盐酸反应
您最近半年使用:0次
名校
解题方法
6 . 我国的青铜文化历史悠久。西汉时期的“湿法炼铜”工艺就是利用铁和硫酸铜溶液反应制取铜,有关反应的离子方程式为___________ 。
您最近半年使用:0次
解题方法
7 . 利用废旧镀锌铁皮制备Fe3O4胶体粒子的流程如下:
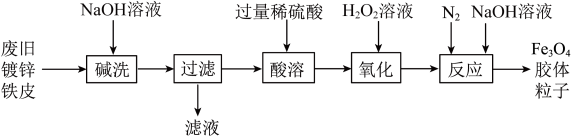
| A.Fe3O4俗称铁红 |
| B.“碱洗”的主要目的是除去镀锌铁皮表面的油污 |
| C.“酸溶”反应的离子方程式为Fe+2H+=Fe2++H2↑ |
D.“氧化”后溶液中所存在的离子为:H+、Fe3+、SO |
您最近半年使用:0次
解题方法
8 . 下列离子方程式正确的是
| A.向FeI2的溶液中通少量氯气: 2Fe2++2I- +2Cl2=2Fe3++I2+4Cl- |
B.NaHCO3溶液中加少量Ba(OH)2溶液: +Ba2++OH-=BaCO3↓+H2O +Ba2++OH-=BaCO3↓+H2O |
| C.氢氧化铝与盐酸反应:Al(OH)3+3H+= Al3++3H2O |
D.硫酸铜溶液与氢氧化钡溶液反应: +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
您最近半年使用:0次
解题方法
9 . 实验室模拟工业漂白液脱除废水中氨氮 的流程如下:
的流程如下:
粗盐水 精制盐水
精制盐水 Cl2
Cl2 漂白液
漂白液 NaCl
NaCl
下列分析正确的是
 的流程如下:
的流程如下:粗盐水
 精制盐水
精制盐水 Cl2
Cl2 漂白液
漂白液 NaCl
NaCl下列分析正确的是
A.漂白液的有效成分是 |
| B.①中蒸发浓缩粗盐水,不用加入其它试剂,即可得到纯氯化钠 |
C.③中制备漂白液的反应: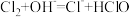 |
| D.②、③、④中均发生了氧化还原反应 |
您最近半年使用:0次
解题方法
10 . 某课外小组对金属钠进行研究。已知 、
、 都是单质,
都是单质, 的水溶液是一种常见的强酸。
的水溶液是一种常见的强酸。 在空气中放置足够长时间,最终的生成物是(写化学式):
在空气中放置足够长时间,最终的生成物是(写化学式):_______ ,写出 的用途
的用途_______ 。(答一种即可)
(2)若A是一种常见金属单质,向 溶液中逐滴加入F液至过量,所看到的实验现象是
溶液中逐滴加入F液至过量,所看到的实验现象是______ 。
(3)向集满 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。上述实验过程中发生的离子方程式有
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。上述实验过程中发生的离子方程式有_______ 、_______ 。
(4)某溶液,只可能含有 、
、 、
、 、
、 、
、 、
、 、
、 中的某些离子,当向该溶液中加入
中的某些离子,当向该溶液中加入 溶液时发现生成沉淀的物质的量随
溶液时发现生成沉淀的物质的量随 溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子
溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子_______ ,其对应的物质的量浓度之比为_______ 。
 、
、 都是单质,
都是单质, 的水溶液是一种常见的强酸。
的水溶液是一种常见的强酸。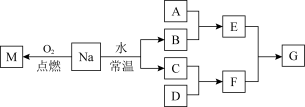
 在空气中放置足够长时间,最终的生成物是(写化学式):
在空气中放置足够长时间,最终的生成物是(写化学式): 的用途
的用途(2)若A是一种常见金属单质,向
 溶液中逐滴加入F液至过量,所看到的实验现象是
溶液中逐滴加入F液至过量,所看到的实验现象是(3)向集满
 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。上述实验过程中发生的离子方程式有
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。上述实验过程中发生的离子方程式有(4)某溶液,只可能含有
 、
、 、
、 、
、 、
、 、
、 、
、 中的某些离子,当向该溶液中加入
中的某些离子,当向该溶液中加入 溶液时发现生成沉淀的物质的量随
溶液时发现生成沉淀的物质的量随 溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子
溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子
您最近半年使用:0次



