解题方法
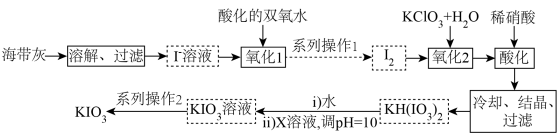
1 . 1833年,布森戈提出用富含碘的盐治疗甲肿,这是第一位提出向盐中添加碘防治甲肿的人。我国政府规定:碘盐添加KIO3。某厂生产碘酸钾(KIO3)的工艺流程如图所示。
(1) KIO3属于__________ (填“酸”“碱”“盐”或“氧化物”),其中I的化合价为__________ 价。
(2)“氧化1”中发生反应的离子方程式为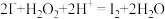 ,用单线桥法标出该反应中电子转移的方向和数目:
,用单线桥法标出该反应中电子转移的方向和数目:______________ ,该氧化过程中需要控制温度不宜过高,其原因是______________ 。系列操作2包括蒸发浓缩_______________ 过滤、乙醇洗涤、干燥等。
(3)X的化学式为______________ 。
(4)测定产品纯度:称取wg产品溶于蒸馏水,滴加适量稀硫酸,加入VmLcmol/LKI溶液恰好完全反应,发生反应: (未配平)。
(未配平)。
①根据上述数据,测得产品中碘元素质量分数为__________ (用含w、c、V的表达式表示)。
②如果将稀硫酸换成稀硝酸,则测得结果会__________ (填“偏高”“偏低”或“无影响”)。
(1) KIO3属于
(2)“氧化1”中发生反应的离子方程式为
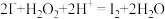 ,用单线桥法标出该反应中电子转移的方向和数目:
,用单线桥法标出该反应中电子转移的方向和数目:(3)X的化学式为
(4)测定产品纯度:称取wg产品溶于蒸馏水,滴加适量稀硫酸,加入VmLcmol/LKI溶液恰好完全反应,发生反应:
 (未配平)。
(未配平)。①根据上述数据,测得产品中碘元素质量分数为
②如果将稀硫酸换成稀硝酸,则测得结果会
您最近半年使用:0次
解题方法
2 . 现有下列10种物质:①液态HCl;② 固体;③NaCl溶液;④
固体;③NaCl溶液;④ ;⑤蔗糖溶液;⑥
;⑤蔗糖溶液;⑥ 粉末;⑦稀硫酸;⑧氨水;⑨
粉末;⑦稀硫酸;⑧氨水;⑨ ;⑩Zn。
;⑩Zn。
(1)物质中属于电解质的有_______ (填序号,下同),能导电的有_______ 。
(2)写出⑨与⑩在水溶液中反应的离子方程式:_______ 。
(3)写出过氧化钠与④反应的化学方程式并用双线桥表示其得失电子情况:_______ 。
(4)同温、同压下等质量的 和CO,它们所占的体积比为
和CO,它们所占的体积比为_______ 。
(5)将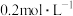 的
的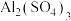 和
和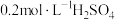 溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
_______  。
。
(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为____ 。
 固体;③NaCl溶液;④
固体;③NaCl溶液;④ ;⑤蔗糖溶液;⑥
;⑤蔗糖溶液;⑥ 粉末;⑦稀硫酸;⑧氨水;⑨
粉末;⑦稀硫酸;⑧氨水;⑨ ;⑩Zn。
;⑩Zn。(1)物质中属于电解质的有
(2)写出⑨与⑩在水溶液中反应的离子方程式:
(3)写出过氧化钠与④反应的化学方程式并用双线桥表示其得失电子情况:
(4)同温、同压下等质量的
 和CO,它们所占的体积比为
和CO,它们所占的体积比为(5)将
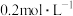 的
的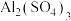 和
和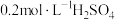 溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
 。
。(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为
您最近半年使用:0次
3 . 按要求回答问题:
(1)①铁红的化学式是___________ ;②氨气的电子式___________ 。
(2)NaHCO3在水中的电离方程式:___________ 。
(3)写出铁与水蒸气反应的化学方程式为并用单线桥法表示出该反应中电子转移的方向和数目___________ 。
(4)关于固体NaHSO4的组成和性质的表述正确的是:___________ (填写符合要求的序号)。
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电
(1)①铁红的化学式是
(2)NaHCO3在水中的电离方程式:
(3)写出铁与水蒸气反应的化学方程式为并用单线桥法表示出该反应中电子转移的方向和数目
(4)关于固体NaHSO4的组成和性质的表述正确的是:
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电
您最近半年使用:0次
名校
4 . 配平方程式并标出电子转移方向及数目___________ 。
___________ ___________
___________ ___________
___________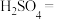 ___________
___________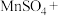 ___________
___________ ___________
___________ ___________
___________
___________
 ___________
___________ ___________
___________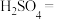 ___________
___________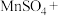 ___________
___________ ___________
___________ ___________
___________
您最近半年使用:0次
5 . 下列反应中电子转移的表示方法正确的是
A.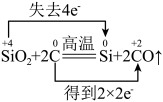 |
B.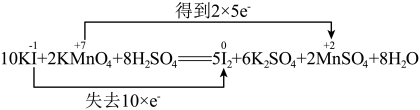 |
C. |
D.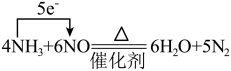 |
您最近半年使用:0次
解题方法
6 . 甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、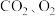 作用产生的,化学式为
作用产生的,化学式为 ,“铜绿”能跟酸反应生成铜盐、
,“铜绿”能跟酸反应生成铜盐、 和
和 。
。
(1) 属于
属于___________ (填“电解质”、“非电解质”)。
(2)从物质分类标准看,“铜绿”属于___________(填字母)。
(3)铜器表面有时会生成铜绿,这层铜绿可用化学方法除去。试写出用盐酸除去铜绿而不损伤器物的反应的离子方程式___________ 。
(4)古代人们高温灼烧孔雀石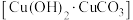 和木炭的混合物得到一种紫红色的金属铜,其化学反应式为
和木炭的混合物得到一种紫红色的金属铜,其化学反应式为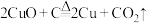 ,该反应属于___________(填序号)。
,该反应属于___________(填序号)。
(5)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应: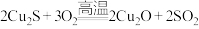 ;
; 。第一个反应中生成
。第一个反应中生成 时,转移的电子数是
时,转移的电子数是___________  ,第二个反应中氧化剂有
,第二个反应中氧化剂有___________ 。如把红色的 固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为:
固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为: 。请用双线桥表示该反应电子转移的方向和数目
。请用双线桥表示该反应电子转移的方向和数目___________ 。
(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为___________ 。
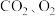 作用产生的,化学式为
作用产生的,化学式为 ,“铜绿”能跟酸反应生成铜盐、
,“铜绿”能跟酸反应生成铜盐、 和
和 。
。(1)
 属于
属于(2)从物质分类标准看,“铜绿”属于___________(填字母)。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(4)古代人们高温灼烧孔雀石
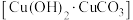 和木炭的混合物得到一种紫红色的金属铜,其化学反应式为
和木炭的混合物得到一种紫红色的金属铜,其化学反应式为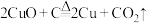 ,该反应属于___________(填序号)。
,该反应属于___________(填序号)。| A.化合反应 | B.置换反应 | C.氧化还原反应 | D.非氧化还原反应 |
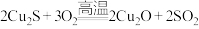 ;
; 。第一个反应中生成
。第一个反应中生成 时,转移的电子数是
时,转移的电子数是 ,第二个反应中氧化剂有
,第二个反应中氧化剂有 固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为:
固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为: 。请用双线桥表示该反应电子转移的方向和数目
。请用双线桥表示该反应电子转移的方向和数目(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为
您最近半年使用:0次
7 . 次磷酸 是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
(1)次磷酸中 的化合价为
的化合价为___________ ,画出 的原子结构示意图:
的原子结构示意图:___________ 。
(2)写出 与足量
与足量 溶液反应的化学方程式:
溶液反应的化学方程式:___________ 。
(3)工业上次磷酸 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: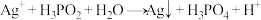 (方程式未配平)
(方程式未配平)
①该反应中___________ (填化学式)被还原。
②配平该反应方程式并标出电子转移的方向和数目:___________ 。
 。
。
③据该反应判断,还原性:___________ >___________ (填化学式)。
④若有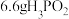 参加该反应,则反应中转移电子的物质的量为
参加该反应,则反应中转移电子的物质的量为___________  。
。
(4)若将氯气通入 溶液中,也发生
溶液中,也发生 的转化,写出该反应的化学方程式:
的转化,写出该反应的化学方程式:___________ 。
 是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:(1)次磷酸中
 的化合价为
的化合价为 的原子结构示意图:
的原子结构示意图:(2)写出
 与足量
与足量 溶液反应的化学方程式:
溶液反应的化学方程式:(3)工业上次磷酸
 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: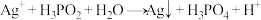 (方程式未配平)
(方程式未配平)①该反应中
②配平该反应方程式并标出电子转移的方向和数目:
 。
。③据该反应判断,还原性:
④若有
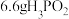 参加该反应,则反应中转移电子的物质的量为
参加该反应,则反应中转移电子的物质的量为 。
。(4)若将氯气通入
 溶液中,也发生
溶液中,也发生 的转化,写出该反应的化学方程式:
的转化,写出该反应的化学方程式:
您最近半年使用:0次
8 . 实验室用 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是___________ ,还原产物是___________ ;
(2)用单线桥标明电子转移的方向与数目___________ 。
(3)该反应中,氧化剂与还原剂的物质的量之比为___________ (前者比后者);盐酸在反应中表现出来的性质是___________ 。
(4)当生成标准状况下 时,转移的电子数目为
时,转移的电子数目为___________ ,被氧化的还原剂的物质的量为___________ 。
(5)也可以用 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:___________ 。
(6)举例说明氯气的氧化性比硫单质强,___________ 。
 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是
(2)用单线桥标明电子转移的方向与数目
(3)该反应中,氧化剂与还原剂的物质的量之比为
(4)当生成标准状况下
 时,转移的电子数目为
时,转移的电子数目为(5)也可以用
 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:(6)举例说明氯气的氧化性比硫单质强,
您最近半年使用:0次
解题方法
9 . 饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,有研究人员提出,在碱性条件下用铝粉将
的浓度,有研究人员提出,在碱性条件下用铝粉将 转化为无毒的
转化为无毒的 ,其化学方程式为
,其化学方程式为 。请回答下列问题:
。请回答下列问题:
(1)上述反应中,氧化剂是______ ;______ 发生氧化反应。
(2)用双线桥法表示出反应中电子转移的方向和数目_____ 。
(3)上述反应的离子方程式为______ 。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,有研究人员提出,在碱性条件下用铝粉将
的浓度,有研究人员提出,在碱性条件下用铝粉将 转化为无毒的
转化为无毒的 ,其化学方程式为
,其化学方程式为 。请回答下列问题:
。请回答下列问题:(1)上述反应中,氧化剂是
(2)用双线桥法表示出反应中电子转移的方向和数目
(3)上述反应的离子方程式为
您最近半年使用:0次
10 . 海洋是资源的宝库,以海水为原料可以制取粗盐、Br2、镁等多种物质。
I.粗盐中主要含NaCl,还含有少量泥沙、CaCl2、MgCl2和Na2SO4。
(1)将粗盐提纯的方法是:将粗盐溶于水,向里面依次加入稍过量的_______ (填字母),过滤,将滤液用盐酸酸化后,蒸发结晶。
A.Na2CO3 B.NaOH C.BaCl2
(2)实验中,判断所加BaCl2溶液已经过量的方法是_______ 。
II.浓缩海水中含有NaCl、NaBr等物质。从浓缩海水中提取溴的流程如下:_______ 。
(4)“吸收”时是用SO2水溶液吸收空气吹出的溴蒸汽。写出“吸收”时发生反应的化学方程式,并用双线桥标出电子转移的方向和数目:_______ 。
III.从海水中提取镁流程如下:
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(5)操作②是_______ 、过滤。
(6)工业上是将氢氧化镁转变为氯化镁,再电解氯化镁来制取镁单质,而不采用加热Mg(OH)2得到MgO,再电解熔融MgO的方法制取金属镁,其原因是_______ 。
I.粗盐中主要含NaCl,还含有少量泥沙、CaCl2、MgCl2和Na2SO4。
(1)将粗盐提纯的方法是:将粗盐溶于水,向里面依次加入稍过量的
A.Na2CO3 B.NaOH C.BaCl2
(2)实验中,判断所加BaCl2溶液已经过量的方法是
II.浓缩海水中含有NaCl、NaBr等物质。从浓缩海水中提取溴的流程如下:

(4)“吸收”时是用SO2水溶液吸收空气吹出的溴蒸汽。写出“吸收”时发生反应的化学方程式,并用双线桥标出电子转移的方向和数目:
III.从海水中提取镁流程如下:
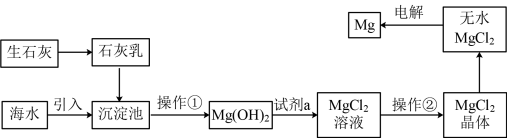
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(5)操作②是
(6)工业上是将氢氧化镁转变为氯化镁,再电解氯化镁来制取镁单质,而不采用加热Mg(OH)2得到MgO,再电解熔融MgO的方法制取金属镁,其原因是
您最近半年使用:0次



