1 . 现有中学化学常见的物质A、B、C、D、E、F、G、H,满足如下图所示转化关系。其中A、F为气体单质,A呈黄绿色,C为淡黄色固体化合物。 为生活中常见的液体化合物。回答下列问题:
为生活中常见的液体化合物。回答下列问题:
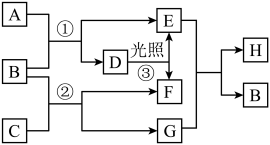
(1)写出下列物质的化学式:A___________ ,C___________ ,H___________ 。
(2)写出下列化学反应方程式:①___________ ,③___________ 。
(3)由于D易于发生③反应而不易于保存,故生产生活中往往用A与石灰乳反应生成易于保存运输的固体,其在潮湿空气中可以反应生成D,请写出这两个反应方程式:___________ ,___________ 。
(4)B可用于呼吸面具作氧气的来源,有关反应的化学方程式为___________ 。
(5)在实验室制取A物质的离子反应___________ 。
 为生活中常见的液体化合物。回答下列问题:
为生活中常见的液体化合物。回答下列问题:
(1)写出下列物质的化学式:A
(2)写出下列化学反应方程式:①
(3)由于D易于发生③反应而不易于保存,故生产生活中往往用A与石灰乳反应生成易于保存运输的固体,其在潮湿空气中可以反应生成D,请写出这两个反应方程式:
(4)B可用于呼吸面具作氧气的来源,有关反应的化学方程式为
(5)在实验室制取A物质的离子反应
您最近半年使用:0次
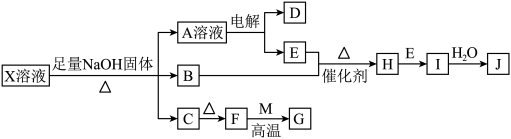
2 . 某些无机物的转化关系(部分反应物和生成物未列出)如图。已知常温常压下,M为有毒气体,D为密度最小的气体,单质E为无色气体,F可用作红色颜料,G是常见的金属单质,气体B能使湿润的红色石蕊试纸变蓝。___________ ;X溶液可以确定含有的阳离子为___________ (填离子符号)。
(2)检验NaOH中阳离子的方法为___________ 。
(3)写出B和E反应生成H的化学方程式:___________ 。
(4)B和H在一定条件下反应能生成一种单质,则该反应中氧化产物与还原产物的物质的量之比为___________ 。
(5)F→G在工业上的应用为___________ 。
(6)过量G和J的稀溶液反应的离子方程式为___________ ,该反应中J体现的性质为___________ 。
(2)检验NaOH中阳离子的方法为
(3)写出B和E反应生成H的化学方程式:
(4)B和H在一定条件下反应能生成一种单质,则该反应中氧化产物与还原产物的物质的量之比为
(5)F→G在工业上的应用为
(6)过量G和J的稀溶液反应的离子方程式为
您最近半年使用:0次
名校
3 . 非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题: ,另外
,另外 容积为无色气体。
容积为无色气体。
①A的电子式是___________ 。
②写出C→D的化学方程式:___________ 。
③D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式:___________ 。
(2)若A在常温下为非金属气态氢化物,且能使湿润的红色石蕊试纸变蓝,B遇到空气变成红棕色。
①A的电子式是___________ 。
②写出实验室制取A气体的化学方程式:___________ 。
③写出A→B的化学方程式:___________ 。
(3)若A为淡黄色晶体,D为二元强酸。
①将C气体通入 溶液产生的白色沉淀的化学方程式为
溶液产生的白色沉淀的化学方程式为___________
②将B通入 溶液不会产生沉淀。若在通入另一种气体X就会产生沉淀,如产生的沉淀与①产生的沉淀相同,则气体X可能是:
溶液不会产生沉淀。若在通入另一种气体X就会产生沉淀,如产生的沉淀与①产生的沉淀相同,则气体X可能是:___________ 。
A. B.
B. C.
C. D.
D. E.
E.

 ,另外
,另外 容积为无色气体。
容积为无色气体。①A的电子式是
②写出C→D的化学方程式:
③D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式:
(2)若A在常温下为非金属气态氢化物,且能使湿润的红色石蕊试纸变蓝,B遇到空气变成红棕色。
①A的电子式是
②写出实验室制取A气体的化学方程式:
③写出A→B的化学方程式:
(3)若A为淡黄色晶体,D为二元强酸。
①将C气体通入
 溶液产生的白色沉淀的化学方程式为
溶液产生的白色沉淀的化学方程式为②将B通入
 溶液不会产生沉淀。若在通入另一种气体X就会产生沉淀,如产生的沉淀与①产生的沉淀相同,则气体X可能是:
溶液不会产生沉淀。若在通入另一种气体X就会产生沉淀,如产生的沉淀与①产生的沉淀相同,则气体X可能是:A.
 B.
B. C.
C. D.
D. E.
E.
您最近半年使用:0次
4 . 部分含Mg或含Al物质的类别与化合价关系如图所示。下列推断不合理的是
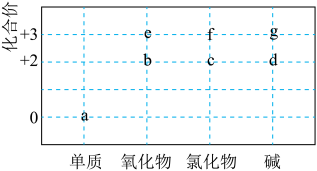

A.a不能与 反应生成d或g 反应生成d或g |
| B.b和e均可用于制造耐高温材料 |
| C.可存在a→f→g→e→a的循环转化关系 |
| D.直接加热蒸干c或f溶液无法得到无水氯化物 |
您最近半年使用:0次
名校
5 . 在如图所示的物质转化关系中,A是常见的气态氢化物,也是一种重要的化工产品、化工原料,B是能使带火星的木条复燃的无色、无味气体,E的相对分子质量比D的大17,合成A以及制取E的流程示意图如图所示,G是一种紫红色金属单质(反应条件和部分生成物未列出)。_______ 。
(2)反应A+B→C的化学方程式_______ 。
(3)反应E+G→C的离子反应方程式_______ 。
(4)D+F→E中氧化剂和还原剂的物质的量之比为_______ 。
(5)实验室保存E的浓溶液时用棕色试剂瓶,请用化学方程式解释原因__________ 。
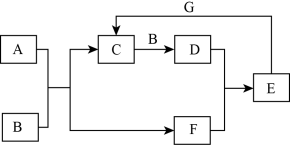
(6)有一瓶稀硫酸和稀硝酸的混合溶液,其中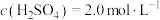 ,
,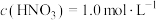 。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为_______ L。
(2)反应A+B→C的化学方程式
(3)反应E+G→C的离子反应方程式
(4)D+F→E中氧化剂和还原剂的物质的量之比为
(5)实验室保存E的浓溶液时用棕色试剂瓶,请用化学方程式解释原因
(6)有一瓶稀硫酸和稀硝酸的混合溶液,其中
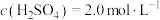 ,
,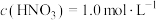 。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
您最近半年使用:0次
名校
解题方法
6 . 如图是无机物 在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体,
在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体, 都含有相同的元素。
都含有相同的元素。
(1)写出反应①的化学方程式:_______ 。
(2)在①②③④中属于氮的固定的是_______ (填序号)。
(3)下列说法正确的是_______(填字母)。
(4) 易溶于水。已知某温度压强下
易溶于水。已知某温度压强下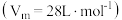 ,将体积为
,将体积为 的试管充满
的试管充满 后倒扣在水中。
后倒扣在水中。
①最终试管中所得 的物质的量浓度为(不考虑
的物质的量浓度为(不考虑 的扩散)
的扩散)_______  。
。
②若 按物质的量之比
按物质的量之比 被
被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是_______ 。为提高吸收速率与效率,最好选用_______ 装置(填字母)。 制取
制取 ,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗
,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗 的
的 制取
制取 ,在该过程中至少消耗的
,在该过程中至少消耗的 的物质的量为
的物质的量为_______  。
。
(6)实验室里检验 中阳离子的方法是
中阳离子的方法是_______ 。
 在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体,
在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体, 都含有相同的元素。
都含有相同的元素。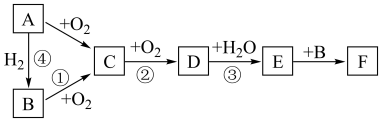
(1)写出反应①的化学方程式:
(2)在①②③④中属于氮的固定的是
(3)下列说法正确的是_______(填字母)。
A.通过水可以除去 中含有的少量D 中含有的少量D |
B.物质 均可以用向上排空气法收集 均可以用向上排空气法收集 |
C. 的浓溶液的存放方法是保存在无色细口玻璃瓶 的浓溶液的存放方法是保存在无色细口玻璃瓶 |
D.物质 中只含离子键 中只含离子键 |
(4)
 易溶于水。已知某温度压强下
易溶于水。已知某温度压强下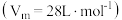 ,将体积为
,将体积为 的试管充满
的试管充满 后倒扣在水中。
后倒扣在水中。①最终试管中所得
 的物质的量浓度为(不考虑
的物质的量浓度为(不考虑 的扩散)
的扩散) 。
。②若
 按物质的量之比
按物质的量之比 被
被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是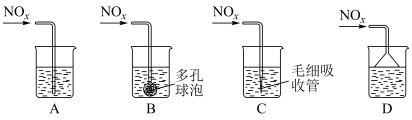
 制取
制取 ,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗
,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗 的
的 制取
制取 ,在该过程中至少消耗的
,在该过程中至少消耗的 的物质的量为
的物质的量为 。
。(6)实验室里检验
 中阳离子的方法是
中阳离子的方法是
您最近半年使用:0次
名校
7 . X、Y、Z、M、R、Q是短周期主族元素,部分信息如表所示:
(1)Z的单质与水反应的化学方程式为___________ 。
(2)Y与R相比,非金属性较强的是___________ (用元素符号表示),下列事实能证明这一结论的是___________ (填标号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:
c.最高价氧化物对应的水化物的酸性: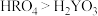
(3)根据表中数据推测Y的原子半径的范围:___________ 
___________  。
。
(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙 丙+水,则丙的化学式为
丙+水,则丙的化学式为___________ (写出一种即可)。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色试验呈黄色 |
(2)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:

c.最高价氧化物对应的水化物的酸性:
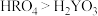
(3)根据表中数据推测Y的原子半径的范围:

 。
。(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙
 丙+水,则丙的化学式为
丙+水,则丙的化学式为
您最近半年使用:0次
解题方法
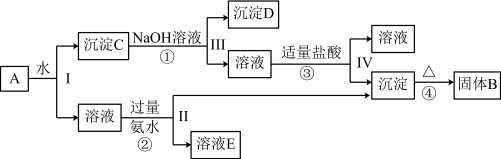
8 . 某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是___________ 。
(2)写出KAl(SO4)2在水中的电离方程式___________ 。
(3)已知H+ +[Al(OH)4]- = Al(OH)3↓+ H2O,根据上述框图反应关系,写出下列B、D、E所含物质的化学式:固体B___________ ;沉淀D___________ ;溶液E是K2SO4和___________ 。
(4)写出①②反应的离子方程式。
①___________ 。
②___________ 。
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
(2)写出KAl(SO4)2在水中的电离方程式
(3)已知H+ +[Al(OH)4]- = Al(OH)3↓+ H2O,根据上述框图反应关系,写出下列B、D、E所含物质的化学式:固体B
(4)写出①②反应的离子方程式。
①
②
您最近半年使用:0次
名校
9 . 已知X、Y和Z为中学化学中的常见元素﹐根据如图所示转化关系(反应条件及部分产物已略去)。回答下列问题:

(1)若A、B、C、D均为含X的化合物。A常用作制冷剂,D是一种强酸,则
①反应I的化学方程式为___________ 。
②常温下,C的颜色为___________ 色。
③足量的铜与一定量的D的浓溶液充分反应,向所得溶液中加入100mL 4 NaOH溶液,
NaOH溶液, 恰好沉淀完全。则消耗铜的质量为
恰好沉淀完全。则消耗铜的质量为___________ g。
(2)若A、B、C、D均为含Y的化合物。A是一元强碱且焰色为黄色,E是“碳中和”的主角,则B的化学式为___________ ;C的用途有___________ (任写一种);E的空间结构为___________ 。
(3)若A、B、C、D均为含Z的化合物。A为黄铁矿的主要成分,D为强酸,则
①A在空气中煅烧生成氧化铁的化学方程式为___________ 。
②C→D的过程中选择用98.3%的浓硫酸吸收而不用 吸收的原因是
吸收的原因是___________ 。

(1)若A、B、C、D均为含X的化合物。A常用作制冷剂,D是一种强酸,则
①反应I的化学方程式为
②常温下,C的颜色为
③足量的铜与一定量的D的浓溶液充分反应,向所得溶液中加入100mL 4
 NaOH溶液,
NaOH溶液, 恰好沉淀完全。则消耗铜的质量为
恰好沉淀完全。则消耗铜的质量为(2)若A、B、C、D均为含Y的化合物。A是一元强碱且焰色为黄色,E是“碳中和”的主角,则B的化学式为
(3)若A、B、C、D均为含Z的化合物。A为黄铁矿的主要成分,D为强酸,则
①A在空气中煅烧生成氧化铁的化学方程式为
②C→D的过程中选择用98.3%的浓硫酸吸收而不用
 吸收的原因是
吸收的原因是
您最近半年使用:0次
解题方法
10 . 现有金属单质A、B、C 和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
(1)写出下列物质的化学式:C___________ ,丙___________ ;
(2)写出实验室制备黄绿色气体乙的化学方程式:___________ ,过程⑦可能观察到的实验现象是:___________ ;
(3)写出过程⑦涉及的化学方程式___________ ,___________ ;
(4)反应⑦中如果可以长时间看到白色沉淀,可采取哪些方法:___________

(1)写出下列物质的化学式:C
(2)写出实验室制备黄绿色气体乙的化学方程式:
(3)写出过程⑦涉及的化学方程式
(4)反应⑦中如果可以长时间看到白色沉淀,可采取哪些方法:
您最近半年使用:0次



