1 . 某Q溶液中含有如表所示离子中的某5种且浓度均为0.5 (不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
(不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
已知:S2O + 2H+ = S + SO2 + H2O
+ 2H+ = S + SO2 + H2O
请回答下列问题:
(1)写出一种检验气体R的方法:______ 。写出产生气体R的离子方程式:______ 。
(2)由“向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变”可推知:Q溶液中一定不含表格中可能含有的8中阴离子中的___________ (填1-7数字)种阴离子。
(3)综合排断,Q溶液中一定含有的5种离子(浓度均为0.5 )分别为 :
)分别为 :______ (填离子符号,阳离子在前,阴离子在后)。
(4)取100ml的Q溶液与氯气充分反应,实验过程和结果如下:______ 。
②V的范围为:______ 。(格式写为m<V<n的形式)
 (不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
(不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。| 阳离子 | 阴离子 |
 、 、 、 、 、 、 、 、 、 、 、 、 、 、 |  、 、 、 、 、 、 、 、 、 、 , , 、 、 |
 + 2H+ = S + SO2 + H2O
+ 2H+ = S + SO2 + H2O请回答下列问题:
(1)写出一种检验气体R的方法:
(2)由“向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变”可推知:Q溶液中一定不含表格中可能含有的8中阴离子中的
(3)综合排断,Q溶液中一定含有的5种离子(浓度均为0.5
 )分别为 :
)分别为 :(4)取100ml的Q溶液与氯气充分反应,实验过程和结果如下:

②V的范围为:
您最近半年使用:0次
2 . 某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、Fe、FeO、Fe2O3中的若干种。某同学为确定该固体粉末的成分,取甲进行连续实验。实验过程及现象如下:
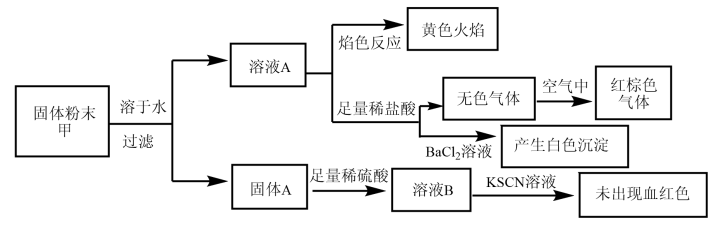
| A.固体粉末中含有钠元素,但不含钾元素 |
| B.固体粉末中无法确定是否含有K2SO3 |
| C.固体粉末中至少含有KNO3、NaNO2中的一种 |
| D.固体粉末中可能含有K2CO3、不含Fe2O3 |
您最近半年使用:0次
名校
解题方法
3 . 如图是无机物A~F在一定条件下的转化关系(部分产物及反应条件未标出)。已知:A为气体,A~F都含有相同的元素。
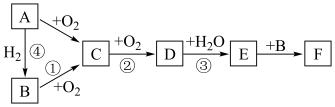
试回答下列问题。
(1)写出反应①的化学方程式:___________ 。
(2)在①②③④中属于氮的固定的是___________ (填序号)。
(3)下列说法正确的是___________。
(4)D易溶于水。常温常压下(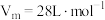 ),将体积为VmL的试管充满D后倒扣在水中。
),将体积为VmL的试管充满D后倒扣在水中。
①最终试管中所得E的物质的量浓度为(不考虑E的扩散)___________  。
。
②若C、D按物质的量之比1:1被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是___________ 。为提高吸收速率与效率,最好选用___________ 装置(填序号)。
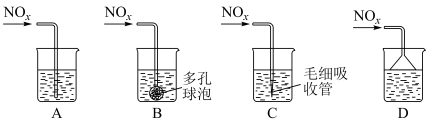
(5)工业上可用①②③由B制取E,为了提高原料的利用率并尽量减轻对环境的污染,C必须循环使用。若消耗1mol的B制取E,在该过程中至少消耗的 的物质的量为
的物质的量为___________ 。
(6)C气体与ag O2混合后通入水中,恰好被水完全吸收生成稀硝酸。若用该稀硝酸去溶解铜,假设该溶解过程只产生C气体,理论上能消耗铜的质量为___________ g。

试回答下列问题。
(1)写出反应①的化学方程式:
(2)在①②③④中属于氮的固定的是
(3)下列说法正确的是___________。
| A.通过水可以除去C中含有的少量D |
| B.物质C、D均可以用向上排空气法收集 |
| C.E的浓溶液的存放方法是保存在无色细口玻璃瓶 |
| D.物质 F 中含离子键 |
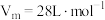 ),将体积为VmL的试管充满D后倒扣在水中。
),将体积为VmL的试管充满D后倒扣在水中。①最终试管中所得E的物质的量浓度为(不考虑E的扩散)
 。
。②若C、D按物质的量之比1:1被
 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是
(5)工业上可用①②③由B制取E,为了提高原料的利用率并尽量减轻对环境的污染,C必须循环使用。若消耗1mol的B制取E,在该过程中至少消耗的
 的物质的量为
的物质的量为(6)C气体与ag O2混合后通入水中,恰好被水完全吸收生成稀硝酸。若用该稀硝酸去溶解铜,假设该溶解过程只产生C气体,理论上能消耗铜的质量为
您最近半年使用:0次
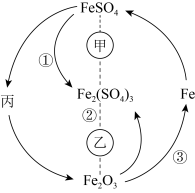
4 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题: 表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
(1)根据分析可知丙为______ (填化学式);甲可能是______ (填标号,下同),乙可能是______ 。
A.稀硝酸 B. 溶液
溶液
C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量______ (填药品名称);可以用______ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为______ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是______ (填化学方程式)。
(4)绿矾 常用于制备铁触媒催化剂。隔绝空气条件下,
常用于制备铁触媒催化剂。隔绝空气条件下, 绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至
绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至 时,绿矾发生反应的化学方程式为
时,绿矾发生反应的化学方程式为______ ;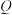 点对应的固体是一种金属氧化物,该物质的化学式为
点对应的固体是一种金属氧化物,该物质的化学式为______ 。
 表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。(1)根据分析可知丙为
A.稀硝酸 B.
 溶液
溶液C.
 D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
(4)绿矾
 常用于制备铁触媒催化剂。隔绝空气条件下,
常用于制备铁触媒催化剂。隔绝空气条件下, 绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至
绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至 时,绿矾发生反应的化学方程式为
时,绿矾发生反应的化学方程式为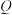 点对应的固体是一种金属氧化物,该物质的化学式为
点对应的固体是一种金属氧化物,该物质的化学式为
您最近半年使用:0次
2024-03-27更新
|
107次组卷
|
4卷引用:江西省部分地区2023-2024学年高一下学期3月月考化学试题
5 . 如图为某些中学常见物质的转化关系(部分反应条件或生成物略去)。其中A、B、C为常见单质,其余物质为化合物,C为黑色固体,气体D溶于水所得溶液显碱性,E为常用调味剂且焰色试验为黄色火焰,J为细小的白色晶体,常用作食物膨松剂,F常温下为无色无味液体。回答下列问题:
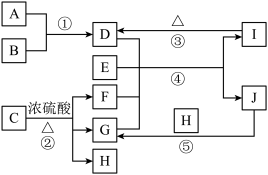
(1)H中含有的化学键为_______ (填“离子键”“共价键”或“离子键和共价键”)。
(2)实验室检验I中所含阳离子的方法为_________ 。
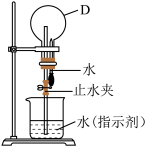
(3)反应①的化学方程式为________ ,以气体D与蒸馏水利用如图装置进行喷泉实验,引发喷泉的操作为________ 。
(4)反应②的化学方程式为________ ,其中氧化产物和还原产物的物质的量之比为________ 。
(5)反应④的化学方程式为_______ ,该反应可以发生的原因为________ 。
(6)向J的溶液中通入过量H时发生反应的离子方程式为________ 。

(1)H中含有的化学键为
(2)实验室检验I中所含阳离子的方法为
(3)反应①的化学方程式为

(4)反应②的化学方程式为
(5)反应④的化学方程式为
(6)向J的溶液中通入过量H时发生反应的离子方程式为
您最近半年使用:0次
6 . 在稀硫酸、二氧化碳、铜片、食盐、石灰水、一氧化碳、纯碱、铁片和木炭粉9种物质间存在图示关系,选择其中适当的物质,使有连线的两种物质发生反应。

请推断它们的化学式:①___________ ;②___________ ;③___________ ;④___________ ;⑤ 。
。

请推断它们的化学式:①
 。
。
您最近半年使用:0次
名校
解题方法
7 . 无机物A~B均为短周期元素组成的物质,且均含有同种元素,其中A是最简单氢化物、B是单质;上述物质在一定条件下可以发生如下转化。
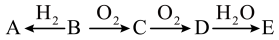
(1)若E为强碱,则A的电子式为____________________ 。
(2)若E为二元弱酸,则D的结构式为________________ 。
(3)若E为强酸,D在标准状况下是白色固体,则:
①E的浓溶液与炭反应的化学方程式________________ 。
②实验室检验E的酸根离子的方法是________________ 。
(4)若E为强酸,且A和E可以发生反应生成一种盐F,则:
①工业上制备C的化学方程式________________ 。
②实验室检验F中阳离子的离子方程式为________________ 。
③F固体可受热分解生成B、E和H2O,写出该反应化学方程式________________ 。
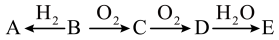
(1)若E为强碱,则A的电子式为
(2)若E为二元弱酸,则D的结构式为
(3)若E为强酸,D在标准状况下是白色固体,则:
①E的浓溶液与炭反应的化学方程式
②实验室检验E的酸根离子的方法是
(4)若E为强酸,且A和E可以发生反应生成一种盐F,则:
①工业上制备C的化学方程式
②实验室检验F中阳离子的离子方程式为
③F固体可受热分解生成B、E和H2O,写出该反应化学方程式
您最近半年使用:0次
解题方法
8 . 固体X由四种元素组成,可用来治疗胃酸过多,其成分属于硅酸形成的复盐;为探究M的具体组成,设计下列实验流程。
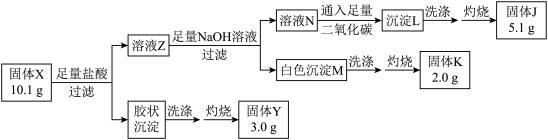
已知:K常用作高温耐火材料。
下列说法正确的是

已知:K常用作高温耐火材料。
下列说法正确的是
A.生成L的离子方程式为 |
| B.固体J和K都能溶于强酸和强碱 |
| C.洗涤和灼烧过程中都要用到玻璃棒和烧杯 |
D.固体X的化学式为 |
您最近半年使用:0次
9 . 现有中学化学常见的金属单质A、B、C和气体甲、乙、丙、丁以及物质D、E、F、G、H、X,其中气体乙为黄绿色气体,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
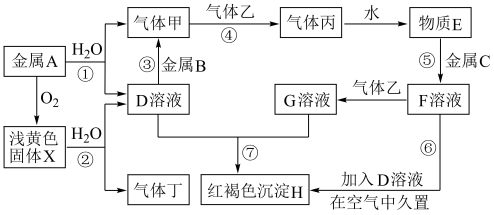
请根据以上信息完成下列各题:
(1)写出反应①的离子方程式:___________ 。
(2)写出反应②的化学方程式:___________ ,该反应的氧化剂是_____ 。
(3)写出反应③的化学方程式:___________ 。
(4)写出反应⑥的化学方程式:___________ 。

请根据以上信息完成下列各题:
(1)写出反应①的离子方程式:
(2)写出反应②的化学方程式:
(3)写出反应③的化学方程式:
(4)写出反应⑥的化学方程式:
您最近半年使用:0次
10 . 已知甲、乙为单质,丙为化合物,能实现下述转化关系:
甲+乙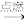 丙
丙 溶液
溶液 甲
甲
下列说法错误的是
甲+乙
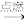 丙
丙 溶液
溶液 甲
甲下列说法错误的是
A.若丙溶于水得到蓝绿色溶液,则甲可能为 |
B.若“溶液”遇 放出 放出 气体,则甲可能是 气体,则甲可能是 |
C.若丙溶于水后得到强碱溶液,则甲可能是 |
| D.若“溶液”滴加NaOH溶液产生白色沉淀,则甲可能是Mg |
您最近半年使用:0次



