1 . 某Q溶液中含有如表所示离子中的某5种且浓度均为0.5 (不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
(不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
已知:S2O + 2H+ = S + SO2 + H2O
+ 2H+ = S + SO2 + H2O
请回答下列问题:
(1)写出一种检验气体R的方法:______ 。写出产生气体R的离子方程式:______ 。
(2)由“向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变”可推知:Q溶液中一定不含表格中可能含有的8中阴离子中的___________ (填1-7数字)种阴离子。
(3)综合排断,Q溶液中一定含有的5种离子(浓度均为0.5 )分别为 :
)分别为 :______ (填离子符号,阳离子在前,阴离子在后)。
(4)取100ml的Q溶液与氯气充分反应,实验过程和结果如下:______ 。
②V的范围为:______ 。(格式写为m<V<n的形式)
 (不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
(不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。| 阳离子 | 阴离子 |
 、 、 、 、 、 、 、 、 、 、 、 、 、 、 |  、 、 、 、 、 、 、 、 、 、 , , 、 、 |
 + 2H+ = S + SO2 + H2O
+ 2H+ = S + SO2 + H2O请回答下列问题:
(1)写出一种检验气体R的方法:
(2)由“向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变”可推知:Q溶液中一定不含表格中可能含有的8中阴离子中的
(3)综合排断,Q溶液中一定含有的5种离子(浓度均为0.5
 )分别为 :
)分别为 :(4)取100ml的Q溶液与氯气充分反应,实验过程和结果如下:

②V的范围为:
您最近一年使用:0次
2 . 某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、Fe、FeO、Fe2O3中的若干种。某同学为确定该固体粉末的成分,取甲进行连续实验。实验过程及现象如下:
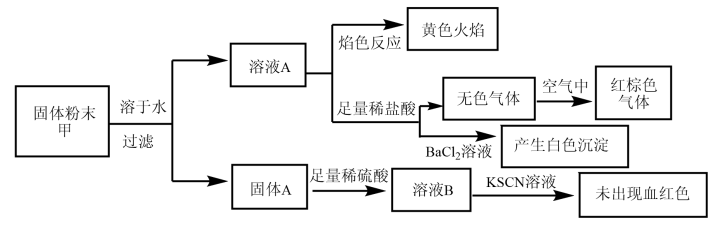
| A.固体粉末中含有钠元素,但不含钾元素 |
| B.固体粉末中无法确定是否含有K2SO3 |
| C.固体粉末中至少含有KNO3、NaNO2中的一种 |
| D.固体粉末中可能含有K2CO3、不含Fe2O3 |
您最近一年使用:0次
名校
解题方法
3 . 如图是无机物A~F在一定条件下的转化关系(部分产物及反应条件未标出)。已知:A为气体,A~F都含有相同的元素。
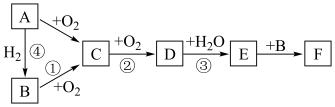
试回答下列问题。
(1)写出反应①的化学方程式:___________ 。
(2)在①②③④中属于氮的固定的是___________ (填序号)。
(3)下列说法正确的是___________。
(4)D易溶于水。常温常压下(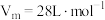 ),将体积为VmL的试管充满D后倒扣在水中。
),将体积为VmL的试管充满D后倒扣在水中。
①最终试管中所得E的物质的量浓度为(不考虑E的扩散)___________  。
。
②若C、D按物质的量之比1:1被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是___________ 。为提高吸收速率与效率,最好选用___________ 装置(填序号)。
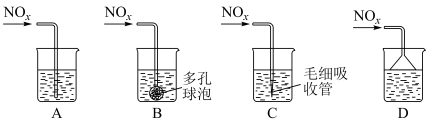
(5)工业上可用①②③由B制取E,为了提高原料的利用率并尽量减轻对环境的污染,C必须循环使用。若消耗1mol的B制取E,在该过程中至少消耗的 的物质的量为
的物质的量为___________ 。
(6)C气体与ag O2混合后通入水中,恰好被水完全吸收生成稀硝酸。若用该稀硝酸去溶解铜,假设该溶解过程只产生C气体,理论上能消耗铜的质量为___________ g。

试回答下列问题。
(1)写出反应①的化学方程式:
(2)在①②③④中属于氮的固定的是
(3)下列说法正确的是___________。
| A.通过水可以除去C中含有的少量D |
| B.物质C、D均可以用向上排空气法收集 |
| C.E的浓溶液的存放方法是保存在无色细口玻璃瓶 |
| D.物质 F 中含离子键 |
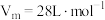 ),将体积为VmL的试管充满D后倒扣在水中。
),将体积为VmL的试管充满D后倒扣在水中。①最终试管中所得E的物质的量浓度为(不考虑E的扩散)
 。
。②若C、D按物质的量之比1:1被
 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是
(5)工业上可用①②③由B制取E,为了提高原料的利用率并尽量减轻对环境的污染,C必须循环使用。若消耗1mol的B制取E,在该过程中至少消耗的
 的物质的量为
的物质的量为(6)C气体与ag O2混合后通入水中,恰好被水完全吸收生成稀硝酸。若用该稀硝酸去溶解铜,假设该溶解过程只产生C气体,理论上能消耗铜的质量为
您最近一年使用:0次
名校
解题方法
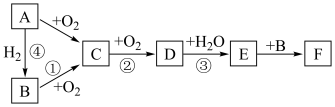
4 . 如图是无机物A~F在一定条件下的转化关系(部分产物及反应条件未标出)。
已知:A为气体,A~F都含有相同的元素。
(1)写出下列物质的化学式:C___________ 、F___________
(2)在①②③④中属于氮的固定的是___________ (填序号)
(3)D易溶于水。常温常压下(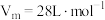 ),将体积为VmL的试管充满D后倒扣在水中。
),将体积为VmL的试管充满D后倒扣在水中。
①最终试管中所得E的物质的量浓度为(不考虑E的扩散)___________  。
。
②为了消除D的污染,可将它与B在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是___________ 。
③若C、D按物质的量之比1:1被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是___________ 。为提高吸收速率与效率,最好选用___________ 装置(填序号)。 的物质的量为
的物质的量为___________ 。
已知:A为气体,A~F都含有相同的元素。
(1)写出下列物质的化学式:C
(2)在①②③④中属于氮的固定的是
(3)D易溶于水。常温常压下(
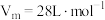 ),将体积为VmL的试管充满D后倒扣在水中。
),将体积为VmL的试管充满D后倒扣在水中。①最终试管中所得E的物质的量浓度为(不考虑E的扩散)
 。
。②为了消除D的污染,可将它与B在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是
③若C、D按物质的量之比1:1被
 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是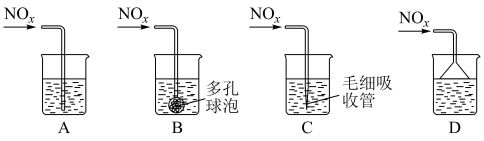
 的物质的量为
的物质的量为
您最近一年使用:0次
2024-01-28更新
|
277次组卷
|
3卷引用:江西省南昌市第十九中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
5 . A、B、C、D、E、F六种物质的焰色试验均为黄色。A、B、C、D与盐酸反应均生成E,此外B与盐酸反应还生成一种可燃性气体;C、D与酸反应还生成一种无色无味的气体H,该气体能使澄清的石灰水变浑浊。D与A可反应生成C,F与H也可反应生成C和另一种无色无味气体。回答下列问题:
(1)写出E的化学式:_______ 。
(2)写出F与H反应的化学方程式:_______ 。
(3)写出下列反应的离子方程式:
①C中滴少量盐酸:_______ 。
②D与A反应:_______ 。
(1)写出E的化学式:
(2)写出F与H反应的化学方程式:
(3)写出下列反应的离子方程式:
①C中滴少量盐酸:
②D与A反应:
您最近一年使用:0次
解题方法
6 . I.完成下列问题:
(1)实验室若金属钠等活泼金属着火时,应该用_________ 来灭火,金属钠应保存在_______ 中。
(2)金属钠在空气中燃烧生成Na2O2,Na2O2与CO2反应的化学方程式:___________ ,每消耗2mol Na2O2,转移的电子为___________  。
。
(3) Na2CO3固体中混有少量NaHCO3固体,除杂方法是___________ ,化学方程式是___________ 。
Ⅱ.下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色试验均为黄色。
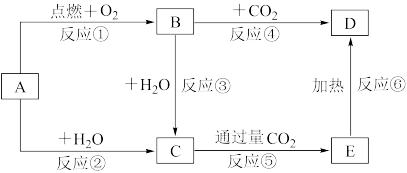
请填写下列空白:
(4)以上反应中,属于氧化还原反应的有___________ (填写编号)。
(5)写出B→C反应的化学方程式:_________ ,C→E的离子方程式:________ 。
(1)实验室若金属钠等活泼金属着火时,应该用
(2)金属钠在空气中燃烧生成Na2O2,Na2O2与CO2反应的化学方程式:
 。
。(3) Na2CO3固体中混有少量NaHCO3固体,除杂方法是
Ⅱ.下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色试验均为黄色。

请填写下列空白:
(4)以上反应中,属于氧化还原反应的有
(5)写出B→C反应的化学方程式:
您最近一年使用:0次
名校
解题方法
7 . 有一包固体,可能含有镁粉、炭粉、氧化铜、氢氧化钠、氯化钾中的一种或几种。为探究固体的组成,某化学兴趣小组进行了如图所示实验:
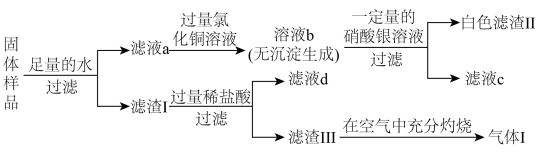
已知:①常温下,镁粉不与冷水反应;②滤液d的颜色为蓝色。
回答下列问题:
(1)滤渣Ⅰ的主要成分为炭粉、氧化铜和镁粉。
①写出一组碳元素的同素异形体:___________ 。
②少量的炭粉与氧化铜在高温条件下反应的化学方程式为___________ ,该反应中氧化剂与还原剂的质量之比为___________ 。
③查阅资料可知,镁粉在空气中燃烧会生成一种化学式为 的物质,该物质能与水发生反应,生成氢氧化镁和氨气,
的物质,该物质能与水发生反应,生成氢氧化镁和氨气, 与水发生反应的化学方程式为
与水发生反应的化学方程式为___________ 。
(2)由滤液a→溶液b可知,该固体中一定不含___________ (填化学式)。
(3)白色滤渣Ⅱ为___________ (填名称),___________ (填“能”或“不能”)判断该固体中含有氯化钾,判断的理由为___________ 。
(4)写出气体Ⅰ的一种用途:___________ 。

已知:①常温下,镁粉不与冷水反应;②滤液d的颜色为蓝色。
回答下列问题:
(1)滤渣Ⅰ的主要成分为炭粉、氧化铜和镁粉。
①写出一组碳元素的同素异形体:
②少量的炭粉与氧化铜在高温条件下反应的化学方程式为
③查阅资料可知,镁粉在空气中燃烧会生成一种化学式为
 的物质,该物质能与水发生反应,生成氢氧化镁和氨气,
的物质,该物质能与水发生反应,生成氢氧化镁和氨气, 与水发生反应的化学方程式为
与水发生反应的化学方程式为(2)由滤液a→溶液b可知,该固体中一定不含
(3)白色滤渣Ⅱ为
(4)写出气体Ⅰ的一种用途:
您最近一年使用:0次
2023-10-15更新
|
125次组卷
|
3卷引用:江西省南昌市等5地2023-2024学年高一上学期10月月考化学试题
名校
解题方法
8 . 现有原子序数依次增大的短周期主族元素W、P、Q,气体X、Y、Z分别为W、P、Q的单质,X、Y、Z之间能发生如图转换关系。已知化合物乙的水溶液常用于蚀刻玻璃,化合物乙与化合物甲反应可生成白烟。下列说法正确的是
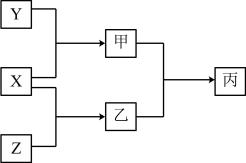

| A.W元素的氧化物中只存在极性共价键 |
| B.P元素的氧化物都是酸性氧化物 |
| C.化合物甲能使湿润的紫色石蕊试纸变红 |
| D.化合物甲和乙分子中所含电子总数相同 |
您最近一年使用:0次
解题方法
9 . X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色试验均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
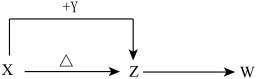
已知: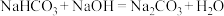 ;请回答:
;请回答:
(1)X生成Z的化学方程式是_______ 。
(2)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置III中产生白色沉淀,装置V中可收集到一种无色气体。
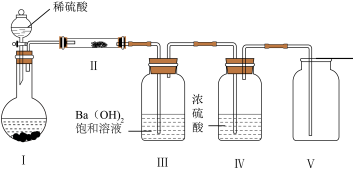
①装置II中物质的化学式是_______ 。
②装置I中盛放稀硫酸的仪器名称是_______ 。
(3)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是_______ 。
(4)为测定X和Z混合物中Z的质量分数,某课外小组取a g混合物充分加热,质量减少b g,则混合物中Z的质量分数是_______ (用含a、b的代数式表示)。

已知:
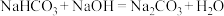 ;请回答:
;请回答:(1)X生成Z的化学方程式是
(2)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置III中产生白色沉淀,装置V中可收集到一种无色气体。

①装置II中物质的化学式是
②装置I中盛放稀硫酸的仪器名称是
(3)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是
(4)为测定X和Z混合物中Z的质量分数,某课外小组取a g混合物充分加热,质量减少b g,则混合物中Z的质量分数是
您最近一年使用:0次
名校
10 . 元素及其化合物知识在工农业生产、生活中被广泛使用,造福人类。
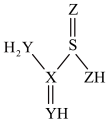
I.元素X、Y、Z和H、S元素组成的某种化合物(结构如图)常用作丝绸漂白剂,图中所有元素仅X、Y、Z同周期且原子序数依次增大。回答下列问题:
(1)Y元素的原子结构示意图为_______ ,该漂白剂所含元素非金属性最强的元素是在元素周期表中的位置为_______ 。
(2)下列说法错误的是_______(选填序号)。
II.该漂白剂中有两种元素的氢化物均可发生如下转化:
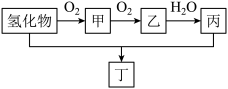
(3)若该氢化物的水溶液呈碱性,写出该氢化物的电子式为_______ 。图中该氢化物转化为甲的化学方程式_______ 。
(4)若该化合物的水溶液呈酸性,图中甲转化为乙的化学方程式为_____ 。该氢化物与丙的浓溶液反应,出现淡黄色浑浊且有刺激性气体放出。每生成1摩尔沉淀时,转移的电子数目为______ 。

I.元素X、Y、Z和H、S元素组成的某种化合物(结构如图)常用作丝绸漂白剂,图中所有元素仅X、Y、Z同周期且原子序数依次增大。回答下列问题:
(1)Y元素的原子结构示意图为
(2)下列说法错误的是_______(选填序号)。
A.原子半径: | B.简单气态氢化物稳定性: |
C.沸点: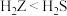 | D.该化合物中所有原子均为8电子稳定结构 |
II.该漂白剂中有两种元素的氢化物均可发生如下转化:

(3)若该氢化物的水溶液呈碱性,写出该氢化物的电子式为
(4)若该化合物的水溶液呈酸性,图中甲转化为乙的化学方程式为
您最近一年使用:0次



