某Q溶液中含有如表所示离子中的某5种且浓度均为0.5 (不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
(不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
已知:S2O + 2H+ = S + SO2 + H2O
+ 2H+ = S + SO2 + H2O
请回答下列问题:
(1)写出一种检验气体R的方法:______ 。写出产生气体R的离子方程式:______ 。
(2)由“向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变”可推知:Q溶液中一定不含表格中可能含有的8中阴离子中的___________ (填1-7数字)种阴离子。
(3)综合排断,Q溶液中一定含有的5种离子(浓度均为0.5 )分别为 :
)分别为 :______ (填离子符号,阳离子在前,阴离子在后)。
(4)取100ml的Q溶液与氯气充分反应,实验过程和结果如下:______ 。
②V的范围为:______ 。(格式写为m<V<n的形式)
 (不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。
(不考虑水的微弱电离与离子的单一水解)。向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变。| 阳离子 | 阴离子 |
 、 、 、 、 、 、 、 、 、 、 、 、 、 、 |  、 、 、 、 、 、 、 、 、 、 , , 、 、 |
 + 2H+ = S + SO2 + H2O
+ 2H+ = S + SO2 + H2O请回答下列问题:
(1)写出一种检验气体R的方法:
(2)由“向Q溶液中加入足量稀氢溴酸(HBr的水溶液),有气体R产生。经分析,加入前后阴离子的种类不变”可推知:Q溶液中一定不含表格中可能含有的8中阴离子中的
(3)综合排断,Q溶液中一定含有的5种离子(浓度均为0.5
 )分别为 :
)分别为 :(4)取100ml的Q溶液与氯气充分反应,实验过程和结果如下:

②V的范围为:
更新时间:2024-04-22 10:29:38
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】有A、B、C三种可溶性盐,阴、阳离子各不相同,三种盐的摩尔质量按A、B、C的顺序依次增大。将等物质的量的A、B、C溶于水,所得溶液中只含Fe3+、K+、NO 、SO
、SO 、Cl-五种离子(水的电离忽略不计),同时生成一种白色沉淀。请回答下列问题:
、Cl-五种离子(水的电离忽略不计),同时生成一种白色沉淀。请回答下列问题:
(1)经检验,这三种盐中还含有下列选项中的一种离子,该离子是_______ (填字母)。
(2)A的化学式是________ 。
(3)不需要加入任何试剂就能将上述三种盐溶液区分开来,鉴别出来的先后顺序为______ (用A、B、C表示),涉及的离子方程式是______ 。
(4)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Fe3+、SO 、NO
、NO 、K+四种离子(水的电离忽略不计),且Fe3+、SO
、K+四种离子(水的电离忽略不计),且Fe3+、SO 、NO
、NO 、K+的物质的量之比为1∶2∶3∶4,则A、B、C三种盐的物质的量之比为
、K+的物质的量之比为1∶2∶3∶4,则A、B、C三种盐的物质的量之比为_______ 。
(5)设计实验方案除去(4)中所得溶液中的Fe3+和SO (用流程图表示,如:原溶液
(用流程图表示,如:原溶液 溶液1
溶液1 溶液2)
溶液2)_______ 。
 、SO
、SO 、Cl-五种离子(水的电离忽略不计),同时生成一种白色沉淀。请回答下列问题:
、Cl-五种离子(水的电离忽略不计),同时生成一种白色沉淀。请回答下列问题:(1)经检验,这三种盐中还含有下列选项中的一种离子,该离子是
| A.Na+ | B.Mg2+ | C.Cu2+ | D.Ag+ |
(3)不需要加入任何试剂就能将上述三种盐溶液区分开来,鉴别出来的先后顺序为
(4)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Fe3+、SO
 、NO
、NO 、K+四种离子(水的电离忽略不计),且Fe3+、SO
、K+四种离子(水的电离忽略不计),且Fe3+、SO 、NO
、NO 、K+的物质的量之比为1∶2∶3∶4,则A、B、C三种盐的物质的量之比为
、K+的物质的量之比为1∶2∶3∶4,则A、B、C三种盐的物质的量之比为(5)设计实验方案除去(4)中所得溶液中的Fe3+和SO
 (用流程图表示,如:原溶液
(用流程图表示,如:原溶液 溶液1
溶液1 溶液2)
溶液2)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】回答下列问题。
(1)Fujta等学者开展了在Cu催化剂上进行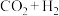 合成甲醇机理的研究。机理如下:
合成甲醇机理的研究。机理如下:___________ 。
(2)科学家设计了一种新的 可循环系统,可以实现温室气体的零排放,同时也回避了
可循环系统,可以实现温室气体的零排放,同时也回避了 的难储存问题,装置如下:
的难储存问题,装置如下:___________ 。
②b电极上的电极反应式为___________ ,如果将电解质溶液换为KOH溶液,对合成甲醇造成的不良后果是___________ 。
(3)常温下,向NaOH溶液中逐渐通入 气体,溶液中由水电离的
气体,溶液中由水电离的 随着
随着 通入体积的变化曲线如图所示:
通入体积的变化曲线如图所示:___________ 。
②比较pH:b___________ d(填“>”“<”或“=”)。
③向a、b、c、d四点溶液中加入少量等质量的 固体后,溶液漂白性最强的点是
固体后,溶液漂白性最强的点是___________ 。
(4)向含有 、
、 、
、 、
、 四种离子的溶液中加入少量
四种离子的溶液中加入少量 固体后,这四种离子中离子数目肯定增加的是
固体后,这四种离子中离子数目肯定增加的是___________ 。
(1)Fujta等学者开展了在Cu催化剂上进行
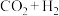 合成甲醇机理的研究。机理如下:
合成甲醇机理的研究。机理如下: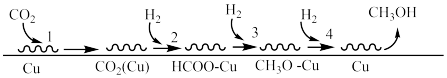
(2)科学家设计了一种新的
 可循环系统,可以实现温室气体的零排放,同时也回避了
可循环系统,可以实现温室气体的零排放,同时也回避了 的难储存问题,装置如下:
的难储存问题,装置如下: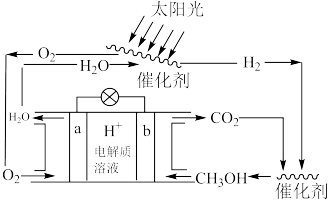
②b电极上的电极反应式为
(3)常温下,向NaOH溶液中逐渐通入
 气体,溶液中由水电离的
气体,溶液中由水电离的 随着
随着 通入体积的变化曲线如图所示:
通入体积的变化曲线如图所示:
②比较pH:b
③向a、b、c、d四点溶液中加入少量等质量的
 固体后,溶液漂白性最强的点是
固体后,溶液漂白性最强的点是(4)向含有
 、
、 、
、 、
、 四种离子的溶液中加入少量
四种离子的溶液中加入少量 固体后,这四种离子中离子数目肯定增加的是
固体后,这四种离子中离子数目肯定增加的是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】某溶液中,可能含有下表所列离子中的某几种:
取少量该溶液,向其中加入某试剂X,产生沉淀的物质的量(n)与加入试剂X的体积(V)关系如下图所示:
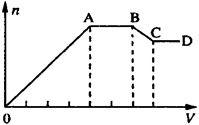
(1)若X是NaOH溶液,原溶液中一定含有的阴离子有___________ ;BC段反应的离子方程式为___________ 。
(2)若X是盐酸,则原溶液中一定含有的金属阳离子是___________ ;AB段发生反应的总离子方程式为___________ ;OA段生成沉淀的物质的量之比为___________ 。
| 阳离子 | Al3+、Mg2+、NH 、Na+ 、Na+ |
| 阴离子 | CO 、SiO 、SiO 、[Al(OH)4]-、Cl- 、[Al(OH)4]-、Cl- |

(1)若X是NaOH溶液,原溶液中一定含有的阴离子有
(2)若X是盐酸,则原溶液中一定含有的金属阳离子是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】探究无机盐X(仅含三种短周期元素)的组成和性质,设计并完成如下实验:

请回答:
(1)X的化学式是____ 。
(2)白色粉末溶于氢氧化钠溶液的离子方程式是____ 。
(3)高温条件下白色粉末与焦炭发生置换反应,写出该反应的化学方程式____ 。

请回答:
(1)X的化学式是
(2)白色粉末溶于氢氧化钠溶液的离子方程式是
(3)高温条件下白色粉末与焦炭发生置换反应,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】为探究某矿物的主要成分X(仅含三种元素)的组成,某兴趣小组进行了如下实验:
①取55.2g固体X在空气存在下高温煅烧,有刺激性气味的气体产生(标况下为13.44L),该 气体能使品红溶液褪色。
②高温煅烧后的固体用磁分离技术进行分离,得到19.2g红色固体单质和23.2g 黑色固体。
③将23.2g固体溶于稀硫酸,再加氢氧化钠,将所得沉淀充分灼烧,得到24g 红棕色固体。 已知各步反应试剂均过量,请回答:
(1)X化学式为______
(2)写出X在空气存在下高温煅烧的化学反应方程式______
(3)写出X高温煅烧后的气体通入碘水中发生的离子反应方程式______
①取55.2g固体X在空气存在下高温煅烧,有刺激性气味的气体产生(标况下为13.44L),该 气体能使品红溶液褪色。
②高温煅烧后的固体用磁分离技术进行分离,得到19.2g红色固体单质和23.2g 黑色固体。
③将23.2g固体溶于稀硫酸,再加氢氧化钠,将所得沉淀充分灼烧,得到24g 红棕色固体。 已知各步反应试剂均过量,请回答:
(1)X化学式为
(2)写出X在空气存在下高温煅烧的化学反应方程式
(3)写出X高温煅烧后的气体通入碘水中发生的离子反应方程式
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
【推荐3】某待测溶液中可能含有 、
、 、
、 、
、 、
、 、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出)。
、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出)。
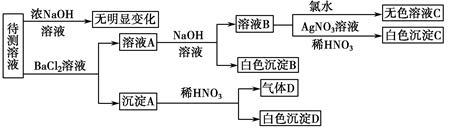
请回答下列问题:(1)根据上述框图信息填写下表(不能确定的不填):
(2)写出沉淀A三种可能的情况:______________________________ ,若气体D遇空气变红棕色,则生成沉淀D时肯定发生的反应的离子方程式为________________ 。
(3)若Mn+位于第三周期,则要确定它具体是何种离子的方法是_____________________ 。
 、
、 、
、 、
、 、
、 、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出)。
、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出)。
请回答下列问题:(1)根据上述框图信息填写下表(不能确定的不填):
| 肯定存在的离子 | 肯定没有的离子 | |
| 化学式或离子符号 |
(3)若Mn+位于第三周期,则要确定它具体是何种离子的方法是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知A、B、C和甲、乙、丙均是由短周期元素形成的物质,D是过渡元素形成的常见单质,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)
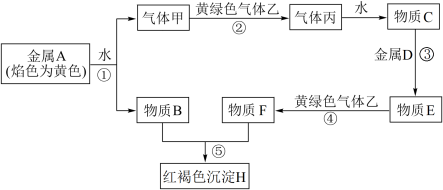
请回答下列问题:
(1)丙的电子式为_____ ;组成气体乙的元素在周期表的位置____ ;物质B含有的化学键类型是______ ;
(2)写出下列反应的离子方程式:
④_________________________ ;
⑤_____________________ ;
(3)金属D与稀硝酸反应,产生标准状况下1.12L的NO气体,则参加反应的硝酸为_______ mol。

请回答下列问题:
(1)丙的电子式为
(2)写出下列反应的离子方程式:
④
⑤
(3)金属D与稀硝酸反应,产生标准状况下1.12L的NO气体,则参加反应的硝酸为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】为了证明铜与稀硝酸反应产生NO,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
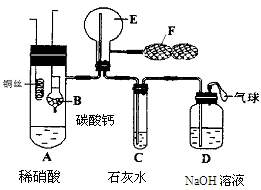
(1) 实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为____ 。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为________________________________________ 。
(3)装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是______________________________________ 。
(4)一段时间后,C中白色沉淀溶解,其原因是________________________ 。
(5)装置D的作用是___________________________________________ 。

(1) 实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为
(3)装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是
(4)一段时间后,C中白色沉淀溶解,其原因是
(5)装置D的作用是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】氨元素是动植物生长不可缺少的元素,图1是自然界中氨元素的循环示意图,图2是氨元素的常见化合价与部分物质类别的对应关系。回答下列问题:
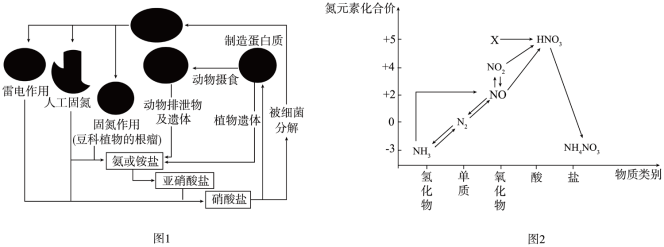
(1)图1中属于固氮过程的是_______ (写两种即可)。
(2) 可以将
可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁。
。某学习小组欲制备氨气以还原氧化铁。
①下列各装置中常用于实验室制备氨气的是_______ (填字母),利用该装置制备氨气的化学方程式为_______ 。
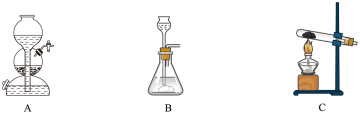
② 还原
还原 并检验有水生成的实验装置如图所示:
并检验有水生成的实验装置如图所示:
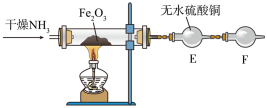
写出氨气与氧化铁反应的化学方程式:_______ 。干燥管F中装有无水氯化钙,其作用是_______ 。
(3)图2中物质X的化学式是_______ ,其与水反应生成 。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为
。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为 ,硝酸的浓度为
,硝酸的浓度为 ,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
,现向其中加入9.6g铜粉,充分反应生成气体的化学式为_______ (假设只生成一种气体),最多可收集到标准状况下的该气体的体积为_______ L。

(1)图1中属于固氮过程的是
(2)
 可以将
可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁。
。某学习小组欲制备氨气以还原氧化铁。①下列各装置中常用于实验室制备氨气的是

②
 还原
还原 并检验有水生成的实验装置如图所示:
并检验有水生成的实验装置如图所示:
写出氨气与氧化铁反应的化学方程式:
(3)图2中物质X的化学式是
 。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为
。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为 ,硝酸的浓度为
,硝酸的浓度为 ,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】填空。
(1)由几种离子组成的混合物中可能含有下列离子中的若干种: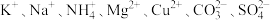 。将该混合物溶于水后得到澄清的溶液,现取三份各
。将该混合物溶于水后得到澄清的溶液,现取三份各 该溶液分别进行如下实验:
该溶液分别进行如下实验:
请回答下列问题:
①实验1说明存在的离子是_______ (填离子符号,下同),一定不存在的离子是_______ 。
②溶液中 的范围是
的范围是_______ 。
(2)电解质溶于水时会发生电离产生自由移动的离子,电导率变化一定程度上可以反映溶液中自由移动的离子浓度变化。在两份相同的 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的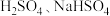 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
下列分析正确的是_______。
(3)甲同学认为(1)实验3能证明溶液中存在 ,乙同学认为不能证明。那么甲同学如何利用题目涉及药品证明溶液中一定存在
,乙同学认为不能证明。那么甲同学如何利用题目涉及药品证明溶液中一定存在 :
:_______ 。
(1)由几种离子组成的混合物中可能含有下列离子中的若干种:
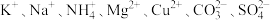 。将该混合物溶于水后得到澄清的溶液,现取三份各
。将该混合物溶于水后得到澄清的溶液,现取三份各 该溶液分别进行如下实验:
该溶液分别进行如下实验:| 实验序号 | 实验内容 | 实验结果 |
| 1 | 加入盐酸 | 有气泡产生 |
| 2 | 加入足量浓 溶液并加热 溶液并加热 | 收集到标准状况下的气体 |
| 3 | 加入足量 溶液,对所得沉淀进行洗涤、干燥、称量; 溶液,对所得沉淀进行洗涤、干燥、称量; | 第一次称量读数为 ;再向沉淀中加入足量盐酸,然后过滤、洗涤、干燥、称量,第二次称量读数为 ;再向沉淀中加入足量盐酸,然后过滤、洗涤、干燥、称量,第二次称量读数为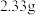 |
①实验1说明存在的离子是
②溶液中
 的范围是
的范围是(2)电解质溶于水时会发生电离产生自由移动的离子,电导率变化一定程度上可以反映溶液中自由移动的离子浓度变化。在两份相同的
 溶液中,分别滴入物质的量浓度相等的
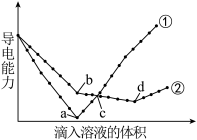
溶液中,分别滴入物质的量浓度相等的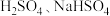 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
下列分析正确的是_______。
A.①代表滴加 溶液的变化曲线 溶液的变化曲线 |
B.b点,溶液中大量存在的离子是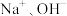 |
| C.a、d两点对应的溶液均显中性 |
D. 导电能力比 导电能力比 弱 弱 |
 ,乙同学认为不能证明。那么甲同学如何利用题目涉及药品证明溶液中一定存在
,乙同学认为不能证明。那么甲同学如何利用题目涉及药品证明溶液中一定存在 :
:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某化学学习小组在帮助老师整理实验室的化学试剂时,发现一盛无色盐溶液的试剂瓶,标签破损如右图,该小组根据已掌握的知识,对药品作出猜想,并设计实验验证。

(1)该实验药品为中学化学常用试剂,推测它的阳离子化合价为______________________ 。
(2)同学们做出以下三种推测。
猜想1:Na2SO4
实验设计: 进行……,.证明是Na2SO4溶液;
猜想2: K2SO4
实验设计:____________________________ ,证明是K2SO4溶液;
猜想3; (NH4)2SO4
实验设计:____________________________ ,证明是(NH4)2SO4溶液。
(3)通过实验发现“猜想3”成立,已知(NH4)2SO4受热易分解,该小组拟用下图所示装置探究其分解产物。(夹持和加热装置略)
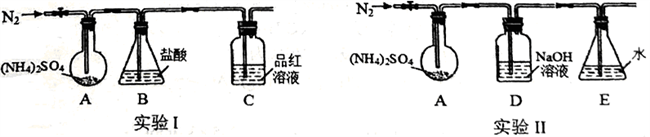
实验I:装置B 盛0.5000mol/L盐酸50.00mL,通入N2排尽空气后,将装置A 加热至260℃一段时间,停止加热,停止通入N2,品红溶液不褪色,取下装置B,用0.1000mol/LNaOH溶液滴定剩余盐酸,消耗NaOH 溶液50.00mL。经检验滴定后的溶液中无SO42-。
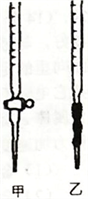
①请从右图选择盛放0.1000mol/LNaOH 溶液的滴定管____________ (填“甲”或“乙”)。
②装置B 内溶液吸收气体的物质的量是_____________________ mol。
实验Ⅱ:通入N2排尽空气后,将装置A 加热到400℃,至固体无残留,停止加热,停止通入N2,观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。
①装置E 的作用是____________________________ 。
②A、D之间的导气管内的少量白色固体是____________________________ 。
③有同学提出在AD之间需要增加一个防倒吸的安全瓶,老师说不需要,原因是____________________________ 。
④进一步研究发现,气体产物中无氮氧化物,则(NH4)2SO4在400℃分解的化学方程式是_______________________________ 。

(1)该实验药品为中学化学常用试剂,推测它的阳离子化合价为
(2)同学们做出以下三种推测。
猜想1:Na2SO4
实验设计: 进行……,.证明是Na2SO4溶液;
猜想2: K2SO4
实验设计:
猜想3; (NH4)2SO4
实验设计:
(3)通过实验发现“猜想3”成立,已知(NH4)2SO4受热易分解,该小组拟用下图所示装置探究其分解产物。(夹持和加热装置略)

实验I:装置B 盛0.5000mol/L盐酸50.00mL,通入N2排尽空气后,将装置A 加热至260℃一段时间,停止加热,停止通入N2,品红溶液不褪色,取下装置B,用0.1000mol/LNaOH溶液滴定剩余盐酸,消耗NaOH 溶液50.00mL。经检验滴定后的溶液中无SO42-。

①请从右图选择盛放0.1000mol/LNaOH 溶液的滴定管
②装置B 内溶液吸收气体的物质的量是
实验Ⅱ:通入N2排尽空气后,将装置A 加热到400℃,至固体无残留,停止加热,停止通入N2,观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。
①装置E 的作用是
②A、D之间的导气管内的少量白色固体是
③有同学提出在AD之间需要增加一个防倒吸的安全瓶,老师说不需要,原因是
④进一步研究发现,气体产物中无氮氧化物,则(NH4)2SO4在400℃分解的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】已知l00mL某无色溶液X可能由K+、Mg2+、Ba2+、Al3+、Fe2+、AlO2-、CO32-、SO42-、I-、SiO32-、MnO4-中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成:
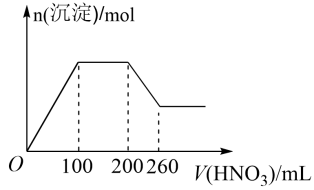
I .取适量该溶液,加入过量1.0 mol·L-1的硝酸,有气体生成,并得到无色溶液。该过程中产生沉淀的物质的量与加入的硝酸溶液体积的关系如上图所示。
II.将I过滤,在所得滤液中再加入过量的碳酸氢铵溶液,有气体生成,析出白色沉淀A;
III.在II所得溶液中逐滴加入氢氧化钡溶液至过量,加热有气体生成,同时析出白色沉淀B;
IV.向沉淀B中加入过量稀盐酸,沉淀部分溶解,将剩余沉淀过滤、洗涤、干燥后称重为2.33克,
根据以上实验事实推断:
(1)原溶液中一定含有的离子是___________________________ 。
(2)上述实验步骤II中产生白色沉淀A的离子方程式是________________________ 。
(3)白色沉淀B的成分是______________________________ 。
(4)原溶液中阳离子物质的量浓度为_____________________________ 。

I .取适量该溶液,加入过量1.0 mol·L-1的硝酸,有气体生成,并得到无色溶液。该过程中产生沉淀的物质的量与加入的硝酸溶液体积的关系如上图所示。
II.将I过滤,在所得滤液中再加入过量的碳酸氢铵溶液,有气体生成,析出白色沉淀A;
III.在II所得溶液中逐滴加入氢氧化钡溶液至过量,加热有气体生成,同时析出白色沉淀B;
IV.向沉淀B中加入过量稀盐酸,沉淀部分溶解,将剩余沉淀过滤、洗涤、干燥后称重为2.33克,
根据以上实验事实推断:
(1)原溶液中一定含有的离子是
(2)上述实验步骤II中产生白色沉淀A的离子方程式是
(3)白色沉淀B的成分是
(4)原溶液中阳离子物质的量浓度为
您最近一年使用:0次



