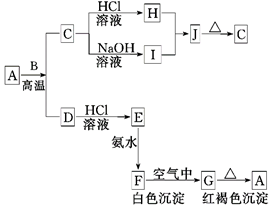
探究无机盐X(仅含三种短周期元素)的组成和性质,设计并完成如下实验:

请回答:
(1)X的化学式是____ 。
(2)白色粉末溶于氢氧化钠溶液的离子方程式是____ 。
(3)高温条件下白色粉末与焦炭发生置换反应,写出该反应的化学方程式____ 。

请回答:
(1)X的化学式是
(2)白色粉末溶于氢氧化钠溶液的离子方程式是
(3)高温条件下白色粉末与焦炭发生置换反应,写出该反应的化学方程式
更新时间:2017-08-09 21:28:03
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】X是一种由4种短周期元素组成含结晶水的盐。某兴趣小组按如下流程进行实验(所用试剂均足量):
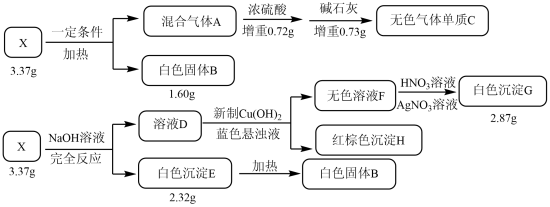
其中:X微溶于水。溶液D中仅有一种溶质。红棕色沉淀H是一种钠盐。请回答:
(1)组成X的元素有_______ ,X的化学式为_______ 。
(2)无色溶液F中的溶质是(用化学式表示):_______ 。
(3)上图生红棕色沉淀H时,溶液D中的溶质与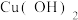 的物质的量之比为1:2,则其离子反应方程式是
的物质的量之比为1:2,则其离子反应方程式是_______ 。
(4)设计实验验证溶液D中的阴离子_______ 。

其中:X微溶于水。溶液D中仅有一种溶质。红棕色沉淀H是一种钠盐。请回答:
(1)组成X的元素有
(2)无色溶液F中的溶质是(用化学式表示):
(3)上图生红棕色沉淀H时,溶液D中的溶质与
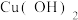 的物质的量之比为1:2,则其离子反应方程式是
的物质的量之比为1:2,则其离子反应方程式是(4)设计实验验证溶液D中的阴离子
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
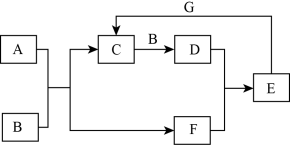
【推荐2】在如图所示的物质转化关系中,A是常见的气态氢化物,也是一种重要的化工产品、化工原料,B是能使带火星的木条复燃的无色、无味气体,E的相对分子质量比D的大17,合成A以及制取E的流程示意图如图所示,G是一种紫红色金属单质(反应条件和部分生成物未列出)。_______ 。
(2)反应A+B→C的化学方程式_______ 。
(3)反应E+G→C的离子反应方程式_______ 。
(4)D+F→E中氧化剂和还原剂的物质的量之比为_______ 。
(5)实验室保存E的浓溶液时用棕色试剂瓶,请用化学方程式解释原因__________ 。
(6)有一瓶稀硫酸和稀硝酸的混合溶液,其中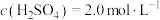 ,
,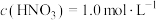 。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为_______ L。
(2)反应A+B→C的化学方程式
(3)反应E+G→C的离子反应方程式
(4)D+F→E中氧化剂和还原剂的物质的量之比为
(5)实验室保存E的浓溶液时用棕色试剂瓶,请用化学方程式解释原因
(6)有一瓶稀硫酸和稀硝酸的混合溶液,其中
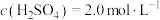 ,
,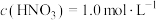 。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料生产铝和氮化铝的一种工艺流程如下【已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀】。
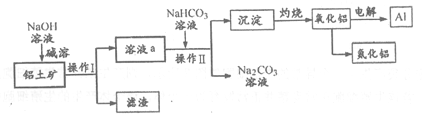
(1)操作I、Ⅱ的名称为____________ 。
(2)用氧化物的形式表示铝硅酸钠的化学式_____________ 。
(3)溶液a中加入NaHCO3后,生成沉淀的离子方程式为____________ 。
(4)Al2O3比另外一种铝的化合物AlCl3熔点高出很多,原因是_________ ; 有人考虑用熔融态AlCl3电解制备铝,你觉得是否可行,____ (选填“可行”或“不可行”),试分析原因_________ 。
(5)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开K2,加入NaOH浓溶液,至不再产生NH3。打开K1,通入N2一段时间。
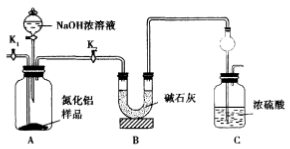
①实验中需要测定的数据是___________ 。
②由于装置存在缺陷,导致测定结果偏高,请提出改进方法:___________ 。

(1)操作I、Ⅱ的名称为
(2)用氧化物的形式表示铝硅酸钠的化学式
(3)溶液a中加入NaHCO3后,生成沉淀的离子方程式为
(4)Al2O3比另外一种铝的化合物AlCl3熔点高出很多,原因是
(5)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开K2,加入NaOH浓溶液,至不再产生NH3。打开K1,通入N2一段时间。

①实验中需要测定的数据是
②由于装置存在缺陷,导致测定结果偏高,请提出改进方法:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】石英砂岩,是硅石中的一种,其主要化学成分可简单表示为MgAl4Si10O26(OH)2 (假设杂质均能溶于硫酸),工业上拟用该物质为原料制备高纯度硅,其艺流程如图所示:
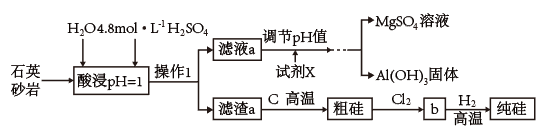
(1)请将石英砂岩的组成用氧化物的形式表示:________________ ,酸浸时,为了提高浸取率可采取的措施有______________________________________ 。 (答出两点)
(2)实验室用18.4mol· L-1的浓硫酸配制250mL4.8mol· L -1的硫酸,需量取浓硫酸_______ mL (结果保留一位小数);配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需__________________________ 。
(3)制备高纯硅的过程中需要用到Cl2,请写出实验室制备Cl2的离子反应方程式:______________ 。
(4)请写出b 和H2反应的化学方程式,并用单线桥法表示该反应过程中电子的转移:_______________ 。
(5)通过实验测得滤液a中c(Al3+)=1.0mol· L-1,c(Mg2+)=0.28mol· L-1,某同学打算通过调节溶液的pH值使Al3+和Mg2+完全分离(当离子浓度降到1.0×10-6mol· L-1时即视为完全分离),则试剂X 用_______ (填“0.1mol· L-1NaOH 或“0.1mol· L-1氨水”)较好;沉淀时应控制溶液的pH值的取值范围为_______ (已知: KspAl(OH)3=8.0×10-33,Ksp[Mg(OH)2]=2.8×10-11,lg2=0.3,lg5=0.7)。

(1)请将石英砂岩的组成用氧化物的形式表示:
(2)实验室用18.4mol· L-1的浓硫酸配制250mL4.8mol· L -1的硫酸,需量取浓硫酸
(3)制备高纯硅的过程中需要用到Cl2,请写出实验室制备Cl2的离子反应方程式:
(4)请写出b 和H2反应的化学方程式,并用单线桥法表示该反应过程中电子的转移:
(5)通过实验测得滤液a中c(Al3+)=1.0mol· L-1,c(Mg2+)=0.28mol· L-1,某同学打算通过调节溶液的pH值使Al3+和Mg2+完全分离(当离子浓度降到1.0×10-6mol· L-1时即视为完全分离),则试剂X 用
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】铁橄榄石是天然的铁矿石,由实验测得铁橄榄石的摩尔质量为204 g·mol-1,其中铁元素的质量分数为54.9%,可以通过如下反应和相应的数据推知它的化学式。其中A ~ J是中学化学中的常见物质,G是一种红褐色固体,D是一种难溶于水的含氧酸,J是一种主要的温室气体,A为强碱,其焰色反应呈黄色,E和B分别与酸化的硝酸银溶液反应时的实验现象相同,均有白色沉淀产生,流程中的部分生成物已略去。
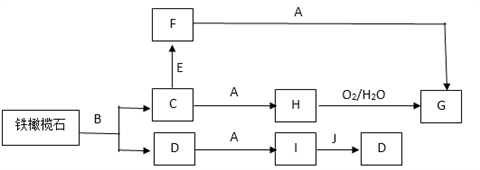
回答下列问题:
(1)A的电子式:__________________ 。
(2)铁橄榄石的化学式:__________________ 。
(3)写出H → G的化学方程式:__________________ 。

回答下列问题:
(1)A的电子式:
(2)铁橄榄石的化学式:
(3)写出H → G的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】天空课堂第二课中航天员展示了金属锆(40Zr)在无容器实验柜中从液体变成固体时的“再辉”现象。以锆英石(主要成分是ZrSiO4,还含有少量Al2O3、SiO2、Fe2O3等杂质)为原料生产锆的流程如图所示:
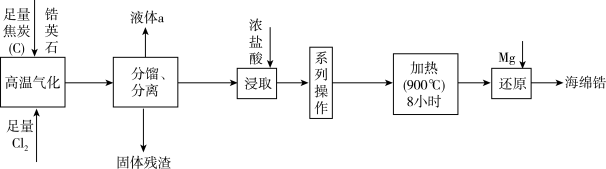
已知:常温下,ZrCl4是白色固体, 604K升华,遇水强烈水解:ZrCl4+9H2O=ZrOCl2·8H2O+2HCl,在浓盐酸中会析出ZrOCl2·8H2O沉淀。请回答下列问题:
(1)“高温气化”中可发生多个反应,写出发生的主要反应的化学方程式是_______ 。
(2)分馏过程中,为防止产品变质,过程中一定需要注意的是_______ 。液体a的电子式是_______ 。
(3)实验室中洗涤ZrOCl2·8H2O沉淀操作是_______ 。
(4)“还原”中氧化剂是_______ (填化学式)。
(5)由于锆铪(Hf)矿石共生,这样制得的锆中常含有少量的铪,需要进一步分离提纯。
第一步:溶解分离
将样品溶于氢氟酸后再加入一定量KOH溶液,锆和铪均以[MF6]2-存在。
①已知在水中K2HfF6比K2ZrF6的溶解度大,且K2ZrF6的溶解度随温度的升高而增大,可以利用_______
方法进行分离。
②离子交换法:利用强碱型酚醛树脂R-N(CH3) Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是
Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是_______ 。
③将所得溶液与有机相磷酸三丁酯(TBP)充分混合、振荡,可以达到Zr与Hf分离。这种分离方法是_______ 。
第二步:高温还原
在高温条件下,加入铝将制得的K2ZrF6还原可得锆,反应的化学方程式是_______ 。

已知:常温下,ZrCl4是白色固体, 604K升华,遇水强烈水解:ZrCl4+9H2O=ZrOCl2·8H2O+2HCl,在浓盐酸中会析出ZrOCl2·8H2O沉淀。请回答下列问题:
(1)“高温气化”中可发生多个反应,写出发生的主要反应的化学方程式是
(2)分馏过程中,为防止产品变质,过程中一定需要注意的是
(3)实验室中洗涤ZrOCl2·8H2O沉淀操作是
(4)“还原”中氧化剂是
(5)由于锆铪(Hf)矿石共生,这样制得的锆中常含有少量的铪,需要进一步分离提纯。
第一步:溶解分离
将样品溶于氢氟酸后再加入一定量KOH溶液,锆和铪均以[MF6]2-存在。
①已知在水中K2HfF6比K2ZrF6的溶解度大,且K2ZrF6的溶解度随温度的升高而增大,可以利用
方法进行分离。
②离子交换法:利用强碱型酚醛树脂R-N(CH3)
 Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是
Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是③将所得溶液与有机相磷酸三丁酯(TBP)充分混合、振荡,可以达到Zr与Hf分离。这种分离方法是
第二步:高温还原
在高温条件下,加入铝将制得的K2ZrF6还原可得锆,反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍;F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为_________________ ,反应④的化学方程式为________________________ 。
(2)若A为常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是_____________________________________________ 。
(3)若A、D、F都是由短周期非金属元素形成的单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为__________________________________ 。

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍;F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为
(2)若A为常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是
(3)若A、D、F都是由短周期非金属元素形成的单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】某科研小组探究工业废Cu粉(杂质可能含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4·5H2O,实现废物综合利用。他们进行了两组实验,过程如下:
Ⅰ:
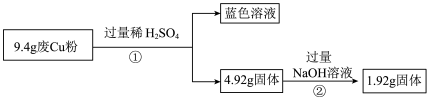
Ⅱ:
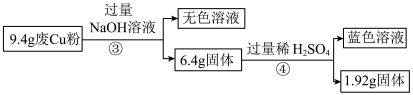
(1)废Cu粉中含有的杂质是________________ 。
(2)分别写出过程①③中发生反应的离子方程式:
①________________________________ 。
③________________________________ 。
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是________ (可不必化简)。
(4)已知25℃时:
从Ⅱ中所得蓝色溶液中分离提纯得到CuSO4·5H2O晶体,需要经过下列步骤:
a、向蓝色溶液中加入一定量的H2O2溶液;
b、调节溶液的pH为__________ 之间;
c、然后过滤、结晶,再过滤,可得CuSO4·5H2O
下列关于实验操作的叙述中,正确的是__________ (填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.上述步骤c中第一次过滤是为了得到滤液,第二次过滤是为了得到固体
D.在pH >4的溶液中Fe3+一定不能大量存在
Ⅰ:

Ⅱ:

(1)废Cu粉中含有的杂质是
(2)分别写出过程①③中发生反应的离子方程式:
①
③
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是
(4)已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
从Ⅱ中所得蓝色溶液中分离提纯得到CuSO4·5H2O晶体,需要经过下列步骤:
a、向蓝色溶液中加入一定量的H2O2溶液;
b、调节溶液的pH为
c、然后过滤、结晶,再过滤,可得CuSO4·5H2O
下列关于实验操作的叙述中,正确的是
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.上述步骤c中第一次过滤是为了得到滤液,第二次过滤是为了得到固体
D.在pH >4的溶液中Fe3+一定不能大量存在
您最近一年使用:0次