名校
1 . 在无机非金属材料中,硅扮演着重要的角色。下列有关硅及其化合物的说法中正确的是
A.制备粗硅的化学方程式为: |
B.硅胶可作瓶装药品的干燥剂及催化剂载体,是因为 是酸性氧化物 是酸性氧化物 |
C. 既可以与NaOH溶液反应,又可以与HF溶液反应 既可以与NaOH溶液反应,又可以与HF溶液反应 |
D.青花瓷胎体的原料为高岭土[ ],若以氧化物形式可表示为 ],若以氧化物形式可表示为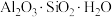 |
您最近半年使用:0次
名校
解题方法
2 . 下列离子方程式书写正确的是
A.向稀硫酸中加入铜粉: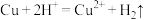 |
B.向稀硝酸中加入少量小苏打: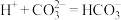 |
C. 与稀盐酸反应: 与稀盐酸反应: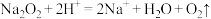 |
D.盛装NaOH溶液的试剂瓶不能用磨口玻璃塞: |
您最近半年使用:0次
3 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括陶瓷、水泥和玻璃,其中制玻璃的主要原料为_______ 。
(2)下列溶液的存放不能使用磨口玻璃塞的是_______ (填序号)。
①浓硝酸 ② 溶液 ③
溶液 ③ 溶液 ④澄清石灰水 ⑤
溶液 ④澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液
(3)关于硅及其相关化合物的叙述正确的是_______ (填字母)。
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于CO2+H2O=H2CO3,用类比法可知,SiO2+H2O=H2SiO3
C.无机非金属材料AlN熔沸点很高,可作为耐高温材料制作特定仪器
D.保存氢氟酸可用玻璃瓶,但不能用玻璃塞
E. 既能和
既能和 溶液反应,又能和氢氟酸反应,所以是两性氧化物
溶液反应,又能和氢氟酸反应,所以是两性氧化物
F.高纯硅可用于制作光导纤维
(4)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:_______ 。
②上述工艺生产中循环使用的物质除Si、SiHCl3外,还有_______ 。
③整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式_______ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是_______ 。
(5)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下: 3SiO2+6C+2N2 Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为
Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为_______  。
。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括陶瓷、水泥和玻璃,其中制玻璃的主要原料为
(2)下列溶液的存放不能使用磨口玻璃塞的是
①浓硝酸 ②
 溶液 ③
溶液 ③ 溶液 ④澄清石灰水 ⑤
溶液 ④澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液(3)关于硅及其相关化合物的叙述正确的是
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于CO2+H2O=H2CO3,用类比法可知,SiO2+H2O=H2SiO3
C.无机非金属材料AlN熔沸点很高,可作为耐高温材料制作特定仪器
D.保存氢氟酸可用玻璃瓶,但不能用玻璃塞
E.
 既能和
既能和 溶液反应,又能和氢氟酸反应,所以是两性氧化物
溶液反应,又能和氢氟酸反应,所以是两性氧化物F.高纯硅可用于制作光导纤维
(4)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:

②上述工艺生产中循环使用的物质除Si、SiHCl3外,还有
③整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是(5)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下: 3SiO2+6C+2N2
 Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为
Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为 。
。
您最近半年使用:0次
4 . 化学知识的应用与我们生产、生活及生产材料密切相关,在我国传统文化中也有很多的记载,下列有关说法合理的是
| A.用纳米技术催化CO2合成可降解塑料聚碳酸酯,可实现“碳”的循环利用 |
| B.半导体行业有这样一句话:“从沙滩到用户”,包含了粗硅的制备反应,该反应说明碳元素的非金属性比硅元素强。 |
| C.“墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”是一种分散质 |
| D.航母舰体材料为合金钢,舰体在海水中发生的电化学腐蚀主要是析氢腐蚀 |
您最近半年使用:0次
名校
解题方法
5 . 下列反应的离子或化学方程式正确的是
A.向NaHS溶液中滴加少量的 溶液: 溶液: |
B.用石英和焦炭制取粗硅: |
C. 溶液中滴入 溶液中滴入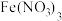 溶液: 溶液: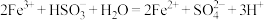 |
D.将 通入NaClO溶液中: 通入NaClO溶液中: |
您最近半年使用:0次
6 . 根据所学过的化学知识判断,下列说法正确的是
| A.SiO2是酸性氧化物,不与任何酸反应 |
| B.镁条在空气中燃烧可生成三种产物 |
| C.在高温高压和催化剂下,硫可与氧气直接化合生成SO3 |
| D.1molSO3和1molNO2分别通入1L水中产生相同浓度的硫酸和硝酸 |
您最近半年使用:0次
7 . 下列说法正确的是
A. 与水反应、红热的 与水反应、红热的 与水蒸气反应均能生成碱 与水蒸气反应均能生成碱 |
B.将 通入 通入 溶液中,无沉淀产生;再通入足量 溶液中,无沉淀产生;再通入足量 ,产生沉淀 ,产生沉淀 |
C.两性氧化物 既可以与氢氧化钠溶液反应,又可溶于氢氟酸溶液 既可以与氢氧化钠溶液反应,又可溶于氢氟酸溶液 |
D.在稀硫酸中加入铜粉,铜粉不溶解;再加入 固体,铜粉仍不溶解 固体,铜粉仍不溶解 |
您最近半年使用:0次
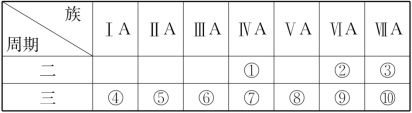
8 . I.1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:_______ (任写一种)。
(2)请写出元素⑦的氧化物与元素③的氢化物的水溶液反应的化学方程式_______ 。
(3)元素①和元素⑦最高价氧化物的水化物中酸性较强的是_______ (填化学式)。
II.硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(4)硅元素在自然界中通常以石英石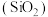 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式_______ 。 的SiO2中含有Si-O键
的SiO2中含有Si-O键_______ 个。
(5)高纯硅单质可由石英砂(主要成分是 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:_______ ;
ii.流程①焦炭体现了_______ (填“氧化性”或“还原性”);
iii.由于硅酸盐组成比较复杂,通常用氧化物的形式表示:请用氧化物的形式表示钾云母K(Al3Si3O10)(OH)2的组成_______ 。
(2)请写出元素⑦的氧化物与元素③的氢化物的水溶液反应的化学方程式
(3)元素①和元素⑦最高价氧化物的水化物中酸性较强的是
II.硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(4)硅元素在自然界中通常以石英石
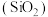 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式 的SiO2中含有Si-O键
的SiO2中含有Si-O键(5)高纯硅单质可由石英砂(主要成分是
 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:
ii.流程①焦炭体现了
iii.由于硅酸盐组成比较复杂,通常用氧化物的形式表示:请用氧化物的形式表示钾云母K(Al3Si3O10)(OH)2的组成
您最近半年使用:0次
9 . 下列物质之间的转化都一步能实现的是
A.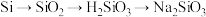 |
B. →Na[Al(OH)4] →Na[Al(OH)4] |
C.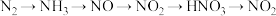 |
D. |
您最近半年使用:0次
10 . 下列元素化合物的转化关系中,可以实现的是
A.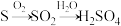 |
B.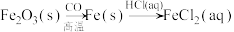 |
C.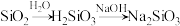 |
D. |
您最近半年使用:0次



